Clear Sky Science · es
Una vía libre de cianuro hacia la electrosíntesis de nitrilos
Limpiando un rincón oculto de la química
Los nitrilos son trabajadores silenciosos de la vida moderna; están presentes en medicamentos, plásticos, colorantes y productos agrícolas. Sin embargo, su producción a escala industrial suele emitir dióxido de carbono, óxidos de nitrógeno e incluso cianuro tóxico. Este estudio presenta un método para fabricar nitrilos usando electricidad y un catalizador modesto en lugar de calor intenso o reactivos venenosos, lo que apunta a fábricas más limpias que podrían incluso reutilizar sus propios gases residuales.

Por qué las rutas actuales generan problemas
La industria normalmente obtiene nitrilos calentando compuestos sencillos con amoníaco y oxígeno a varios cientos de grados Celsius. Esas condiciones ígneas son difíciles de controlar, por lo que parte de la materia prima se quema hasta dióxido de carbono y óxidos de nitrógeno. Rutas alternativas sustituyen el calor por química que emplea grandes cantidades de sales de cianuro, muy tóxicas y difíciles de manejar con seguridad a escala. Con millones de toneladas de cianuro utilizadas cada año, incluso pequeñas ineficiencias dejan residuos peligrosos. Un enfoque más sostenible funcionaría a temperatura ambiente, se conectaría a electricidad renovable y evitaría por completo el cianuro, sin dejar de producir los mismos productos valiosos.
Convertir la electricidad en una herramienta química
Los autores diseñaron un sistema electroquímico que hace precisamente eso: usa energía eléctrica para impulsar la reacción que transforma un aldehído (aquí, benzaldehído) y amoníaco en el nitrilo benzonitrilo. El núcleo del sistema es un catalizador cuidadosamente estructurado crecido sobre espuma de cobre. Pequeños racimos de óxido de cobalto se sitúan en las puntas de nanobastones de óxido de cobre, creando una superficie grande y activa. Cuando se aplica un voltaje positivo modesto en una mezcla líquida de benzaldehído, amoníaco, agua y acetonitrilo, el electrodo convierte casi cada electrón en el nitrilo deseado, con una eficiencia faradaica cercana al 99% y una selectividad casi perfecta. El catalizador funciona durante al menos 100 horas con poca pérdida de rendimiento, lo que sugiere que podría ser lo bastante robusto para uso industrial.
Siguiendo los átomos durante la reacción
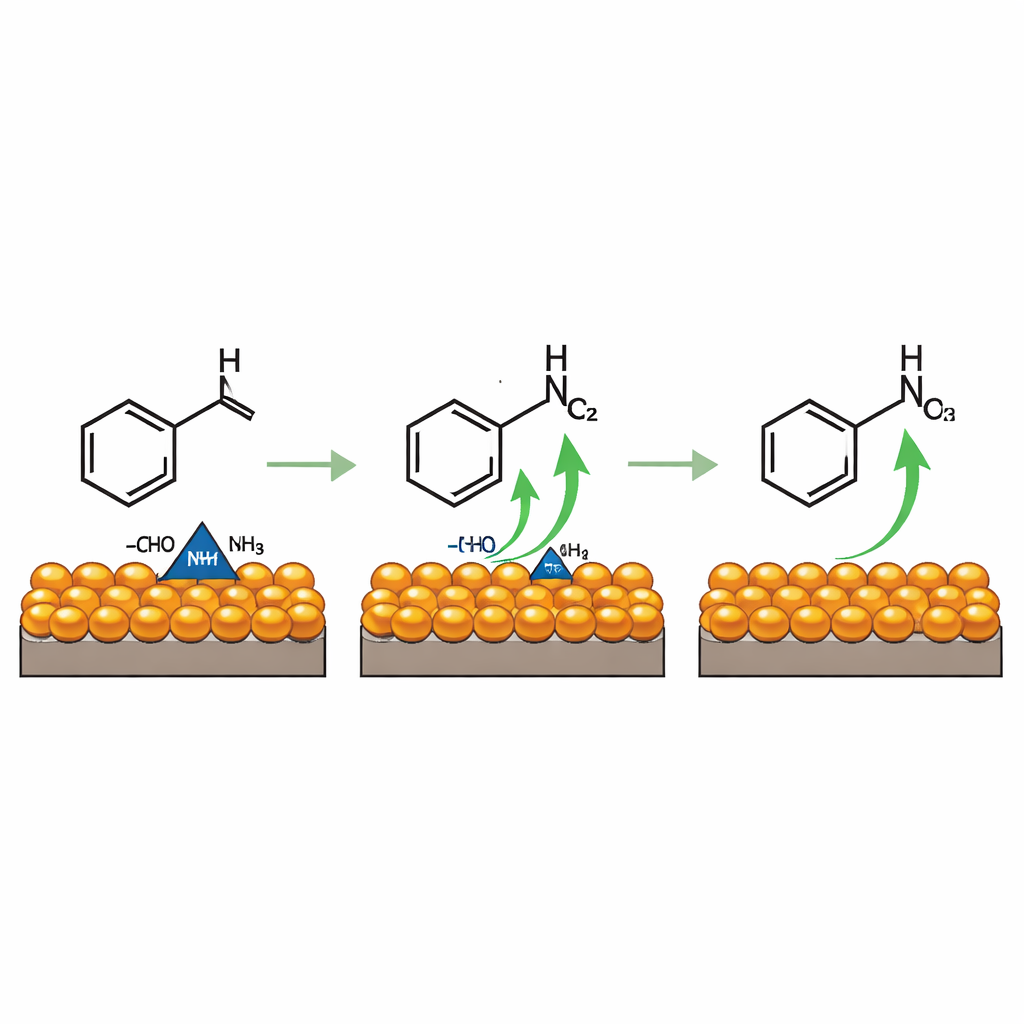
Para entender cómo opera esta conversión limpia, el equipo observó la reacción en tiempo real usando varias técnicas espectroscópicas. Encontraron que el benzaldehído y el amoníaco se combinan primero para formar un intermedio de corta vida que se asemeja a una imina; esencialmente, el doble enlace carbono-oxígeno se reemplaza por un doble enlace carbono-nitrógeno. Esta especie se adsorbe en sitios de cobre en la superficie del catalizador, donde los átomos de hidrógeno se van eliminando gradualmente bajo el voltaje aplicado, dejando el enlace triple carbono–nitrógeno característico de los nitrilos. Simulaciones por ordenador respaldan este esquema, mostrando que el cobre en un estado de oxidación más alto es especialmente eficaz para extraer electrones del intermedio, mientras que los racimos de óxido de cobalto cercanos aumentan el número de sitios activos y afinan sutilmente la naturaleza electrónica del cobre para favorecer este paso de deshidrogenación.
De aromáticos simples a productos del mundo real
Una vez establecido para el benzaldehído, el mismo enfoque demostró ser versátil. Una gama de aldehídos aromáticos y alifáticos, incluidos algunos con grupos cloro, bromo o ciano, se convirtieron sin problemas en sus nitrilos con eficiencias entre aproximadamente el 78% y el 97%. El sistema incluso puede integrarse en rutas multi‑paso que parten de alcoholes o hidrocarburos simples como el tolueno, oxidándolos primero a aldehídos y luego transformándolos en nitrilos. Cabe destacar que algunos de estos materiales de partida pueden obtenerse a partir de dióxido de carbono capturado, lo que insinúa una cadena completamente electrificada desde el gas residual hasta productos químicos de alto valor.
Reciclar aire contaminado en productos útiles
Un giro especialmente atractivo es que el amoníaco necesario para la reacción no tiene por qué provenir del proceso tradicional intensivo en energía Haber–Bosch. Los autores muestran que la producción anódica de nitrilos puede combinarse con un proceso catódico que convierte óxidos de nitrógeno —principales contaminantes atmosféricos— en amoníaco en la misma configuración global. A densidades de corriente de hasta 200 miliamperios por centímetro cuadrado, la cantidad de amoníaco formada en el cátodo coincide estrechamente con la consumida en el ánodo. En principio, esto significa que una planta podría convertir sus propias emisiones de óxidos de nitrógeno en la fuente de nitrógeno para una fabricación de nitrilos más limpia.
Una vía más segura para moléculas de uso cotidiano
En términos sencillos, este trabajo sustituye una química caliente, sucia y a veces venenosa por un método más frío y alimentado eléctricamente que produce los mismos nitrilos útiles con muchos menos subproductos indeseados. Al combinar un catalizador diseñado con precisión con un control cuidadoso de las condiciones de reacción, los autores logran altos rendimientos y largas vidas útiles mientras abren la puerta al uso de gases residuales como ingredientes. Si se escala, tales rutas electroquímicas podrían ayudar a descarbonizar parte de la industria química, reduciendo la huella ambiental de muchos productos cotidianos sin cambiar en qué consisten esos productos.
Cita: Xian, J., Wang, L., Mi, Z. et al. A cyanide-free route towards the electrosynthesis of nitriles. Nat Commun 17, 4095 (2026). https://doi.org/10.1038/s41467-026-70732-5
Palabras clave: electrosíntesis, química verde, nitrilos, amoníaco, utilización de gases residuales