Clear Sky Science · it
Una via senza cianuro verso l’elettrosintesi dei nitrili
Ripulire un angolo nascosto della chimica
I nitrili sono instancabili operai della vita moderna, presenti in farmaci, plastiche, coloranti e prodotti agricoli. Eppure la loro produzione su scala industriale spesso libera anidride carbonica, ossidi di azoto e persino cianuri tossici. Questo studio presenta un modo per produrre nitrili usando elettricità e un catalizzatore moderato invece di calore intenso o reagenti velenosi, indicando la strada verso impianti più puliti che potrebbero persino riutilizzare i propri gas di scarico.

Perché le vie attuali creano problemi
L’industria di solito produce nitrili riscaldando semplici reagenti con ammoniaca e ossigeno a diverse centinaia di gradi Celsius. Quelle condizioni infuocate sono difficili da controllare, quindi parte del materiale di alimentazione si ossida completamente a anidride carbonica e ossidi di azoto. Vie alternative rimpiazzano il calore con chimica che impiega grandi quantità di sali di cianuro, altamente tossici e difficili da maneggiare in sicurezza su larga scala. Con milioni di tonnellate di cianuro utilizzate ogni anno, anche piccole inefficienze lasciano rifiuti pericolosi. Un approccio più sostenibile funzionerebbe a temperatura ambiente, si collegherebbe a elettricità rinnovabile ed eviterebbe del tutto il cianuro pur producendo gli stessi prodotti di valore.
Trasformare l’elettricità in uno strumento chimico
Gli autori hanno progettato un sistema elettrochimico che fa proprio questo: usa energia elettrica per guidare la reazione che trasforma un aldeide (qui, benzaldeide) e ammoniaca nel nitrile benzonitrile. Il cuore del sistema è un catalizzatore attentamente strutturato cresciuto su schiuma di rame. Piccoli aggregati di ossido di cobalto si trovano alle estremità di nanorod di ossido di rame, creando una grande superficie attiva. Quando si applica una modesta tensione positiva in una miscela liquida di benzaldeide, ammoniaca, acqua e acetonitrile, l’elettrodo converte quasi ogni elettrone nel nitrile desiderato, con un’efficienza faradica vicina al 99% e una selettività quasi perfetta. Il catalizzatore continua a funzionare per almeno 100 ore con poca perdita di prestazioni, suggerendo che potrebbe essere sufficientemente robusto per l’uso industriale.
Seguire gli atomi durante la reazione
Per capire come avviene questa conversione pulita, il team ha osservato la reazione in tempo reale usando diverse tecniche spettroscopiche. Hanno scoperto che benzaldeide e ammoniaca si combinano inizialmente formando un intermedio di breve durata che assomiglia a un immina—essenzialmente, il doppio legame carbonio-ossigeno è sostituito da un doppio legame carbonio-azoto. Questa specie si lega a siti di rame sulla superficie del catalizzatore, dove gli atomi di idrogeno vengono progressivamente rimossi sotto la tensione applicata, lasciando il triplo legame carbonio–azoto caratteristico dei nitrili. Simulazioni al computer supportano questo quadro, mostrando che il rame in uno stato di ossidazione più elevato è particolarmente efficace nello strappare elettroni dall’intermedio, mentre gli aggregati di ossido di cobalto nelle vicinanze aumentano il numero di siti attivi e modulano sottilmente il carattere elettronico del rame per favorire questo passo di deidrogenazione.
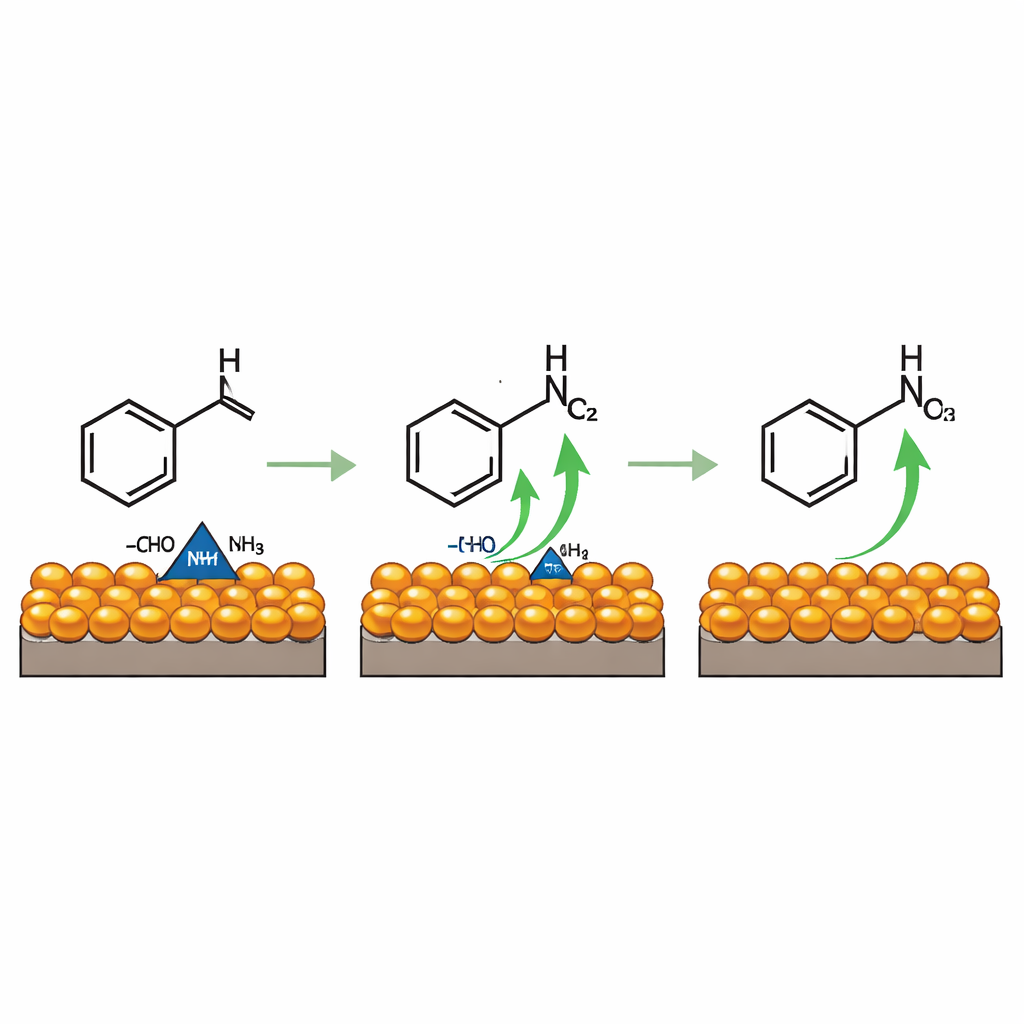
Dagli aromatici semplici ai prodotti reali
Una volta messa a punto per la benzaldeide, la stessa strategia si è dimostrata versatile. Una gamma di aldeidi aromatiche e alifatiche, incluse quelle contenenti gruppi cloro, bromo o ciano, è stata convertita senza problemi nei rispettivi nitrili con efficienze comprese tra circa il 78% e il 97%. Il sistema può persino essere inserito in percorsi a più passaggi che partono da alcoli o idrocarburi semplici come il toluene, ossidandoli prima ad aldeidi e poi proseguendo verso il nitrile. È notevole che alcuni di questi materiali di partenza possano a loro volta essere prodotti da anidride carbonica catturata, suggerendo una filiera completamente elettrificata dal gas di scarico ai prodotti chimici ad alto valore.
Riciclare l’aria inquinata in prodotti utili
Un aspetto particolarmente interessante è che l’ammoniaca necessaria alla reazione non deve provenire dal tradizionale e energivoro processo Haber–Bosch. Gli autori mostrano che la produzione anodica di nitrili può essere accoppiata con un processo catodico che converte gli ossidi di azoto—importanti inquinanti atmosferici—in ammoniaca nello stesso impianto complessivo. A densità di corrente attuali fino a 200 milliampere per centimetro quadrato, la quantità di ammoniaca formata al catodo corrisponde da vicino alla quantità consumata all’anodo. In linea di principio, ciò significa che un impianto potrebbe trasformare le proprie emissioni di ossidi di azoto nella fonte di azoto per una produzione di nitrili più pulita.
Una via più sicura per molecole di uso quotidiano
In termini semplici, questo lavoro sostituisce una chimica calda, sporca e talvolta velenosa con un metodo più freddo e alimentato elettricamente che produce gli stessi nitrili utili con molti meno prodotti di scarto indesiderati. Combinando un catalizzatore progettato con cura e un controllo attento delle condizioni di reazione, gli autori raggiungono rese elevate e lunga durata aprendo la porta all’uso di gas di scarto come ingredienti. Se portate su scala, tali vie elettrochimiche potrebbero contribuire a decarbonizzare una parte dell’industria chimica, riducendo l’impronta ambientale di molti prodotti di uso quotidiano senza cambiarne la natura.
Citazione: Xian, J., Wang, L., Mi, Z. et al. A cyanide-free route towards the electrosynthesis of nitriles. Nat Commun 17, 4095 (2026). https://doi.org/10.1038/s41467-026-70732-5
Parole chiave: elettrosintesi, chimica verde, nitrili, ammoniaca, utilizzo dei gas di scarico