Clear Sky Science · fr
Une voie sans cyanure vers l’électrosynthèse des nitriles
Nettoyer un coin méconnu de la chimie
Les nitriles sont des chevaux de trait discrets de la vie moderne, présents dans les médicaments, les plastiques, les colorants et les produits agricoles. Pourtant, leur production à l’échelle industrielle dégage souvent du dioxyde de carbone, des oxydes d’azote et même du cyanure toxique. Cette étude présente une méthode pour fabriquer des nitriles en utilisant l’électricité et un catalyseur modeste au lieu de températures élevées ou de réactifs nocifs, ouvrant la voie à des usines plus propres qui pourraient même réutiliser leurs propres gaz résiduaires.

Pourquoi les filières actuelles posent problème
L’industrie produit généralement les nitriles en chauffant des précurseurs simples avec de l’ammoniac et de l’oxygène à plusieurs centaines de degrés Celsius. Ces conditions ardentes sont difficiles à contrôler, si bien qu’une partie des intrants brûle complètement en dioxyde de carbone et en oxydes d’azote. D’autres voies remplacent la chaleur par une chimie utilisant de grandes quantités de sels cyanés, fortement toxiques et difficiles à manipuler en sécurité à l’échelle. Avec des millions de tonnes de cyanure utilisées chaque année, même de petites inefficacités laissent des déchets dangereux. Une approche plus durable fonctionnerait à température ambiante, s’alimenterait en électricité renouvelable et éviterait complètement le cyanure tout en produisant les mêmes produits de valeur.
Transformer l’électricité en outil chimique
Les auteurs ont conçu un système électrochimique qui fait exactement cela : il utilise l’énergie électrique pour entraîner la réaction qui convertit un aldéhyde (ici, le benzaldéhyde) et l’ammoniac en le nitrile benzonuitrile. Le cœur du système est un catalyseur finement structuré croissant sur une mousse de cuivre. De petits amas d’oxyde de cobalt reposent sur les extrémités de nanorobes d’oxyde de cuivre, créant une grande surface active. Lorsqu’une tension positive modeste est appliquée dans un mélange liquide de benzaldéhyde, d’ammoniac, d’eau et d’acétonitrile, l’électrode convertit presque chaque électron en nitrile désiré, avec une efficacité faradique proche de 99 % et une sélectivité quasi parfaite. Le catalyseur continue de fonctionner pendant au moins 100 heures avec peu de perte de performance, ce qui suggère qu’il pourrait être suffisamment robuste pour un usage industriel.
Suivre les atomes pendant la réaction
Pour comprendre comment cette conversion propre fonctionne, l’équipe a observé la réaction en temps réel à l’aide de plusieurs techniques spectroscopiques. Ils ont constaté que le benzaldéhyde et l’ammoniac se combinent d’abord pour former un intermédiaire de courte durée ressemblant à une imine — essentiellement, la double liaison carbone–oxygène est remplacée par une double liaison carbone–azote. Cette espèce se fixe sur des sites cuivreux à la surface du catalyseur, où des atomes d’hydrogène sont progressivement retirés sous la tension appliquée, laissant derrière eux la triple liaison carbone–azote caractéristique des nitriles. Des simulations informatiques soutiennent ce tableau, montrant que le cuivre dans un état d’oxydation plus élevé est particulièrement efficace pour arracher des électrons à l’intermédiaire, tandis que les amas d’oxyde de cobalt voisins augmentent le nombre de sites actifs et modulent subtilement le caractère électronique du cuivre pour favoriser cette étape de déshydrogénation.
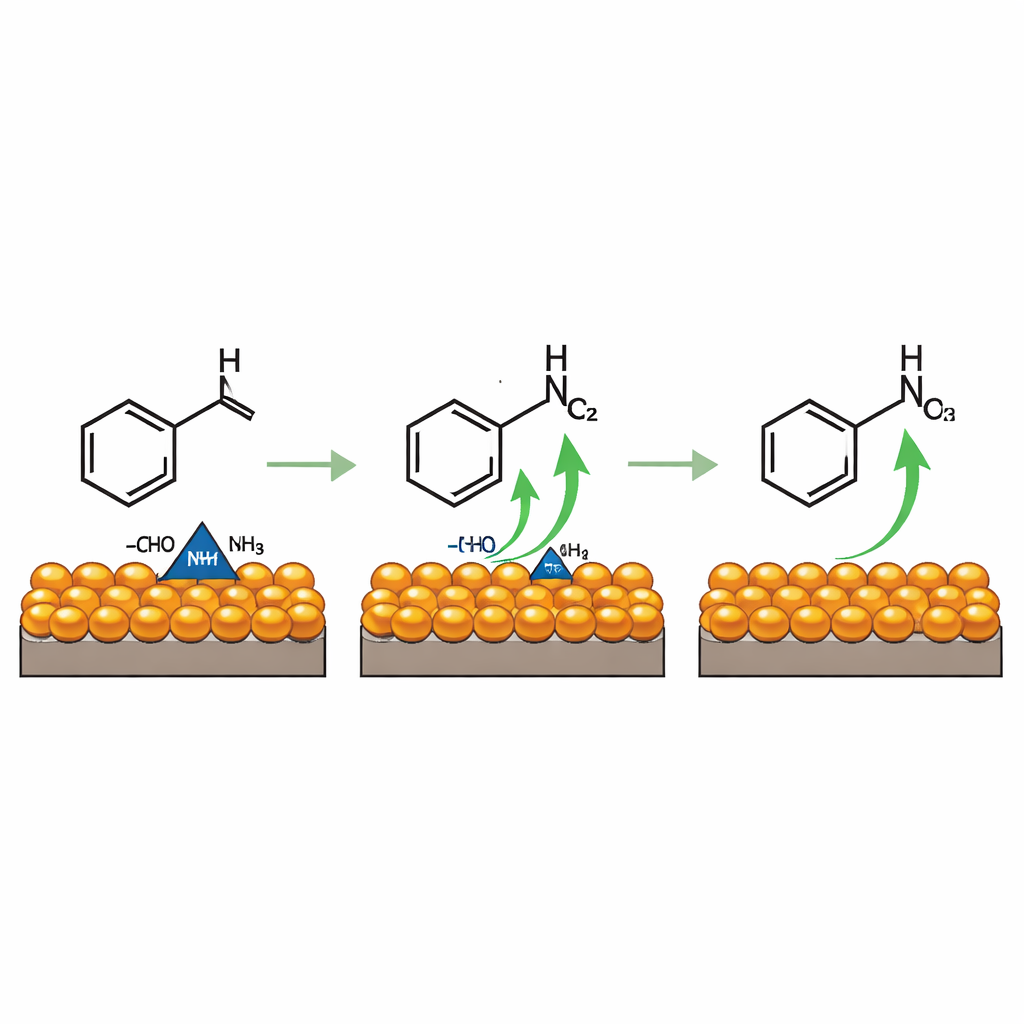
Des aromatiques simples à des produits réels
Une fois la méthode mise au point pour le benzaldéhyde, la même approche s’est révélée polyvalente. Une gamme d’aldéhydes aromatiques et aliphatiques, y compris des composés portant des groupes chlore, brome ou cyano, a été convertie en leurs nitriles avec des efficacités comprises entre environ 78 % et 97 %. Le système peut même s’intégrer à des filières en plusieurs étapes partant d’alcools ou d’hydrocarbures simples comme le toluène, en les oxydant d’abord en aldéhydes puis en poursuivant jusqu’au nitrile. Notamment, certains de ces matériaux de départ peuvent eux-mêmes être obtenus à partir de dioxyde de carbone capturé, suggérant une chaîne entièrement électrifiée allant du gaz résiduaire à des produits chimiques de haute valeur.
Recycler l’air pollué en produits utiles
Un aspect particulièrement séduisant est que l’ammoniac nécessaire à la réaction n’a pas besoin de provenir du procédé traditionnel énergivore Haber–Bosch. Les auteurs montrent que la production anodique de nitriles peut être couplée à un processus cathodique qui convertit les oxydes d’azote — principaux polluants atmosphériques — en ammoniac dans le même dispositif global. À des densités de courant atteignant 200 milliampères par centimètre carré, la quantité d’ammoniac formée au cathode correspond étroitement à celle consommée à l’anode. En principe, cela signifie qu’une usine pourrait transformer ses propres émissions d’oxydes d’azote en source d’azote pour une fabrication de nitriles plus propre.
Une voie plus sûre pour des molécules du quotidien
En termes simples, ce travail remplace une chimie chaude, sale et parfois toxique par une méthode plus froide, alimentée électriquement, qui produit les mêmes nitriles utiles avec beaucoup moins de sous-produits indésirables. En combinant un catalyseur ingénieusement conçu et un contrôle précis des conditions de réaction, les auteurs obtiennent des rendements élevés et une longue durée de vie tout en ouvrant la porte à l’utilisation de gaz résiduaires comme ingrédients. Si elle est montée en échelle, une telle filière électrochimique pourrait aider à décarboner une partie de l’industrie chimique, réduisant l’empreinte environnementale de nombreux produits du quotidien sans en changer la nature.
Citation: Xian, J., Wang, L., Mi, Z. et al. A cyanide-free route towards the electrosynthesis of nitriles. Nat Commun 17, 4095 (2026). https://doi.org/10.1038/s41467-026-70732-5
Mots-clés: électrosynthèse, chimie verte, nitriles, ammoniac, valorisation des gaz résiduaires