Clear Sky Science · nl
BMAL1 reguleert circadiaanse ritmes via door fase-scheiding gemedieerde vorming van transcriptiehubs
Waarom onze interne klokken ertoe doen
Bijna elke cel in ons lichaam houdt de tijd bij en coördineert op de achtergrond slaap, honger, hormoonpieken en zelfs hoe we op medicijnen reageren. In het hart van dit 24-uurs tijdsysteem staat een eiwit genaamd BMAL1, al lang bekend als een cruciaal tandwiel in de biologische klok. Deze studie laat zien dat BMAL1 iets verrassends doet in onze cellen: het verzamelt zich tot kleine, vloeibare druppels die verschijnen en verdwijnen met het tijdstip van de dag, en deze druppels fungeren als controlehubs die helpen onze dagelijkse ritmes stabiel te houden.
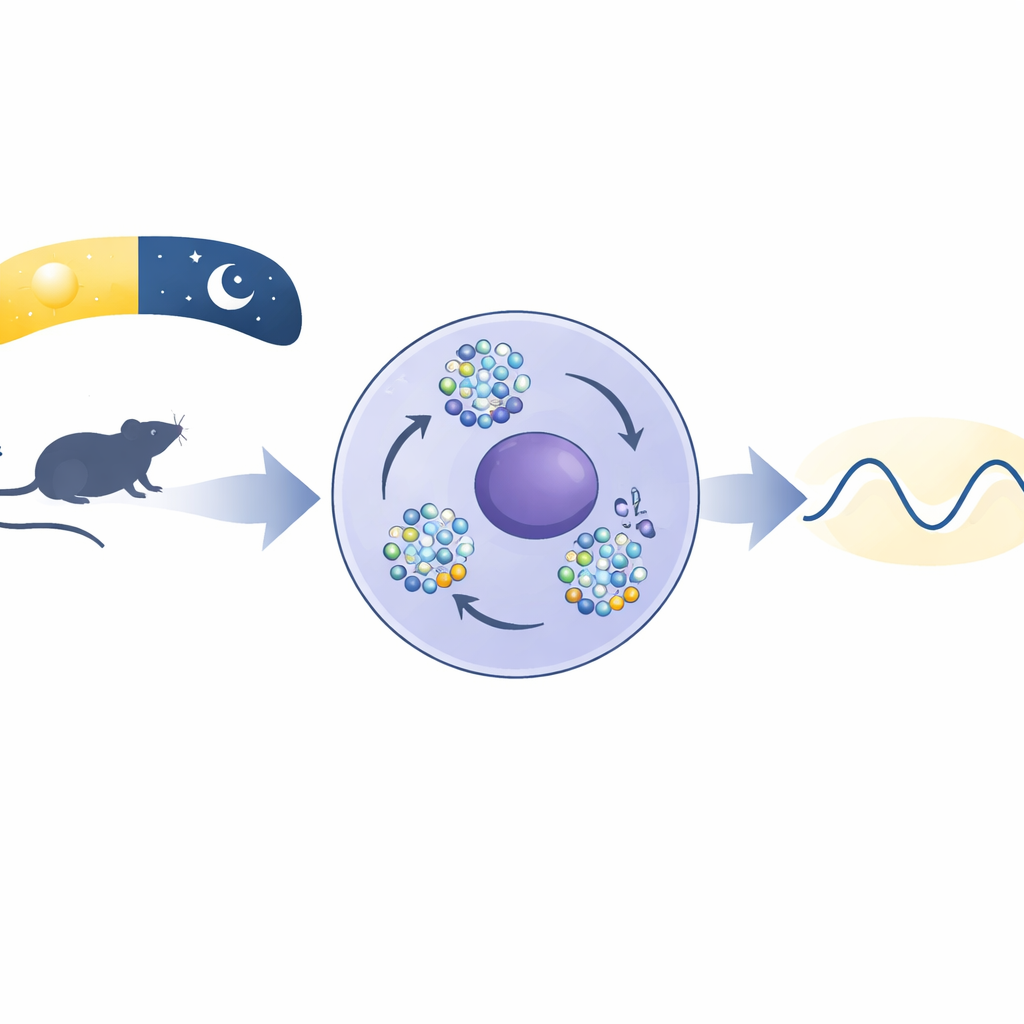
Kleine druppels in de cel
Toen de auteurs keken in muizenhersencellen uit het masterklokgebied en in levercellen, ontdekten ze dat BMAL1 niet gelijkmatig in de kern was verspreid. In plaats daarvan klonterde het samen in felle puncta—kleine vlekjes die gedurende de dag aan en af namen. Deze vlekjes piekten op specifieke tijden die samenvielen met wanneer BMAL1 aan DNA bindt om genen aan te zetten. Met live-celmicrospopie zag het team dat de puncta samensmolten en splitsten als druppels olie in water, hun vorm herstelden nadat ze door een laser waren gebleekt, en oplosten bij blootstelling aan een chemische stof die zwakke moleculaire interacties verstoort. Al dit gedrag zijn kenmerken van “fase-scheiding”, een proces waarbij moleculen zichzelf organiseren in membraanloze compartimenten.
Een flexibele staart die de druppels schakelt
Om te achterhalen wat BMAL1 in staat stelt te condenseren, ontleedden de onderzoekers de structuur ervan. Ze richtten zich op een slappe N-terminaal strook van ongeveer 90 aminozuren die geen vaste vorm heeft. Dergelijke intrinsiek gedesorganiseerde regio’s zijn bekend als drijvende kracht voor druppelvorming in veel eiwitten. Wanneer dit N-terminaal segment werd verwijderd, verloor BMAL1 het vermogen om druppels te vormen en raakte het diffuus verspreid in de kern. In gezuiverde eiwitoplossingen vormde BMAL1 onder specifieke zout- en pH-condities druppels, wat bevestigt dat het zelfstandig kan fase-scheiden. Het team liet ook zien dat chemische wijzigingen—fosforylerings “merken” die aan deze flexibele staart worden toegevoegd—instellen hoe gemakkelijk druppels verschijnen en hoe ze eruitzien, waardoor de condensaten meer of minder stabiel worden zonder de totale hoeveelheid BMAL1 te hoeven veranderen.
Het bouwen van een hub voor gencontrole
Druppels zijn alleen relevant als ze iets doen, en deze BMAL1-condensaten bleken drukke hubs te zijn. Binnen de kern trokken ze selectief CLOCK aan, BMAL1’s belangrijkste partner bij het aandrijven van circadiaanse genen, evenals hulp-eiwitten die DNA openen en transcriptie ondersteunen, zoals het Mediatorcomponent MED1 en de co-activator p300. Korte stukjes DNA met BMAL1’s favoriete bindingssequentie lieten druppels gemakkelijker vormen, wat suggereert dat delen van het genoom zelf helpen bij het nucleëren van deze hubs. Tegelijk bleven andere transcriptiegerelateerde eiwitten buiten of rond de druppels, wat erop wijst dat BMAL1-condensaten gespecialiseerde podia zijn waar de eerste stappen van genactivatie worden georganiseerd voordat volledige transcriptie begint.
Van cellen naar ritmes in het hele lichaam
Het team onderzocht vervolgens wat er gebeurt als BMAL1 deze druppels niet langer kan vormen. In gekweekte humane cellen die BMAL1 misten, herstelde het terugbrengen van het normale eiwit robuuste 24-uurs schommelingen in de activiteit van klokgenen en in nieuw gemaakte RNA. Daarentegen liet een druppel-deficiënt mutant die de N-terminale 90 aminozuren miste deze ritmes vlak, hoewel het eiwit aanwezig was. In deze mutante cellen verloor een belangrijk chromatinemerk geassocieerd met actieve genen (H3K27ac) zijn normale dagelijkse op- en neergang bij circadiaanse genpromoters, en het algemene patroon van ritmische genregulatie verschoof naar meer basale onderhoudsfuncties. Bij muizen leidde het verwijderen van BMAL1 specifiek uit het masterklokgebied van de hersenen tot verlenging van de dagelijkse activiteitscyclus van de dieren, verzwakking van hun ritmes en verandering van hun algemene activiteitsniveau. Het wederinvoeren van normale BMAL1 herstelde deze gedragsritmes, maar de druppel-deficiënte versie deed dat niet, wat benadrukt dat condensaatvorming niet slechts een microscopische curiositeit is maar cruciaal voor het op tijd houden van het interne klokje van het dier.
Wat dit betekent voor dagelijkse gezondheid
Samen vormen deze bevindingen BMAL1 om tot meer dan een simpele aan/uit-schakelaar op DNA. Het functioneert als een organisator die sleutel-moleculen en stukjes DNA verzamelt in tijdsafhankelijke druppels en transcriptie-"hotspots" creëert die genactiviteit op één lijn brengen met de 24-uurs dag. Als dit vermogen tot druppelvorming verstoord raakt, worden cellulaire en gedragsmatige ritmes zwak of ontregeld. Begrijpen hoe dergelijke condensaten het circadiaanse tijdsmechanisme vormgeven, opent de deur naar toekomstige strategieën die onze klokken zouden kunnen bijstellen—bijvoorbeeld door geneesmiddelen te ontwerpen die op specifieke tijden in of uit bepaalde druppels glijden of deze oplossen—om slaap, stofwisseling of behandelreacties te verbeteren.
Bronvermelding: Gao, W., Zhu, L., Wei, Y. et al. BMAL1 regulates circadian rhythms via phase separation–mediated transcriptional hub formation. Sig Transduct Target Ther 11, 160 (2026). https://doi.org/10.1038/s41392-026-02711-7
Trefwoorden: circadiaans ritme, BMAL1, fase-scheiding, biomoleculaire condensaten, genregulatie