Clear Sky Science · ja
上皮細胞と間葉系細胞の時空間的相互作用がヒト象牙質形成を駆動する
なぜ歯にとって重要か
歯の大部分は象牙質で構成されており、エナメル質の下にある硬く生きた組織で、歯に強度と感覚を与えます。深い虫歯、ひび割れ、遺伝性疾患などで象牙質が大きく損なわれると、現行の治療では人工材料で穴をふさぐことしかできず、自然な組織を再構築することはできません。本研究はヒトが発生過程でどのように象牙質を作るかを明らかにし、同じルールを応用して成体の幹細胞に本物の象牙質を再生させる方法を示すことで、歯を内側から修復する将来の治療法の可能性を示しています。
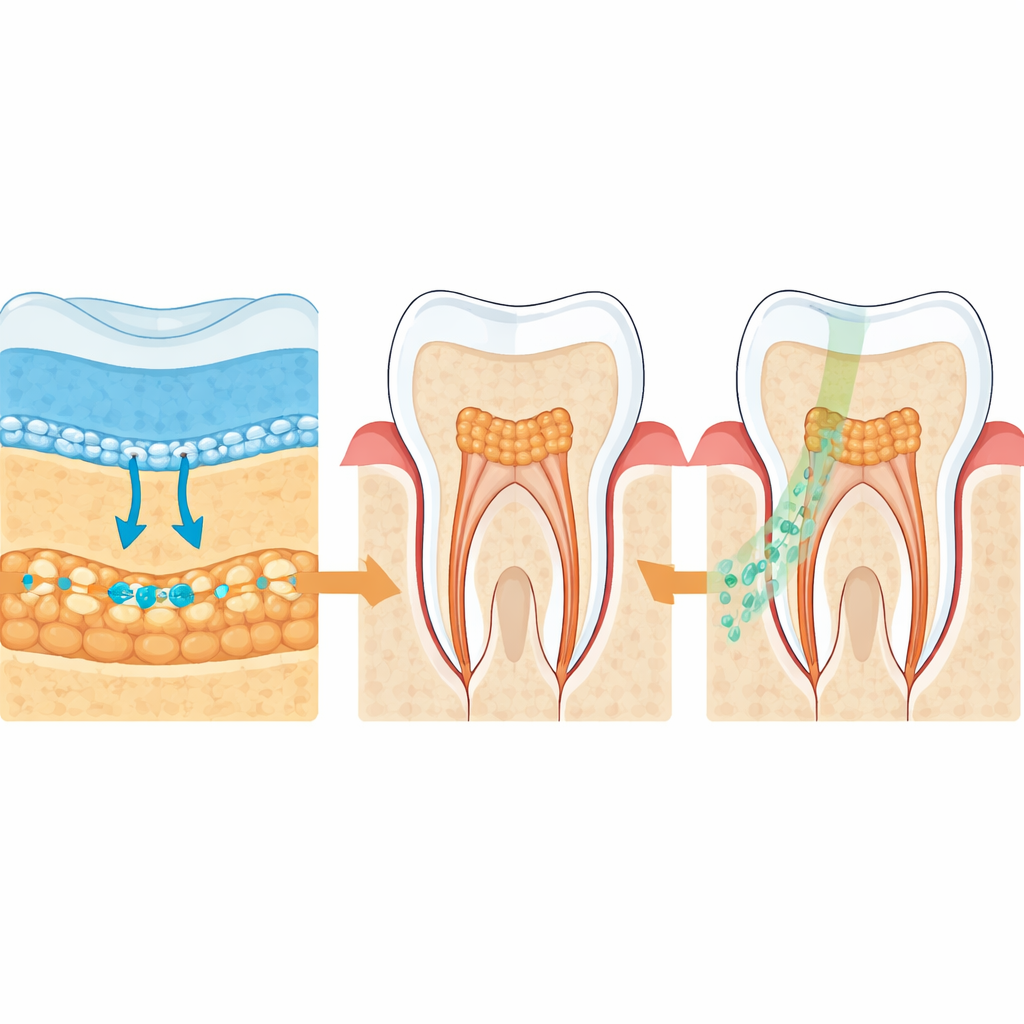
歯はどう形作られるか
ヒトの歯は、外側の上皮細胞シートと内側の間葉系細胞群(後に歯髄や象牙質を形成する)という二つの細胞層の密接な協働から生じます。著者らはシングルセルRNAシーケンシングと空間トランスクリプトミクスを組み合わせることで、胚の初期芽から萌出した歯までのヒト歯発生の詳細な“細胞アトラス”を作成しました。これにより、どの細胞型がいつ出現するか、形成中の歯の中でどのように配置されるか、成熟に伴ってどの化学シグナルを交換しているかを追跡できました。
成長シグナルのリレー
研究チームは二つの主要な細胞間シグナル群に注目しました。一つはWNTで、細胞増殖や初期パターニングを促すことで知られ、もう一つはNOTCHで、細胞が最終的なアイデンティティを決めるのを助けることが多いものです。発生初期には歯の上にある上皮細胞がWNTシグナルを分泌し、隣接する間葉系細胞が対応する受容体を持っていることが見出されました。発生が進むにつれてパターンは変化します:WNTシグナルは減少し、上皮からのNOTCHシグナルが増加し、間葉系細胞はNOTCH受容体と天然のWNT阻害因子を発現し始めます。このWNT優勢の段階からNOTCH優勢の段階への“リレー”は、空間的・時間的に精密に調整されており、どの歯髄細胞が増殖し、どれが象牙質を作るオドントブラストになるかを導いているようです。
信号を受け取る特別な歯髄細胞
間葉系細胞の中で、研究者たちはDLX6-AS1という分子で特徴づけられる、これまであまり注目されてこなかった亜群を同定しました。これらの細胞は上皮の直下に位置し、外来のシグナルを感知するのに最適な場所にあります。遺伝子発現パターンは、これらがWNTとNOTCHの両方に強く応答し、象牙質形成に関与する遺伝子と強く結びついていることを示しています。発生解析は、DLX6-AS1陽性細胞がオドントブラストへ分化するか、象牙質層の直下に留まる予備プールとして保存され、将来の損傷に応答する能力を持つ前駆細胞であることを示唆しています。
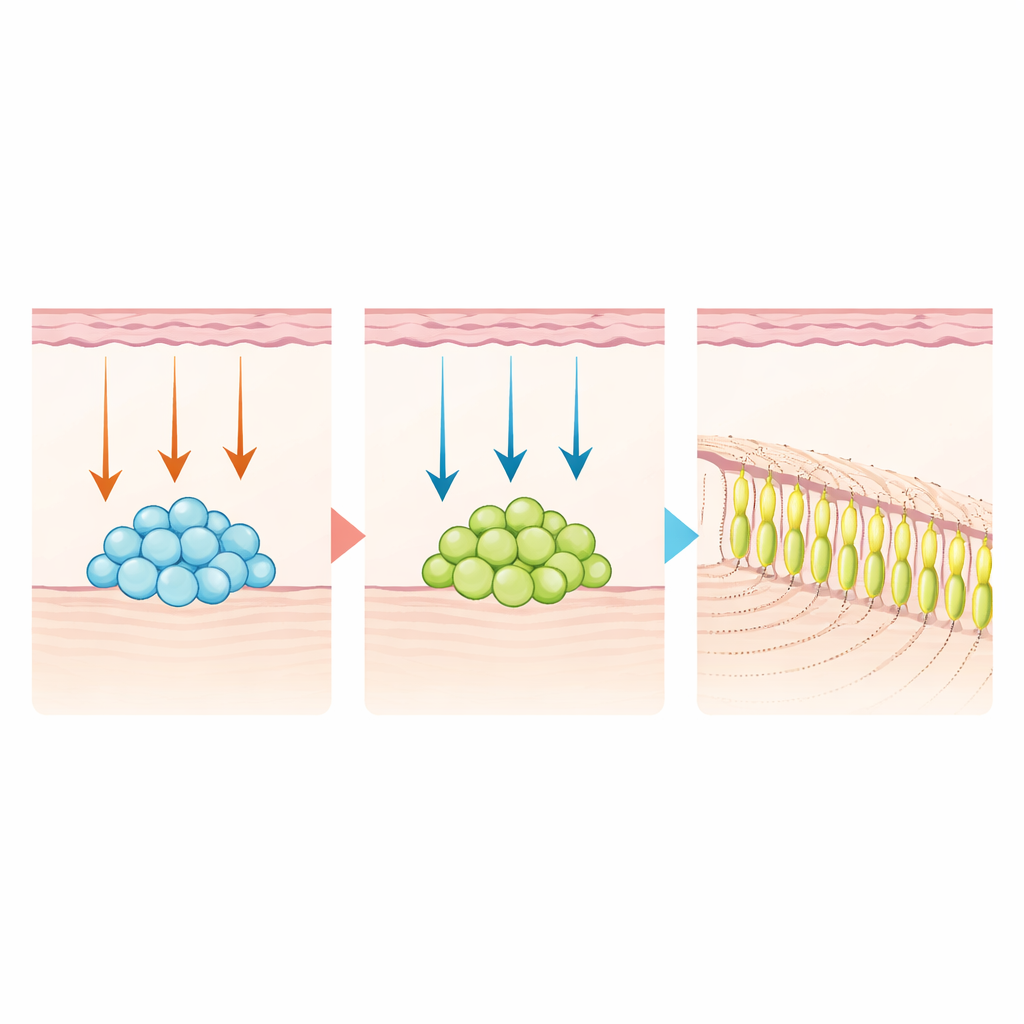
発生過程を再現して新しい象牙質を育てる
これらの知見を治療に応用できるか試すために、チームはヒト歯髄からDLX6-AS1陽性の幹細胞を分離しました。培養皿内で、まずWNTタンパク質のカクテルにさらし、数日後にNOTCH活性化因子のJAG1を与えて発生期のリレーを模倣しました。この二段階処理により、細胞はオドントブラスト様の細胞へと成熟し、標準的なプロトコルに比べて鉱化された象牙質様マトリックスをはるかに効率的に沈着させました。上皮細胞と組み合わせてマウスの腎被膜下に移植したところ、WNT→NOTCH処理を受けた細胞だけが組織化された管状の象牙質構造を生成しました。
動物での損傷歯の修復
次に研究者らは、歯髄に達する深い虫歯に似た損傷をヌードマウスの臼歯に作成しました。彼らはWNTで前処理したヒトDLX6-AS1陽性の歯髄幹細胞と、損傷部位での局所的なNOTCH活性化を導入しました。数週間の追跡観察と顕微解析の結果、これらの細胞は欠損部を横切るよく組織化された象牙質ブリッジを形成し、自然な象牙質に似た細かく平行な管状構造を持つことがわかりました。移植されたヒト細胞は新しい象牙質の縁に整列し、成熟オドントブラストのマーカーを発現しており、実際に歯を再構築していることが確認されました。
将来の歯修復への意義
上皮細胞と間葉系細胞が時間経過の中でどのように相互に情報をやり取りするかを地図化することで、本研究はWNTからNOTCHへの慎重にタイミングされたハンドオフが特定の歯髄幹細胞群を象牙質形成細胞へ導くことを示しました。その配列を成人ヒトの歯髄幹細胞で再現することで、歯損傷の動物モデルで高品質な象牙質を再生させることができました。臨床応用にはより安全な送達法や長期的評価が必要ですが、この研究は合成充填材に代わって生体組織による自己修復を目指す再生歯科治療の概念的かつ実践的な基盤を築くものです。
引用: Wei, W., Wu, C., Sun, J. et al. Spatiotemporal interplay between epithelial and mesenchymal cells drives human dentinogenesis. Nat Commun 17, 2791 (2026). https://doi.org/10.1038/s41467-026-69545-3
キーワード: 歯の再生, 歯髄幹細胞, 象牙質の修復, 細胞シグナル伝達, 再生歯科