Clear Sky Science · es
Interacción espaciotemporal entre células epiteliales y mesenquimales impulsa la dentinogénesis humana
Por qué esto importa para los dientes
La mayor parte de un diente está formada por dentina, el tejido duro y vivo bajo el esmalte que proporciona resistencia y sensibilidad. Cuando las caries profundas, las fisuras o enfermedades genéticas destruyen demasiada dentina, los tratamientos actuales solo pueden parchear el daño con materiales artificiales, no reconstruir tejido natural. Este estudio revela cómo los dientes humanos fabrican dentina durante el desarrollo y muestra cómo esas mismas reglas pueden reutilizarse para inducir a células madre adultas a regenerar dentina real, abriendo la puerta a futuros tratamientos que reparen los dientes desde el interior hacia fuera.
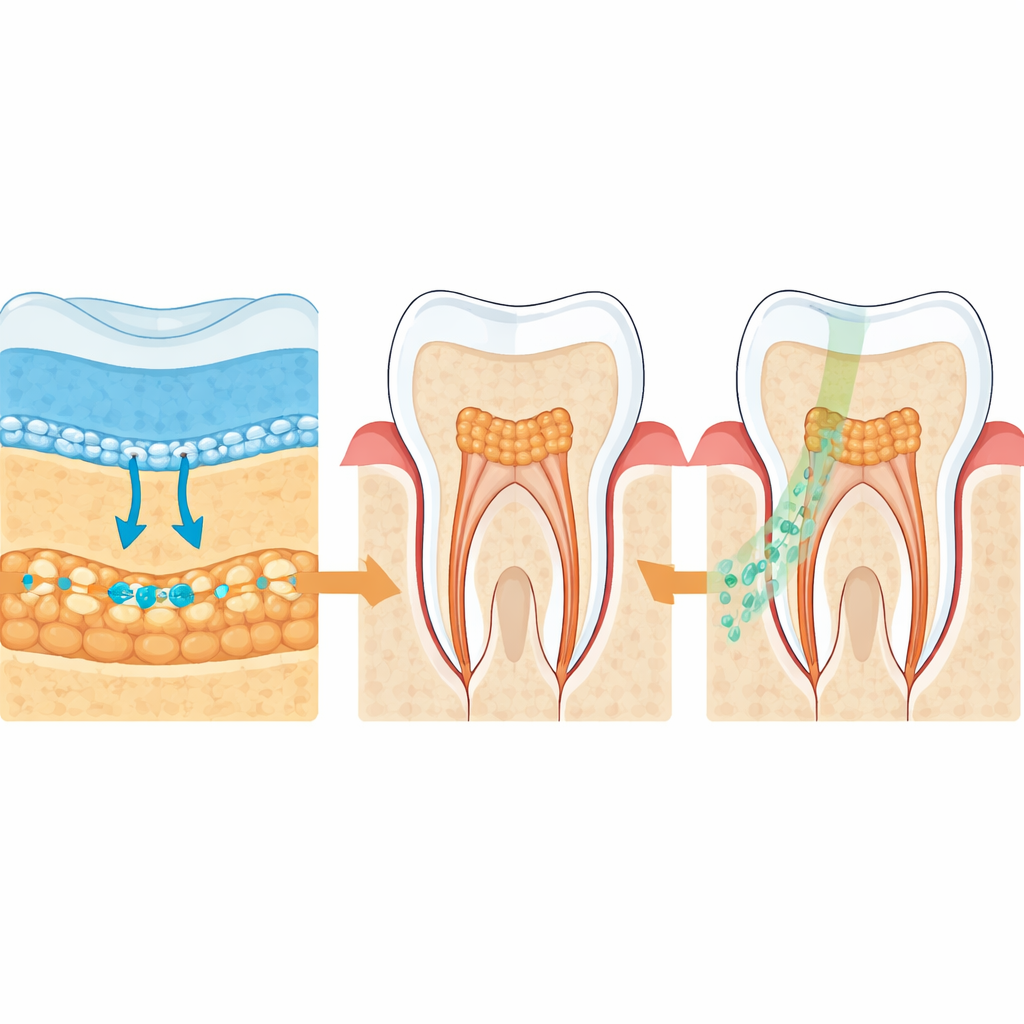
Cómo toma forma un diente
Los dientes humanos surgen de una estrecha colaboración entre dos capas celulares: una lámina externa de células epiteliales y una masa interna de células mesenquimales que más tarde formarán la pulpa dental y la dentina. Los autores crearon un detallado “atlas celular” del desarrollo dental humano, desde brotes embrionarios tempranos hasta dientes erupcionados, combinando secuenciación de ARN unicelular con transcriptómica espacial, que identifica qué genes están activos y dónde. Esto les permitió rastrear qué tipos celulares aparecen cuándo, cómo se organizan en el diente en formación y qué señales químicas intercambian a medida que el diente madura.
El relevo de las señales de crecimiento
El equipo se centró en dos familias principales de señales entre células. Una, llamada WNT, es bien conocida por impulsar el crecimiento celular y el patrónado temprano; la otra, NOTCH, a menudo ayuda a las células a elegir su identidad final. Encontraron que las células epiteliales que recubren el diente en desarrollo secretan señales WNT en fases tempranas, mientras que las células mesenquimales vecinas portan los receptores correspondientes. A medida que avanza el desarrollo, el patrón cambia: las señales WNT disminuyen, las señales NOTCH desde el epitelio aumentan y las células mesenquimales activan receptores NOTCH y bloqueadores naturales de WNT. Este “relevo” de una fase dominada por WNT a otra dominada por NOTCH parece finamente ajustado en espacio y tiempo, orientando qué células de la pulpa proliferan y cuáles se convierten en odontoblastos formadores de dentina.
Las células especiales de la pulpa que reciben la señal
Entre las células mesenquimales, los investigadores identificaron un subgrupo previamente infravalorado marcado por una molécula llamada DLX6-AS1. Estas células se sitúan justo debajo del epitelio, en posición ideal para percibir las señales entrantes. Su actividad génica muestra que responden con fuerza tanto a WNT como a NOTCH y están estrechamente vinculadas a genes implicados en la formación de dentina. Los análisis del desarrollo sugieren que estas células positivas para DLX6-AS1 son progenitores que pueden diferenciarse en odontoblastos o permanecer como una reserva justo bajo la capa de dentina, dispuestas a responder a lesiones más adelante en la vida.
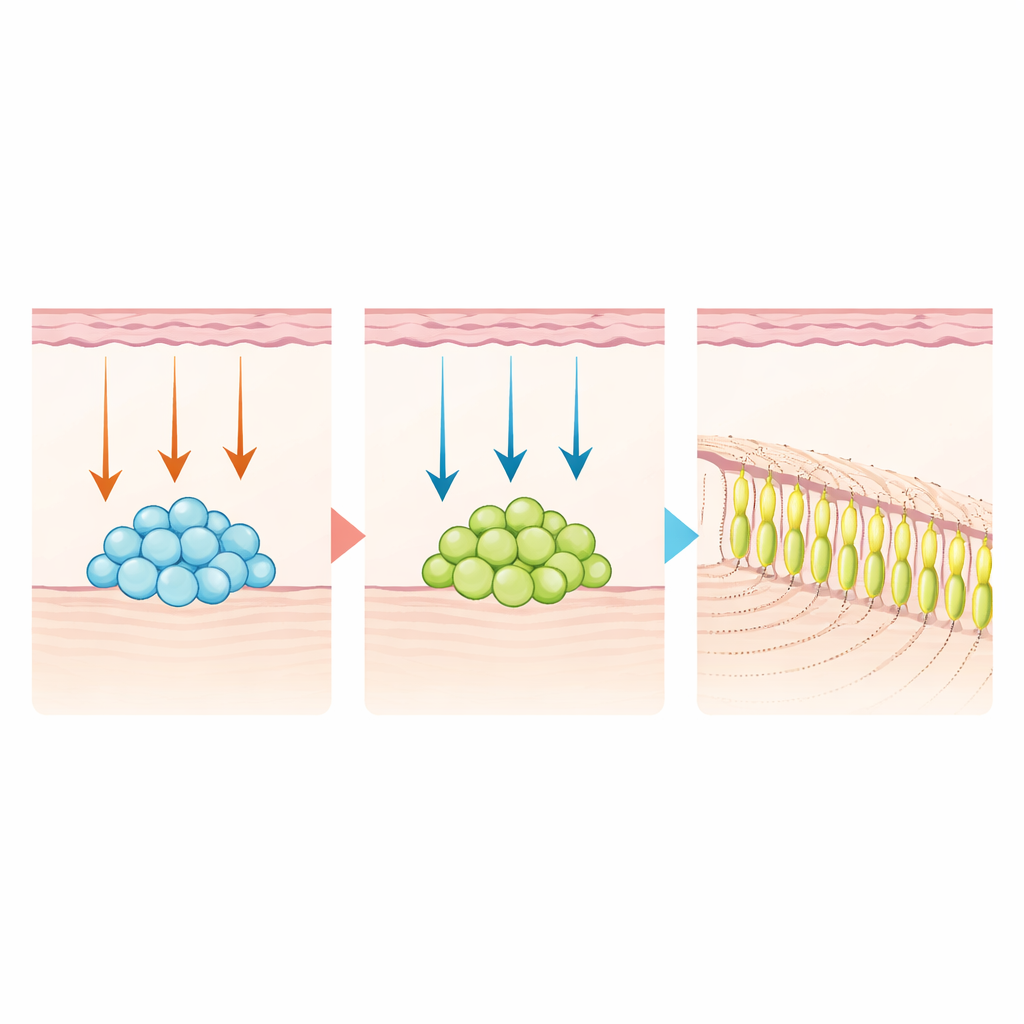
Repetir el desarrollo para generar nueva dentina
Para comprobar si estos hallazgos podían convertirse en terapia, el equipo aisló células madre de la pulpa dental humanas positivas para DLX6-AS1. En placas de laboratorio, expusieron las células primero a un cóctel de proteínas WNT y luego, tras varios días, al activador NOTCH JAG1, imitando el relevo del desarrollo. Este tratamiento en dos pasos impulsó la maduración de las células hacia fenotipos similares a odontoblastos y promovió la deposición de matriz mineralizada, semejante a dentina, con mucha más eficacia que los protocolos estándar. Cuando se combinaron con células epiteliales e implantaron bajo la cápsula renal de ratones, solo las células tratadas con WNT y luego NOTCH generaron estructuras dentinarias organizadas y tubulares.
Reparación de dientes dañados en animales
Los investigadores a continuación provocaron lesiones en los molares de ratones desnudos que imitan caries profundas que alcanzan la pulpa. Introdujeron células madre de la pulpa dental humana positivas para DLX6-AS1 que habían sido preactivadas con señales WNT, junto con activación NOTCH local en el sitio de la lesión. En las semanas siguientes, imágenes y análisis microscópicos revelaron que estas células formaron un puente de dentina bien organizado sobre el defecto, con finos túbulos paralelos que se asemejan a la dentina natural en lugar del tejido “parche” desordenado que suele observarse en la reparación. Las células humanas trasplantadas se alinearon en el borde de la nueva dentina y expresaron marcadores de odontoblastos maduros, confirmando que estaban reconstruyendo activamente el diente.
Qué significa esto para la reparación dental futura
Al cartografiar cómo epitelio y mesénquima se comunican a lo largo del tiempo, este estudio demuestra que una transición cuidadosamente cronometrada de señales WNT a NOTCH guía a una clase especial de células madre de la pulpa para convertirse en formadoras de dentina. Recrear esa secuencia en células madre humanas adultas de la pulpa dental les permitió regenerar dentina de alta calidad en un modelo animal de daño dental. Aunque la aplicación clínica requerirá métodos de entrega más seguros y pruebas a largo plazo, el trabajo establece una base conceptual y práctica para terapias dentales regenerativas que podrían un día sustituir los empastes sintéticos por tejido dental vivo y autorreparable.
Cita: Wei, W., Wu, C., Sun, J. et al. Spatiotemporal interplay between epithelial and mesenchymal cells drives human dentinogenesis. Nat Commun 17, 2791 (2026). https://doi.org/10.1038/s41467-026-69545-3
Palabras clave: regeneración dental, células madre de la pulpa dental, reparación de la dentina, señalización celular, odontología regenerativa