Clear Sky Science · de
Räumlich‑zeitliches Zusammenspiel zwischen epithelialen und mesenchymalen Zellen treibt die menschliche Dentinogenese an
Warum das für Zähne wichtig ist
Der Großteil eines Zahns besteht aus Dentin, dem harten, lebenden Gewebe unter dem Schmelz, das Zähnen Festigkeit und Sensibilität verleiht. Wenn tiefe Karies, Risse oder genetische Erkrankungen zu viel Dentin zerstören, können aktuelle Behandlungen den Schaden nur mit künstlichen Materialien überbrücken, nicht natürliches Gewebe wiederaufbauen. Diese Studie zeigt, wie menschliche Zähne normalerweise Dentin während der Entwicklung bilden, und demonstriert, wie dieselben Prinzipien genutzt werden können, um adulte Stammzellen zur Neubildung echten Dentins zu veranlassen — ein Wegweiser für künftige Therapien, die Zähne von innen heraus reparieren könnten.
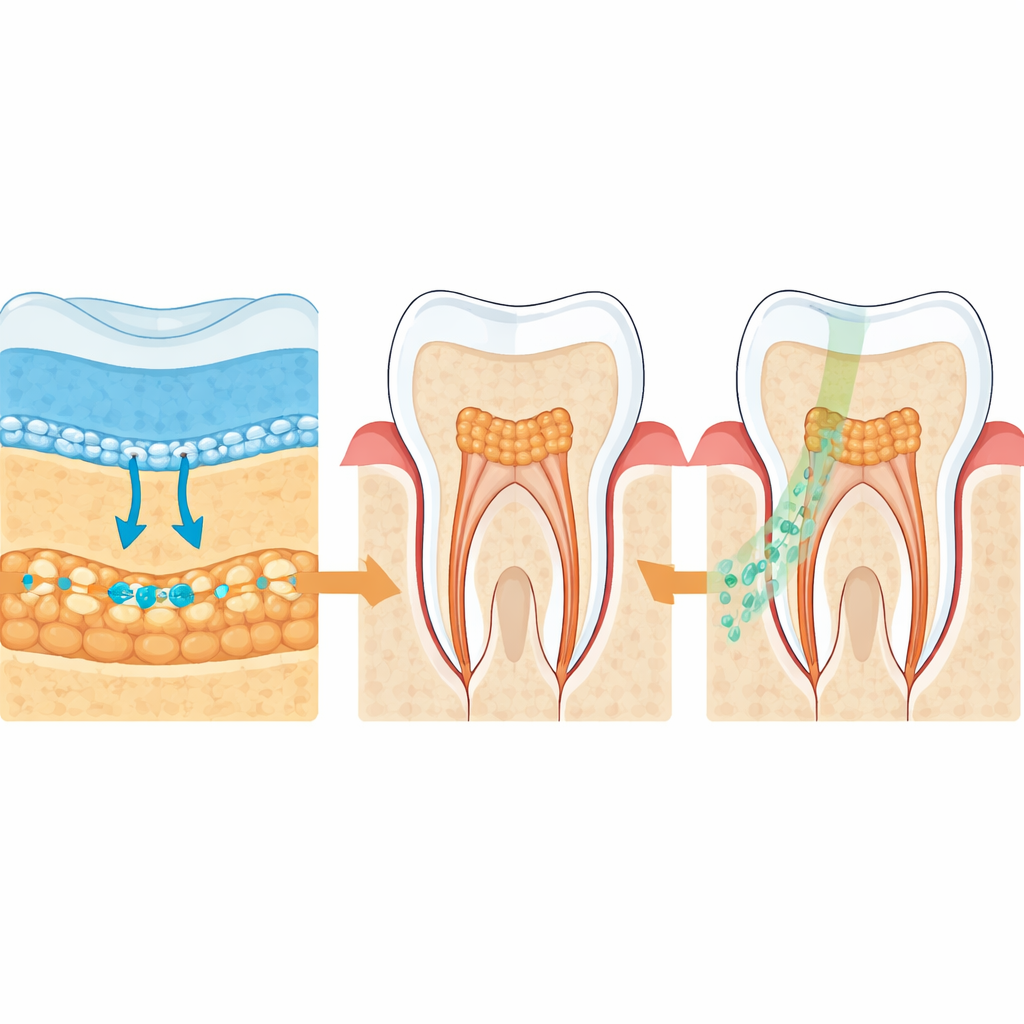
Wie ein Zahn Gestalt annimmt
Beim Menschen entstehen Zähne durch eine enge Zusammenarbeit zweier Zellschichten: ein äußeres Blatt aus epithelialen Zellen und eine innere Masse mesenchymaler Zellen, die später Pulpa und Dentin bilden. Die Autor:innen erstellten einen detaillierten „Zellatlas“ der menschlichen Zahnentwicklung, von frühen embryonalen Knospen bis zu durchgebrochenen Zähnen, indem sie Einzelzell‑RNA‑Sequenzierung mit räumlicher Transkriptomik kombinierten, die zeigt, welche Gene aktiv sind und wo. So konnten sie verfolgen, welche Zelltypen wann auftreten, wie sie im entstehenden Zahn angeordnet sind und welche chemischen Signale sie während der Reifung austauschen.
Die Übergabe von Wachstumssignalen
Das Team konzentrierte sich auf zwei große Familien von Zell‑zu‑Zell‑Signalen. Die eine, WNT genannt, ist bekannt dafür, Zellwachstum und frühe Musterbildung zu steuern; die andere, NOTCH, hilft Zellen häufig bei der Entscheidung ihrer endgültigen Identität. Sie fanden heraus, dass epithelialen Zellen, die den sich entwickelnden Zahn überlagern, früh WNT‑Signale ausschütten, während benachbarte mesenchymale Zellen die passenden Rezeptoren tragen. Mit Fortschreiten der Entwicklung verschiebt sich das Muster: WNT‑Signale nehmen ab, NOTCH‑Signale aus dem Epithel steigen, und die mesenchymalen Zellen schalten NOTCH‑Rezeptoren sowie natürliche WNT‑Blocker ein. Diese „Übergabe“ von einer WNT‑dominierten Phase zu einer NOTCH‑dominierten Phase scheint räumlich und zeitlich fein abgestimmt zu sein und lenkt, welche Pulpa‑Zellen sich teilen und welche zu dentinbildenden Odontoblasten werden.
Die besonderen Pulpa‑Zellen, die den Ruf hören
Unter den mesenchymalen Zellen identifizierten die Forscher:innen eine zuvor wenig beachtete Untergruppe, die durch ein Molekül namens DLX6‑AS1 markiert ist. Diese Zellen liegen direkt unter dem Epithel und sind damit ideal positioniert, um eintreffende Signale zu erfassen. Ihre Genaktivität zeigt, dass sie stark sowohl auf WNT als auch auf NOTCH reagieren und eng mit Genen verbunden sind, die an der Dentinbildung beteiligt sind. Entwicklungsanalysen legen nahe, dass diese DLX6‑AS1‑positiven Zellen Vorläufer sind, die sich entweder zu Odontoblasten differenzieren oder als Reservepool direkt unter der Dentinschicht bleiben können, um später im Leben auf Verletzungen zu reagieren.
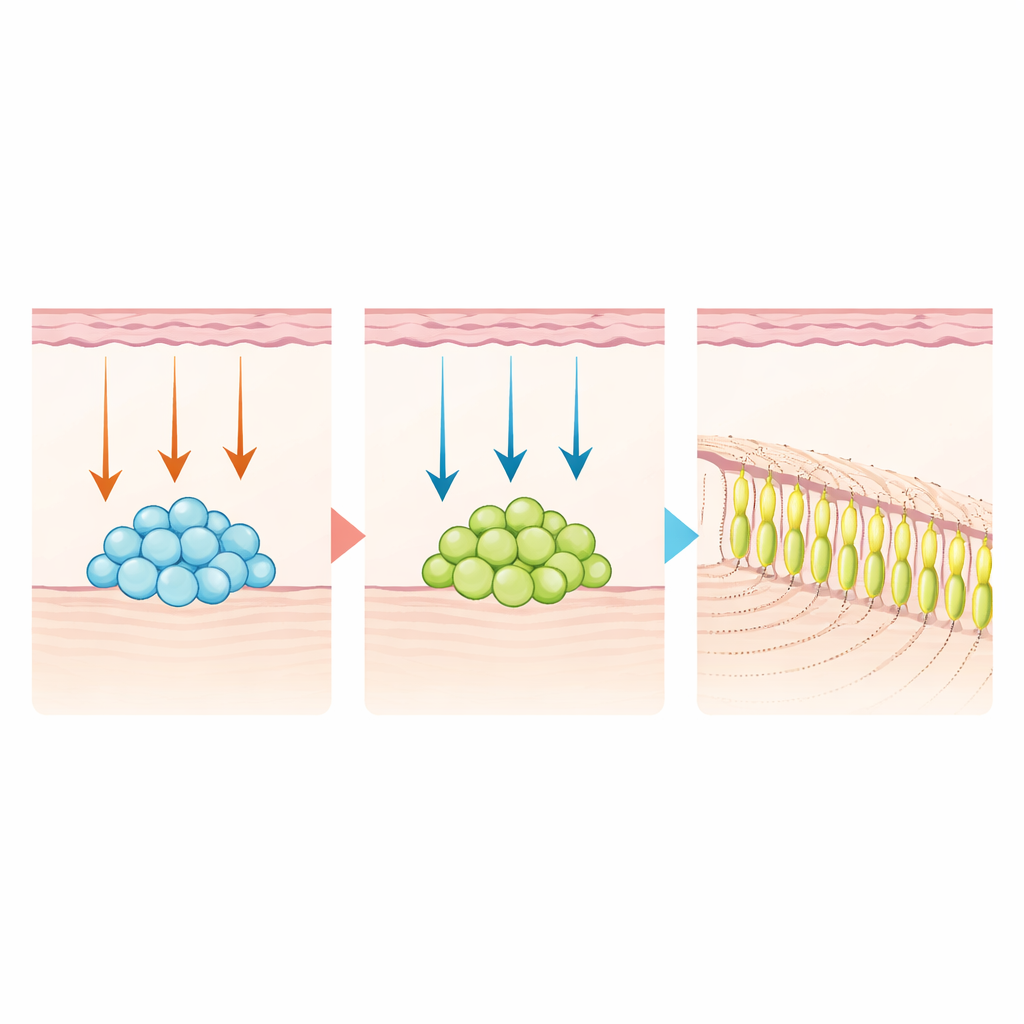
Entwicklungsablauf wiederholen, um neues Dentin zu züchten
Um zu prüfen, ob sich diese Erkenntnisse therapeutisch nutzen lassen, isolierte das Team DLX6‑AS1‑positive Stammzellen aus menschlicher Zahnpulpa. Im Labor be- und setzten sie die Zellen zunächst einem Cocktail aus WNT‑Proteinen aus und danach, nach mehreren Tagen, dem NOTCH‑Aktivator JAG1, um die entwicklungsbedingte Übergabe zu imitieren. Diese zweistufige Behandlung trieb die Zellen dazu, sich zu odontoblastähnlichen Zellen zu reifen und mineralisierten, dentinähnlichen Matrix deutlich effektiver abzusetzen als Standardprotokolle. In Kombination mit epithelialen Zellen und unter die Nierenkapseln von Mäusen implantiert, bildeten nur die WNT‑dann‑NOTCH‑behandelten Zellen organisierte, tubuläre Dentinstrukturen.
Beschädigte Zähne bei Tieren reparieren
Anschließend erzeugten die Forschenden in den Backenzähnen nackter Mäuse Verletzungen, die tiefreichende Karies bis zur Pulpa nachahmen. Sie brachten menschliche DLX6‑AS1‑positive Zahnpulpastammzellen ein, die zuvor mit WNT‑Signalen vorgeprägt worden waren, zusammen mit lokaler NOTCH‑Aktivierung an der Verletzungsstelle. In den folgenden Wochen zeigten bildgebende Verfahren und mikroskopische Analysen, dass diese Zellen eine gut organisierte Dentinbrücke über den Defekt bildeten, mit feinen, parallelen Tubuli, die natürlichem Dentin ähneln, statt dem ungeordneten „Flicken“‑Gewebe, das bei Reparaturen sonst typisch ist. Die transplantierten menschlichen Zellen ordneten sich am Rand des neuen Dentins an und exprimierten Marker reifer Odontoblasten, was bestätigte, dass sie aktiv den Zahn wiederaufbauten.
Was das für künftige Zahnsanierung bedeutet
Indem sie abbilderten, wie Epithel‑ und mesenchymale Zellen über die Zeit miteinander kommunizieren, zeigt diese Studie, dass eine sorgfältig getimte Übergabe von WNT‑ zu NOTCH‑Signalen eine besondere Klasse von Pulpa‑Stammzellen anleitet, zu dentinbildenden Zellen zu werden. Diese Sequenz in adulten menschlichen Zahnpulpastammzellen nachzustellen, ermöglichte es, in einem Tiermodell von Zahnschäden qualitativ hochwertiges Dentin zu regenerieren. Während für eine klinische Anwendung sicherere Abgabemethoden und Langzeitprüfungen nötig sind, legt die Arbeit ein konzeptionelles und praktisches Fundament für regenerative Zahntherapien, die eines Tages synthetische Füllungen durch lebendes, selbstreparierendes Zahngewebe ersetzen könnten.
Zitation: Wei, W., Wu, C., Sun, J. et al. Spatiotemporal interplay between epithelial and mesenchymal cells drives human dentinogenesis. Nat Commun 17, 2791 (2026). https://doi.org/10.1038/s41467-026-69545-3
Schlüsselwörter: Zahnregeneration, Stammzellen des Zahnpulpa, Dentinreparatur, Zell‑Signalgebung, regenerative Zahnmedizin