Clear Sky Science · it
Biomarcatori di imaging multimodale associati alla recidiva dell’edema maculare diabetico durante la terapia treat-and-extend con aflibercept
Perché è importante per le persone con diabete
Molte persone con diabete temono di perdere la vista mentre danni silenziosi si accumulano nella parte posteriore dell’occhio. Questo studio esamina come prevedere meglio quali pazienti con edema maculare diabetico rimarranno asciutti e stabili con meno iniezioni oculari e quali invece sono più a rischio di ricadute. Combinando diversi esami oculari avanzati, i ricercatori mostrano che piccole alterazioni nei vasi retinici danneggiati possono aiutare i medici a personalizzare il trattamento e a ridurre l’onere delle visite frequenti.
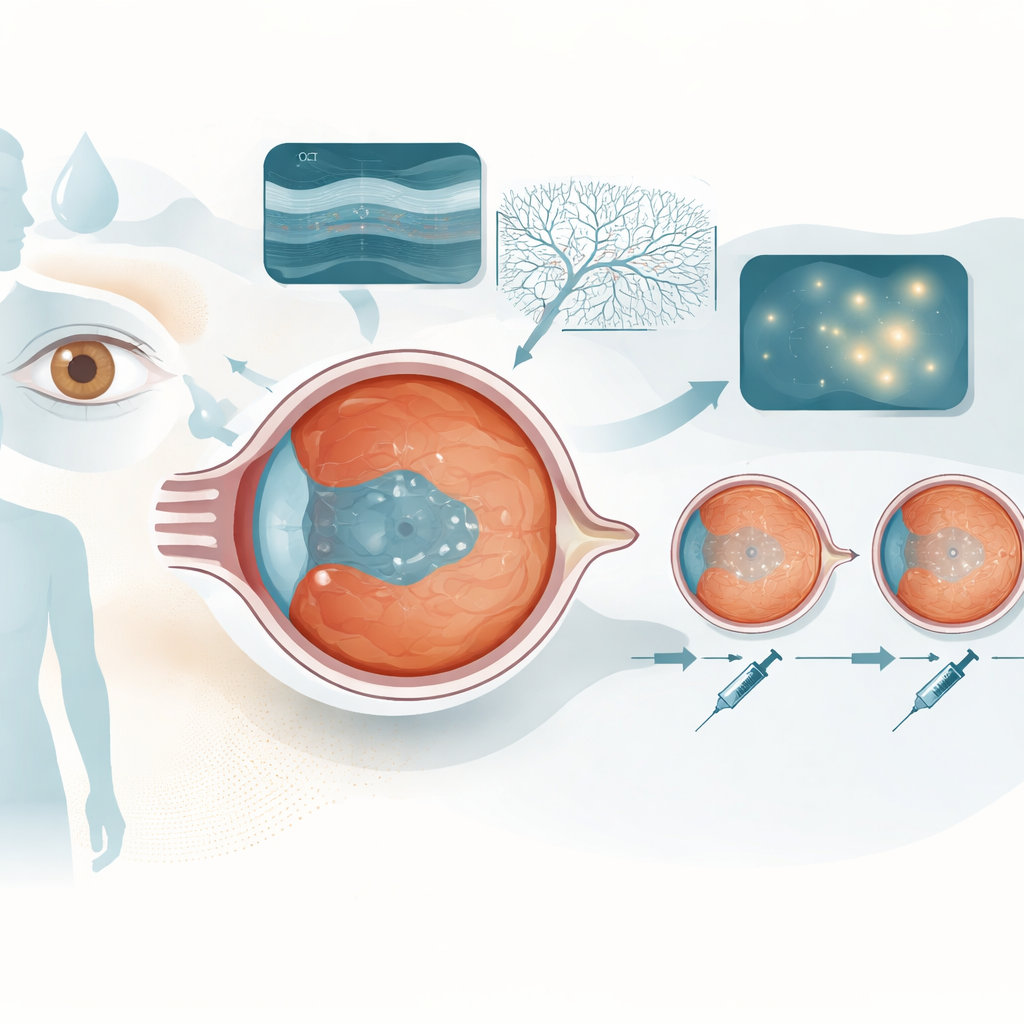
Gonfiore nel centro della vista
L’edema maculare diabetico è un accumulo di liquido nella macula, la parte della retina che ci fornisce la visione centrale nitida. L’iperglicemia e l’infiammazione indeboliscono i piccoli vasi dell’occhio, facendoli perdere. Liquido, piccole dilatazioni dei vasi (microaneurismi) e nuovi canali anomali disturbano gli strati normali della retina e sfumano la vista. I farmaci moderni che bloccano un segnale che promuove la perdita di liquidi, chiamato VEGF, come l’aflibercept, possono asciugare la macula, ma le risposte variano: alcuni restano asciutti per mesi tra un’iniezione e l’altra, mentre altri si riempiono di nuovo in breve tempo.
Un calendario flessibile di iniezioni guidato dagli esami
Il gruppo ha seguito 28 occhi con edema maculare centrale per 18 mesi. Tutti hanno ricevuto inizialmente cinque iniezioni mensili di aflibercept per asciugare la retina in modo aggressivo. Dopo di che, sono entrati in una fase “treat-and-extend”: se la macula rimaneva asciutta e la vista stabile, l’intervallo tra le iniezioni veniva progressivamente allungato fino a 16 settimane; se il gonfiore o la perdita visiva tornavano, l’intervallo veniva accorciato nuovamente a ogni 8 settimane. Durante lo studio i pazienti hanno eseguito diversi tipi di imaging: scansioni tomografiche standard (OCT), angiografia con colorante per i vasi (fluoresceina) e mappe del flusso sanguigno senza colorante (angiografia OCT).
Leggere i segnali di allarme dell’occhio
Dalle scansioni, i ricercatori hanno monitorato diversi potenziali “biomarcatori”. All’OCT hanno contato piccole macchie luminose chiamate formazioni iperreflective, ritenute indice di infiammazione o cellule cariche di lipidi, e misurato l’indice vascolare coroideale, che descrive quanto lo strato vascolare profondo è occupato da sangue rispetto ai tessuti di supporto. Nell’angiografia con fluoresceina hanno valutato l’estensione dell’area maculare che perdeva e il numero di microaneurismi presenti. Nell’angiografia OCT si sono concentrati sulle anomalie microvascolari intraretiniche (IRMA)—vasi tortuosi e dilatati che compaiono quando parti della retina sono in sofferenza per carenza di ossigeno. Hanno quindi confrontato come queste caratteristiche cambiavano in tre gruppi di esito: occhi che necessitavano intervalli più corti, occhi che raggiungevano l’intervallo più lungo e un sottogruppo che rimaneva completamente asciutto.
Quali cambiamenti segnalavano una secchezza duratura?
Nel complesso, la vista è migliorata e lo spessore retinico è diminuito dopo aflibercept, ma i dettagli hanno rivelato chi ha avuto i migliori risultati. Gli occhi che sono rimasti completamente asciutti hanno mostrato riduzioni marcate delle macchie infiammatorie luminose, dell’area di perdita (circa l’84% in meno) e del numero di microaneurismi (quasi il 58% in meno). La maggior parte di questi occhi presentava solo una minima perdita residua alla fine dello studio, mentre la perdita persistente era comune negli occhi che non riuscivano a mantenere intervalli più lunghi. Il risultato più significativo è emerso dall’angiografia OCT: i vasi IRMA anomali sono regrediti nel 75% delle lesioni nel gruppo completamente asciutto, rispetto al solo 10% negli occhi che necessitavano intervalli più corti. La modellizzazione statistica ha mostrato che la regressione delle IRMA era un forte predittore della possibilità di allungare in sicurezza gli intervalli tra le iniezioni.
Mettere tutto insieme per una cura personalizzata
Per un lettore non specialista, il messaggio principale è che un imaging multimodale accurato può rivelare se l’occhio si sta veramente stabilizzando sotto la superficie. Gli occhi in cui i vasi anomali e le perdite si riducono e i modelli di flusso sanguigno si normalizzano dopo il trattamento hanno molte più probabilità di rimanere asciutti con meno iniezioni. Al contrario, gli occhi che conservano molti vasi anomali e perdite, anche se la vista migliora inizialmente, sono più propensi a richiedere terapie frequenti. Prestando attenzione a questi sottili indizi di imaging—in particolare al comportamento delle IRMA nell’angiografia OCT—i medici possono adattare i protocolli treat-and-extend, risparmiando ad alcuni pazienti iniezioni non necessarie e assicurando ad altri cure tempestive per proteggere la vista.
Citazione: Kim, K., Lee, J., Choi, J. et al. Multimodal imaging biomarkers associated with recurrence of diabetic macular edema during aflibercept treat-and-extend therapy. Sci Rep 16, 12639 (2026). https://doi.org/10.1038/s41598-026-42342-0
Parole chiave: edema maculare diabetico, aflibercept, imaging retinico, angiografia OCT, regime treat and extend