Clear Sky Science · de
Multimodale Bildgebungs-Biomarker, die mit dem Rezidiv von diabetischem Makulaödem während einer Aflibercept-Treat‑and‑Extend-Therapie assoziiert sind
Warum das für Menschen mit Diabetes wichtig ist
Viele Menschen mit Diabetes fürchten den schleichenden Verlust des Sehvermögens, während sich im Augenhintergrund Schaden anstaut. Diese Studie untersucht, wie man besser vorhersagen kann, welche Patientinnen und Patienten mit diabetischer Makulaanschwellung mit weniger Augeninjektionen trocken und stabil bleiben und bei welchen die Schwellung zurückkehrt. Durch die Kombination mehrerer fortgeschrittener Augenuntersuchungen zeigen die Forschenden, dass winzige Veränderungen an geschädigten Netzhautgefäßen Ärztinnen und Ärzten helfen können, die Behandlung zu individualisieren und die Belastung durch häufige Termine zu reduzieren.
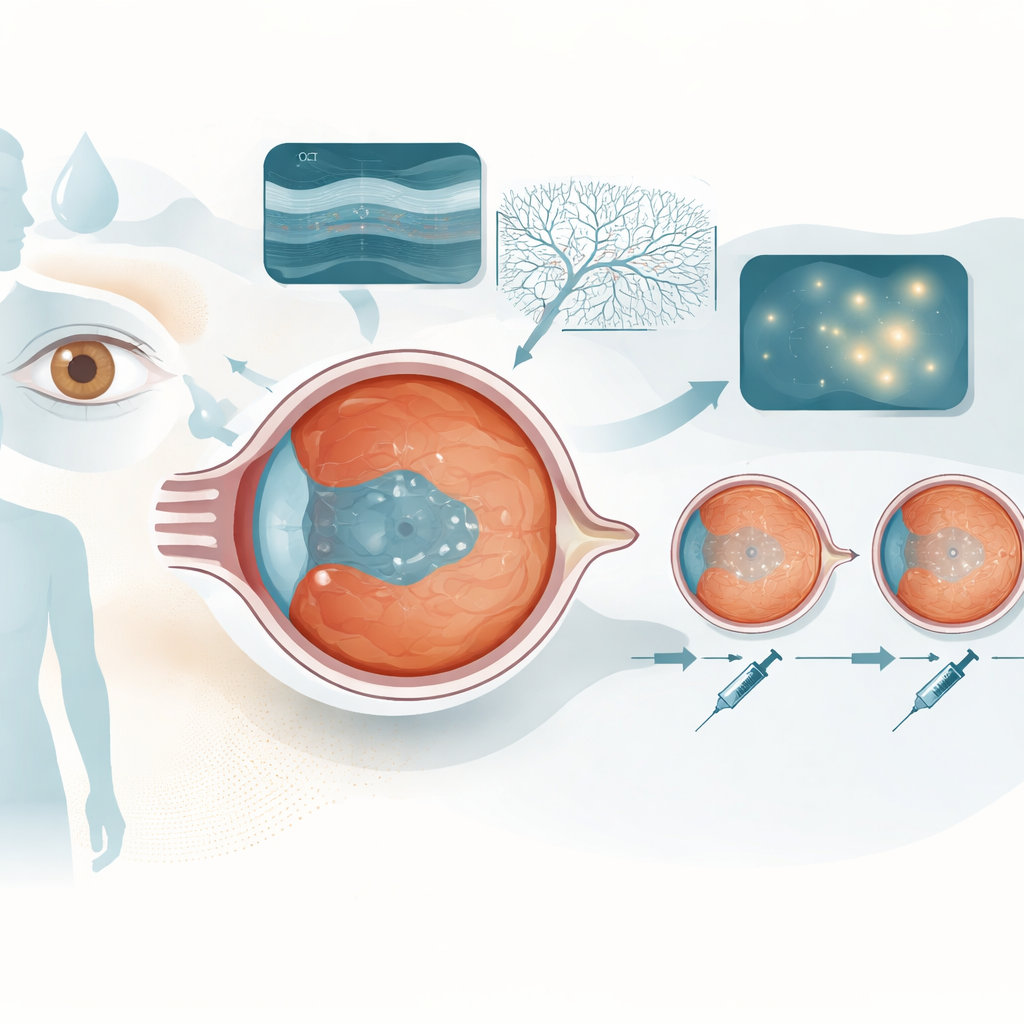
Schwellung im sehaktiven Zentrum des Auges
Das diabetische Makulaödem ist eine Ansammlung von Flüssigkeit in der Makula, dem Teil der Netzhaut, der für scharfes Zentralsehen verantwortlich ist. Hoher Blutzucker und Entzündung schwächen die feinen Blutgefäße im Auge, sodass sie undicht werden. Flüssigkeit, winzige Ausbuchtungen in Gefäßen (Mikroaneurysmen) und abnorme neue Gefäßkanäle stören die normalen Netzhautschichten und verschlechtern das Sehen. Moderne Wirkstoffe, die ein Leck förderndes Signal namens VEGF blockieren, wie Aflibercept, können die Makula austrocknen, doch die Reaktion ist unterschiedlich: Manche bleiben monatelang zwischen den Injektionen trocken, andere schwellen schnell wieder an.
Ein flexibler Injektionsplan, gesteuert durch Bildgebung
Das Team verfolgte 28 Augen mit zentrumsbeteiligtem diabetischem Makulaödem über 18 Monate. Alle erhielten zunächst fünf monatliche Aflibercept‑Injektionen, um die Netzhaut konsequent zu trocknen. Danach begann die „Treat‑and‑Extend“-Phase: Blieb die Makula trocken und das Sehen stabil, wurden die Intervalle zwischen den Injektionen schrittweise bis zu 16 Wochen verlängert; kehrte Schwellung oder Sehverlust zurück, wurde das Intervall wieder auf alle 8 Wochen verkürzt. Während der Studie unterzogen sich die Patientinnen und Patienten mehreren Bildgebungen: standardmäßigen Querschnittsaufnahmen (OCT), gefäßdarstellender Farbstoffangiographie (Fluoreszeinangiographie) und farbstofffreien Durchblutungsdarstellungen (OCT‑Angiographie).
Die Warnsignale des Auges lesen
Aus diesen Aufnahmen verfolgten die Forschenden mehrere potenzielle „Biomarker“. In der OCT zählten sie winzige helle Punkte, sogenannte hyperreflektive Foci, die als Hinweis auf Entzündung oder fettbeladene Zellen gelten, und maßen den choroidalen Gefäßindex, der beschreibt, wie viel der tiefen Gefäßschicht mit Blut im Verhältnis zum Stützgewebe gefüllt ist. In der Fluoreszeinangiographie bestimmten sie, wie groß die undichte Fläche in der Makula war und wie viele Mikroaneurysmen vorhanden waren. In der OCT‑Angiographie konzentrierten sie sich auf intraretinale mikrogefäßmäßige Anomalien (IRMAs) — verdrehte, erweiterte Gefäße, die auftreten, wenn Teile der Netzhaut mangelhaft mit Sauerstoff versorgt werden. Anschließend verglichen sie, wie sich diese Merkmale in drei Ausgangsgruppen veränderten: Augen, die kürzere Intervalle benötigten, Augen, die das längste Intervall erreichten, und eine Untergruppe, die vollständig trocken blieb.
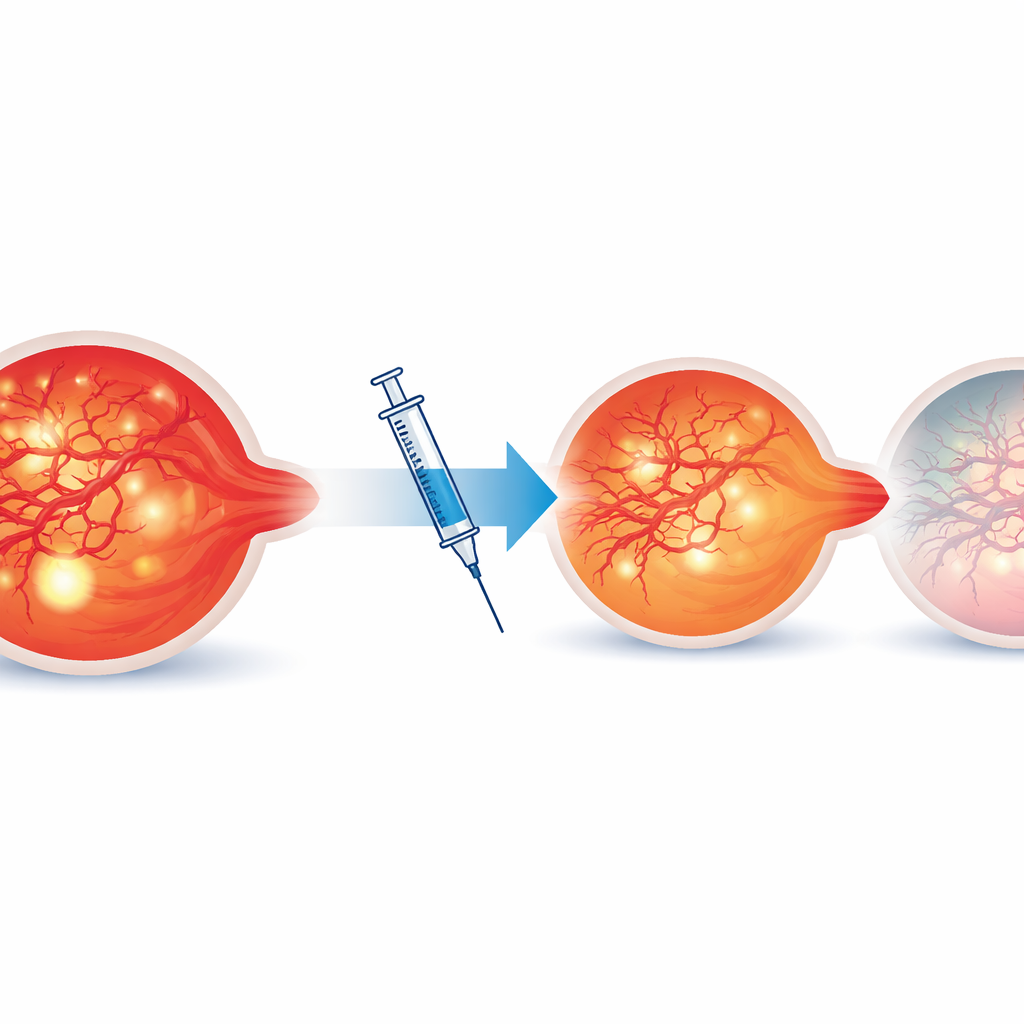
Welche Veränderungen signalisierten anhaltende Trockenheit?
Insgesamt verbesserten sich das Sehvermögen und die Netzhautdicke nach Aflibercept, doch die Details zeigten, wer am besten abschnitt. Augen, die komplett trocken blieben, zeigten deutliche Reduktionen der hellen entzündlichen Punkte, der Leckagefläche (etwa 84 % weniger) und der Anzahl der Mikroaneurysmen (fast 58 % weniger). Die meisten dieser Augen wiesen am Studienende nur noch minimale Restleckage auf, während anhaltende Leckage bei Augen, die längere Intervalle nicht halten konnten, häufig war. Der auffälligste Befund kam aus der OCT‑Angiographie: Abnorme IRMA‑Gefäße gingen in 75 % der Läsionen in der komplett trockenen Gruppe zurück, verglichen mit nur 10 % in den Augen, die kürzere Intervalle benötigten. Statistische Modelle zeigten, dass das Zurückgehen von IRMAs ein starker Prädiktor dafür war, dass ein Auge gefahrlos auf längere Injektionsabstände umgestellt werden kann.
Alles zusammengeführt für personalisierte Versorgung
Für Laien lautet die Hauptbotschaft: Sorgfältige, multimodale Bildgebung kann aufdecken, ob das Auge sich unter der Oberfläche wirklich stabilisiert. Augen, bei denen undichte, abnorme Gefäße zurückgehen und die Durchblutungsmuster nach der Behandlung normalisieren, bleiben wahrscheinlicher mit weniger Injektionen trocken. Im Gegensatz dazu benötigen Augen, die viele abnorme Gefäße und Leckagen behalten, selbst wenn sich das Sehen zunächst verbessert, häufiger Therapie. Wenn Ärztinnen und Ärzte auf diese subtilen Bildgebungszeichen achten — besonders auf das Verhalten der IRMAs in der OCT‑Angiographie —, können sie Treat‑and‑Extend‑Pläne besser anpassen, manchen Patientinnen und Patienten unnötige Injektionen ersparen und gleichzeitig anderen rechtzeitig helfen, ihr Sehvermögen zu schützen.
Zitation: Kim, K., Lee, J., Choi, J. et al. Multimodal imaging biomarkers associated with recurrence of diabetic macular edema during aflibercept treat-and-extend therapy. Sci Rep 16, 12639 (2026). https://doi.org/10.1038/s41598-026-42342-0
Schlüsselwörter: diabetisches Makulaödem, aflibercept, Retina-Bildgebung, optische Kohärenztomographie-Angiographie, Treat‑and‑Extend‑Regime