Clear Sky Science · it
Venti intracellulari compartimentati dirigono le proteine solubili
Come le cellule inviano rifornimenti alla loro linea avanzata
Ogni volta che una cellula striscia su una superficie – per riparare una ferita, connettere il sistema nervoso o inseguire un’infezione – deve recapitare rapidamente le proteine giuste al suo margine anteriore. Questo studio svela un "vento commerciale" nascosto nel citoplasma: un flusso interno dolce ma ordinato che spinge molte proteine solubili verso il fronte della cellula, aiutando la cellula a rimodellarsi e a muoversi con sorprendente rapidità e precisione.
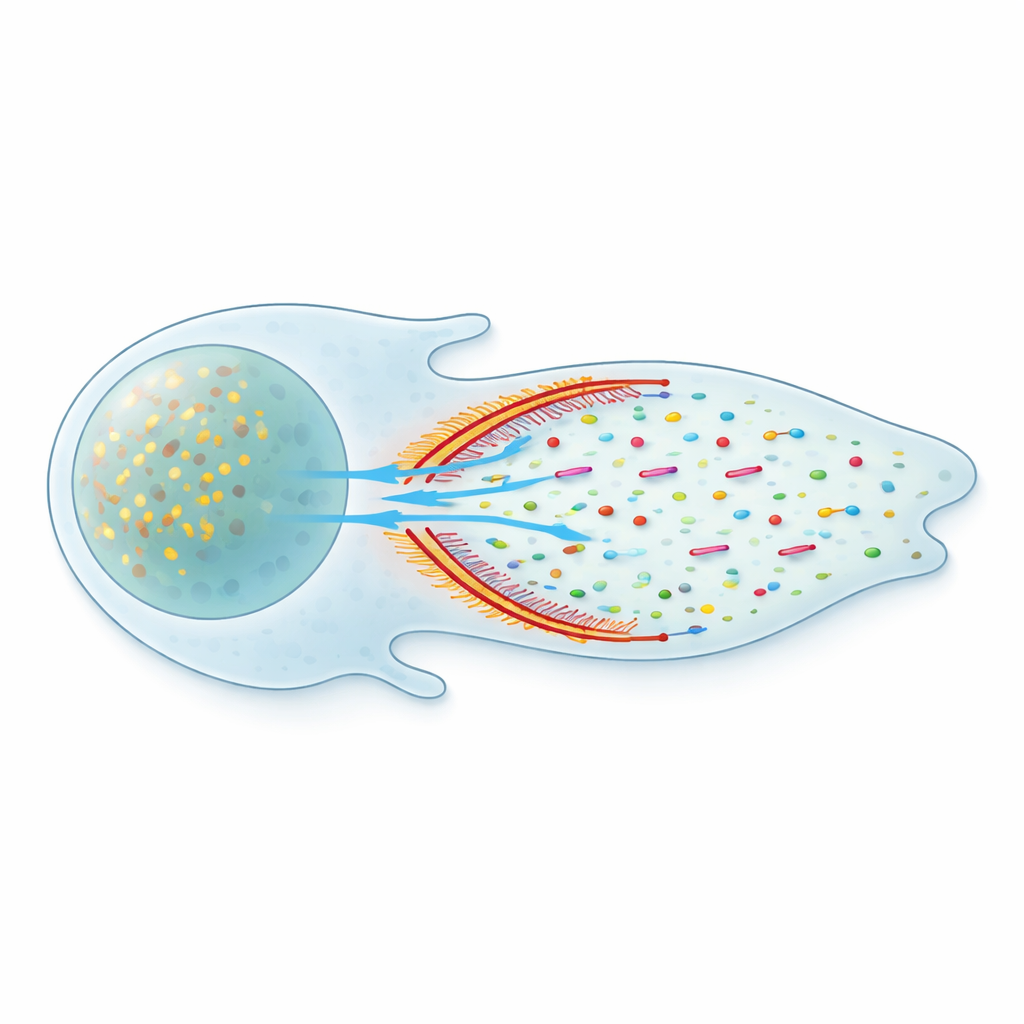
Un problema di spedizione nascosto all’interno delle cellule
All’interno di una cellula, innumerevoli proteine fluttuano attraverso un interno liquido affollato. Alcune viaggiano in vescicole legate a membrane lungo piste molecolari, ma molte proteine importanti galleggiano libere in soluzione. Le classiche immagini dei manuali suggeriscono che queste molecole libere si limitino a diffondere – vagando in modo casuale come un profumo nell’aria. Questa descrizione poneva un enigma: la diffusione è lenta e priva di direzione, eppure le cellule in movimento riescono in qualche modo a mantenere un flusso costante di elementi costitutivi, come i monomeri di actina, pronti al margine avanzato dove continuamente si assemblano nuove strutture.
Trovare un vento d’avanti
Gli autori hanno affrontato questo enigma inventando modi per osservare il movimento di singole proteine solubili all’interno di cellule vive con grande precisione. Hanno usato la luce per oscurare temporaneamente o attivare proteine marcate fluorescentemente, quindi hanno seguito come le molecole appena segnate si diffondevano. In diversi tipi cellulari hanno osservato qualcosa che la sola diffusione non poteva spiegare: dopo aver sbagliato (bleaching) l’actina nella parte posteriore della regione piatta anteriore, in pochi secondi è comparsa una linea scura netta vicino al fronte, mostrando che l’actina non fluorescente era stata trasportata in avanti molto più rapidamente di quanto il moto casuale avrebbe permesso. Quando hanno inibito la miosina II – una proteina motrice capace di generare forze contrattive – questo movimento rapido in avanti si è notevolmente rallentato, indicando che la contrazione attiva contribuisce a guidare un flusso citoplasmatico anteriore che potenzia il trasporto.
Un compartimento frontale separato con una parete soffice
Un’ispezione più accurata ha rivelato che questo flusso non è uniforme in tutta la cellula. La parte anteriore della cellula forma invece un compartimento fluido distinto, separato dal resto del citoplasma da una banda curva di actina e miosina densamente impaccate. Utilizzando microscopia a super-risoluzione, il gruppo ha mostrato che questi "archi" di actina–miosina formano una barriera verticale che attraversa lo spessore della cellula. I traccianti fluorescenti attivati da un lato di questa barriera tendevano a restare in quella regione; attraversare dall’altra parte era ritardato in modo misurabile. Però la barriera non è completamente sigillata – le proteine possono filtrare attraverso – quindi gli autori la descrivono come un condensato permeabile che modella, ma non arresta, il traffico molecolare.
Un flusso non specifico che muove molti carichi
All’interno del compartimento frontale, il citoplasma si comporta come un lento flusso diretto. I ricercatori hanno osservato che non solo i monomeri di actina ma anche proteine leganti l’actina e componenti delle adesioni – tra cui Arp3, vinculina e paxillina – migravano preferenzialmente verso il margine. Anche sonde fluorescenti inerti senza partner di legame specifici venivano trasportate in avanti nello stesso modo. Le misurazioni del moto molecolare hanno mostrato che la semplice diffusione era simile nella parte anteriore e nel corpo della cellula, ma un componente addizionale advettivo – il flusso del fluido – era molto più forte al fronte. Ciò significa che il flusso è in gran parte non specifico: facilita la consegna di qualsiasi proteina solubile sufficientemente piccola da muoversi attraverso la maglia di actina, assicurando che un ampio arsenale di molecole raggiunga il margine più rapidamente di quanto la sola diffusione potrebbe fare.
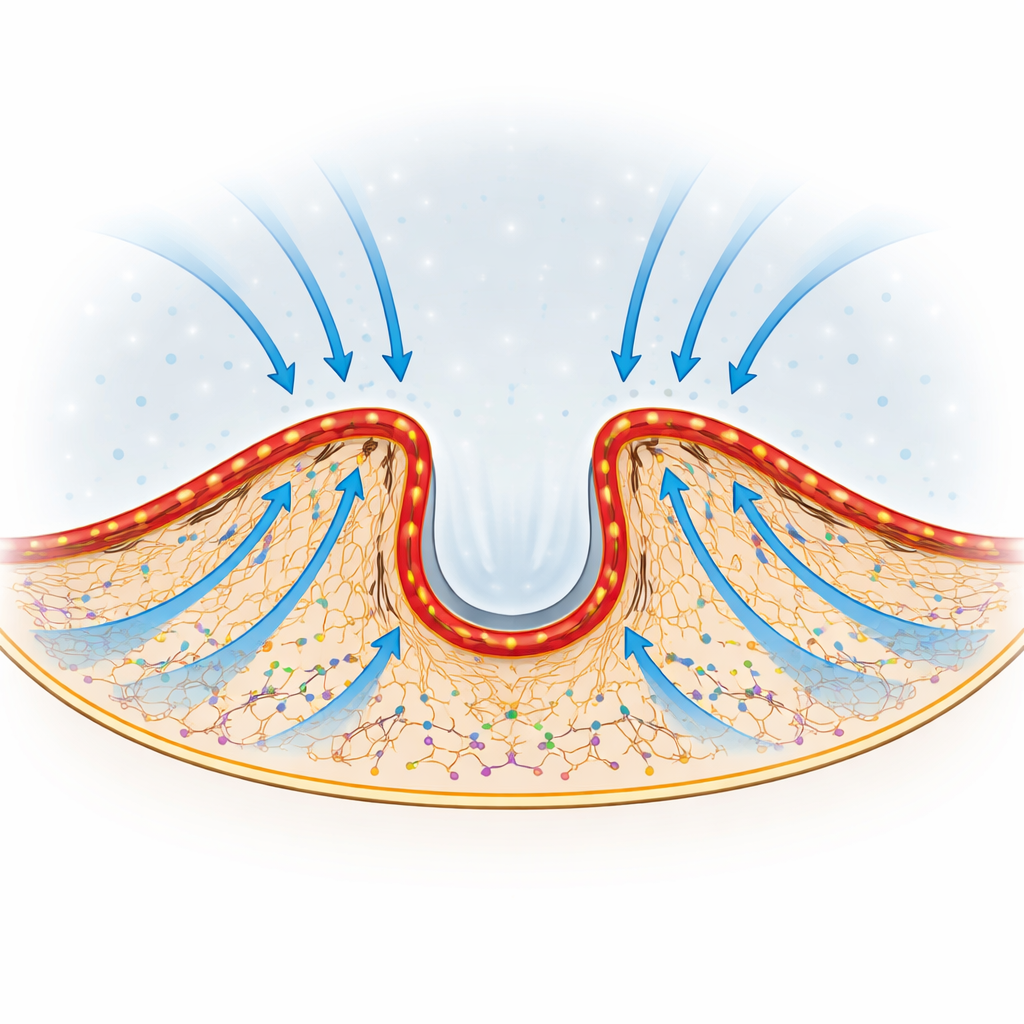
Instradare il flusso verso dove il margine avanza
Forse ciò che colpisce di più è che la direzione di questo "vento commerciale" interno può essere modulata. Man mano che le cellule estendono o ritraggono diverse porzioni del loro margine, la curvatura e la posizione degli archi actina–miosina si spostano. Gli autori hanno osservato che l’actina appena attivata tende a fluire preferenzialmente verso le regioni del margine che stanno effettivamente protrudendo. Quando hanno alterato o appiattito gli archi inibendo la miosina o tagliando un arco isolato con un laser focalizzato, l’avanzamento locale del margine ha rallentato solo nell’area davanti alla struttura danneggiata. Questo suggerisce che la forma della barriera funziona come una serie di deflettori regolabili, reindirizzando il flusso e la fornitura di proteine verso la regione del margine che deve spingere in avanti.
Perché questo conta per la forma e il movimento cellulare
Svelando un compartimento frontale specializzato e un "vento" interno guidato dalla miosina, questo lavoro cambia il modo in cui pensiamo alla cellula in movimento. Piuttosto che fare affidamento esclusivamente sulla lenta e casuale diffusione, le cellule creano un pseudo-organelle al loro margine avanzato: una zona flessibile delimitata da un condensato proteico che sia concentra molecole chiave sia incanala il flusso del fluido. Questa disposizione consente alle cellule di ridistribuire rapidamente proteine solubili dove servono di più, collegando strettamente la fornitura locale di proteine ai cambiamenti di forma, adesione e migrazione cellulare. In sostanza, il fronte della cellula è rifornito da una corrente interna costantemente regolata, permettendo risposte rapide ed energeticamente efficienti all’ambiente esterno.
Citazione: Galbraith, C.G., English, B.P., Boehm, U. et al. Compartmentalized cytoplasmic tradewinds direct soluble proteins. Nat Commun 17, 2589 (2026). https://doi.org/10.1038/s41467-026-70688-6
Parole chiave: migrazione cellulare, cit scheletro di actina, trasporto intracellulare, localizzazione proteica, flusso citoplasmatico