Clear Sky Science · es
Brisas internas citoplasmáticas compartimentadas dirigen proteínas solubles
Cómo las células envían suministros a su frente
Siempre que una célula se desplaza sobre una superficie —para cerrar una herida, conectar el sistema nervioso o perseguir una infección— debe entregar rápidamente las proteínas adecuadas a su borde delantero. Este artículo descubre una "brisa comercial" oculta dentro del citoplasma: un flujo interno suave pero organizado que arrastra muchas proteínas solubles hacia el borde líder de la célula, ayudando a que ésta se reconfigure y se mueva con sorprendente rapidez y precisión.
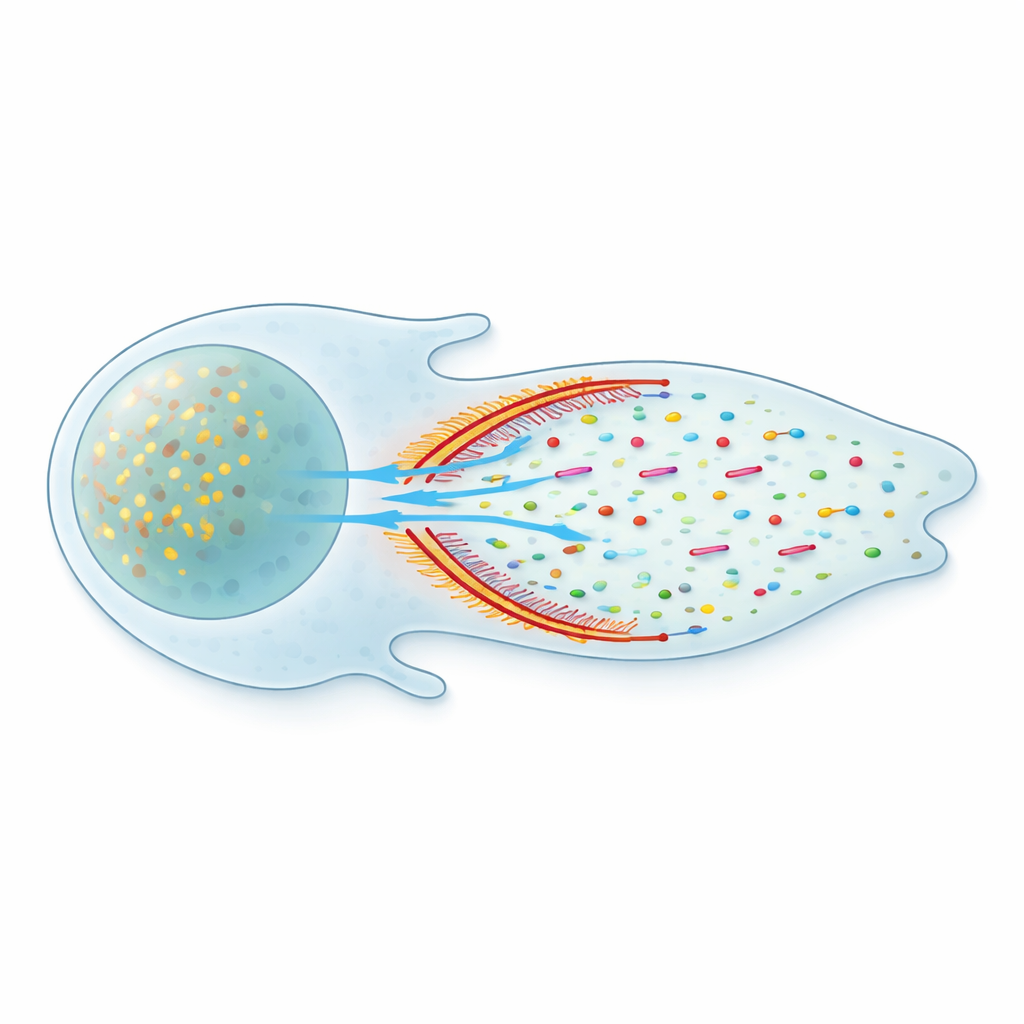
Un problema de envío oculto dentro de las células
En el interior de una célula, innumerables proteínas derivan a través de un interior líquido muy poblado. Algunas viajan en paquetes unidos a membrana por pistas moleculares, pero muchas proteínas importantes flotan libremente en solución. Las imágenes clásicas de los libros de texto sugieren que estas moléculas libres simplemente difunden, vagando al azar como el perfume en el aire. Esa imagen plantea un enigma: la difusión es lenta y sin dirección, y, sin embargo, las células en movimiento mantienen de algún modo un flujo constante de bloques de construcción, como los monómeros de actina, listos en su frente donde se ensamblan constantemente nuevas estructuras.
Encontrando una brisa que empuja hacia adelante
Los autores abordaron este rompecabezas inventando formas de observar proteínas solubles individuales dentro de células vivas con alta precisión. Usaron luz para oscurecer o activar temporalmente proteínas etiquetadas con fluorescencia y luego siguieron cómo se dispersaban las moléculas recién marcadas. En varios tipos celulares observaron algo que la difusión por sí sola no podía explicar: tras blanquear la actina en la parte posterior de la región plana del frente, apareció en segundos una línea oscura marcada cerca del borde anterior, lo que mostró que la actina no fluorescente había sido llevada hacia adelante mucho más rápido de lo que permitiría el movimiento aleatorio. Cuando inhibieron la miosina II —una proteína motora capaz de generar fuerzas contractiles— este movimiento rápido hacia adelante se ralentizó de forma notable, lo que indica que la contracción activa contribuye a impulsar un flujo citoplasmático frontal que potencia el transporte.
Un compartimento frontal separado con una pared blanda
Una inspección más detallada reveló que este flujo no es uniforme en toda la célula. En lugar de eso, el frente de la célula forma un compartimento fluido distinto, separado del resto del citoplasma por una banda curva de actina y miosina densamente empaquetadas. Utilizando microscopía de superresolución, el equipo mostró que estos "arcos" de actina–miosina forman una barrera vertical que atraviesa el espesor de la célula. Los trazadores fluorescentes activados a un lado de esta barrera tendían a permanecer en esa región; cruzar al otro lado se retrasaba de forma medible. Sin embargo, la barrera no está completamente sellada: las proteínas pueden filtrarse a través de ella, por lo que los autores la describen como un condensado con fugas que moldea, pero no detiene, el tráfico molecular.
Un flujo no específico que mueve muchas cargas
Dentro del compartimento frontal, el citoplasma se comporta como un río lento y dirigido. Los investigadores observaron que no solo los monómeros de actina, sino también proteínas que se unen a la actina y componentes de adhesión —incluyendo Arp3, vinculina y paxilina— derivaban preferentemente hacia el borde. Incluso sondas fluorescentes inertes sin socios de unión específicos eran arrastradas hacia adelante de la misma manera. Las mediciones del movimiento molecular mostraron que la difusión simple era similar en el frente y en el cuerpo de la célula, pero un componente advectivo añadido —flujo de fluido— era mucho más fuerte en el frente. Esto significa que el flujo es en gran parte no específico: potencia la entrega de cualquier proteína soluble lo bastante pequeña para moverse a través de la malla de actina, asegurando que un amplio conjunto de moléculas llegue al borde más rápido de lo que la difusión por sí sola podría lograr.
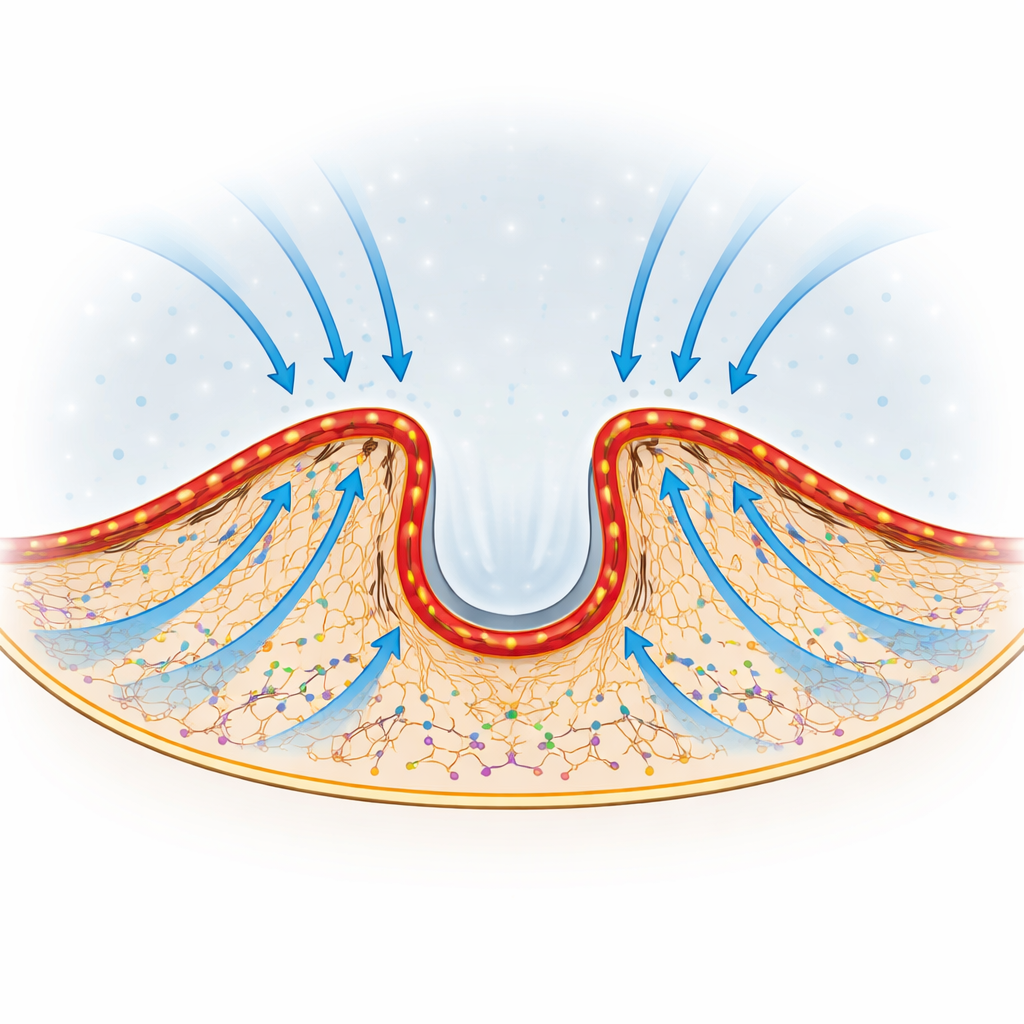
Dirigir el flujo hacia donde avanza el borde
Quizá lo más llamativo es que la dirección de esta brisa interna puede ajustarse. A medida que las células extienden o retraen distintas partes de su borde, la curvatura y la posición de los arcos de actina–miosina cambian. Los autores observaron que la actina recién activada fluye preferentemente hacia las regiones del borde que están protruyendo activamente. Cuando alteraron o aplanaron los arcos inhibiendo la miosina o cortando un arco individual con un láser enfocado, el avance local del borde flaqueó solo en el área delante de la estructura interrumpida. Esto sugiere que la forma de la barrera actúa como un conjunto de deflectores ajustables, redirigiendo el flujo y la entrega de proteínas hacia la región del borde que necesita empujar hacia adelante.
Por qué esto importa para la forma y el movimiento celular
Al revelar un compartimento frontal especializado y una brisa interna impulsada por miosina, este trabajo redefine cómo pensamos sobre la célula en movimiento. En lugar de depender únicamente de una difusión lenta y sin rumbo, las células crean un seudorgánulo en su borde líder: una zona flexible limitada por un condensado proteico que concentra moléculas clave y canaliza el flujo de fluido. Esta disposición permite a las células redistribuir rápidamente proteínas solubles donde más se necesitan, vinculando estrechamente el suministro local de proteínas con los cambios en la forma celular, la adhesión y la migración. En esencia, el frente de la célula se abastece mediante una corriente interna que se ajusta constantemente, permitiendo respuestas rápidas y energéticamente eficientes al mundo exterior.
Cita: Galbraith, C.G., English, B.P., Boehm, U. et al. Compartmentalized cytoplasmic tradewinds direct soluble proteins. Nat Commun 17, 2589 (2026). https://doi.org/10.1038/s41467-026-70688-6
Palabras clave: migración celular, citoesqueleto de actina, transporte intracelular, localización de proteínas, flujo citoplasmático