Clear Sky Science · fr
Des alizés cytoplasmiques compartimentés dirigent les protéines solubles
Comment les cellules envoient des approvisionnements à leur ligne de front
Chaque fois qu’une cellule rampe sur une surface — pour fermer une plaie, connecter le système nerveux ou contenir une infection — elle doit acheminer rapidement les protéines appropriées vers son bord avant. Cet article met au jour un « alizé » caché à l’intérieur du cytoplasme : un flux interne doux mais organisé qui balaye de nombreuses protéines solubles vers le front de la cellule, aidant celle-ci à se remodeler et à se déplacer avec une surprenante rapidité et précision.
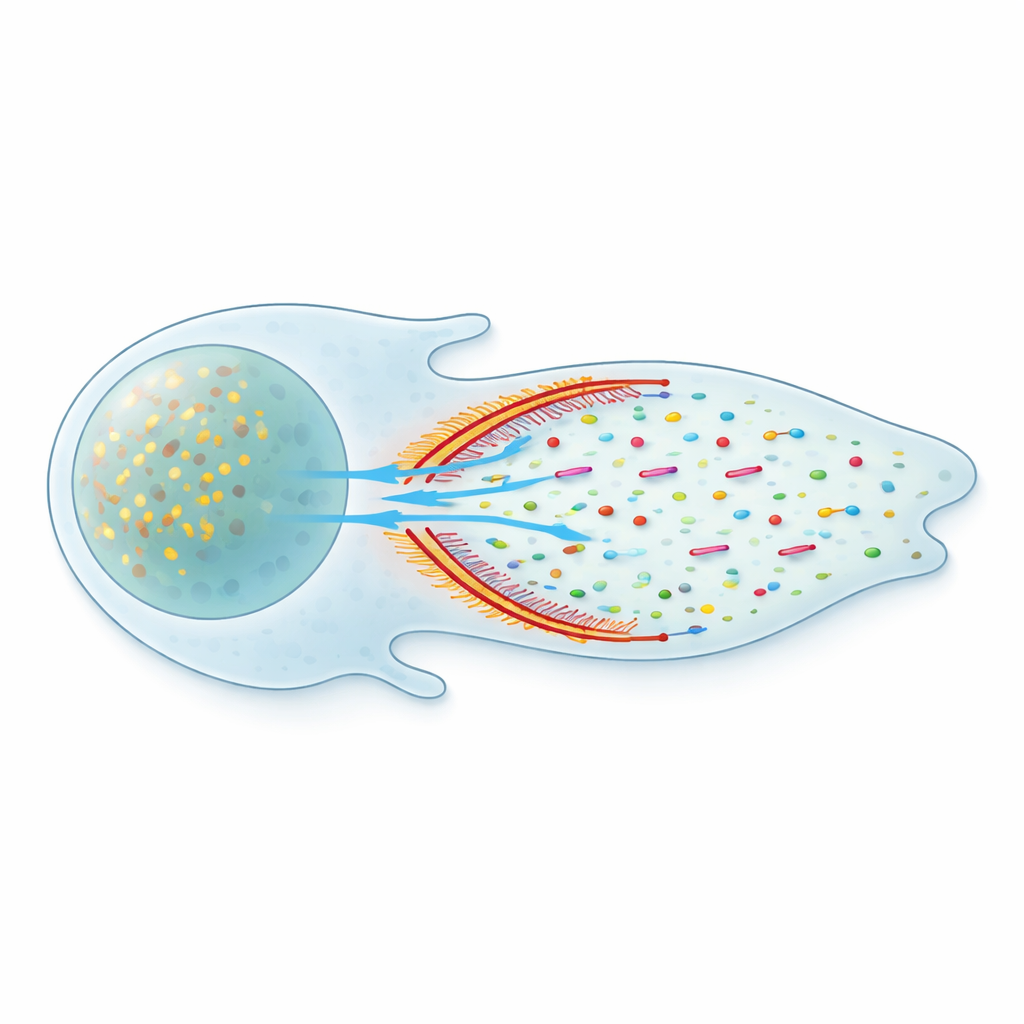
Un problème d’expédition dissimulé à l’intérieur des cellules
À l’intérieur d’une cellule, d’innombrables protéines dérivent dans un intérieur liquide encombré. Certaines voyagent dans des vésicules liées à des membranes le long de pistes moléculaires, mais beaucoup d’autres flottent librement en solution. Les représentations classiques suggèrent que ces molécules libres diffusent simplement — errant au hasard comme un parfum dans l’air. Ce tableau pose une énigme : la diffusion est lente et dépourvue de direction, et pourtant les cellules en mouvement parviennent à maintenir un flux constant de matériaux de construction, comme les monomères d’actine, prêts à l’avant où de nouvelles structures sont en permanence assemblées.
Découvrir un alizé vers l’avant
Les auteurs ont abordé cette énigme en inventant des méthodes pour observer avec grande précision le déplacement de protéines solubles individuelles dans des cellules vivantes. Ils ont utilisé la lumière pour assombrir ou activer temporairement des protéines marquées par fluorescence, puis suivi la diffusion des molécules nouvellement marquées. Dans plusieurs types cellulaires, ils ont observé quelque chose que la diffusion seule ne peut expliquer : après avoir photobléchi l’actine à l’arrière de la zone aplatie en avant, une ligne sombre nette est apparue près du bord en quelques secondes, montrant que l’actine non fluorescente avait été entraînée vers l’avant bien plus vite que ne le permettrait le mouvement aléatoire. Lorsque la myosine II — une protéine motrice capable de générer des forces contractiles — a été inhibée, ce déplacement rapide vers l’avant a fortement ralenti, indiquant que la contraction active contribue à engendrer un flux cytoplasmique avant qui facilite le transport.
Un compartiment frontal distinct avec une paroi souple
Un examen plus approfondi a révélé que ce flux n’est pas uniforme dans toute la cellule. Le front de la cellule forme plutôt un compartiment liquide distinct, séparé du reste du cytoplasme par une bande courbée d’actine et de myosine densément empaquetées. À l’aide de la microscopie super-résolution, l’équipe a montré que ces « arcs » d’actine–myosine constituent une barrière verticale s’étendant sur l’épaisseur de la cellule. Les traceurs fluorescents activés d’un côté de cette barrière avaient tendance à rester dans cette région ; le franchissement vers l’autre côté était nettement retardé. Pourtant la barrière n’est pas complètement étanche — les protéines peuvent s’en échapper — si bien que les auteurs la décrivent comme un condensat perméable qui façonne, mais n’interrompt pas, le trafic moléculaire.
Un flux non spécifique qui transporte de nombreux cargaisons
Dans le compartiment frontal, le cytoplasme se comporte comme un courant lent et dirigé. Les chercheurs ont observé que non seulement les monomères d’actine, mais aussi des protéines liant l’actine et des composants d’adhésion — y compris Arp3, vinculine et paxilline — dérivaient préférentiellement vers le bord. Même des sondes fluorescentes inertes, sans partenaires de liaison spécifiques, étaient entraînées de la même manière. Les mesures du mouvement moléculaire ont montré que la diffusion simple était similaire à l’avant et au corps de la cellule, mais qu’une composante advective ajoutée — un flux de fluide — était beaucoup plus forte à l’avant. Cela signifie que le flux est en grande partie non spécifique : il accélère l’acheminement de toute protéine soluble assez petite pour traverser le maillage d’actine, garantissant qu’un large éventail de molécules atteigne le bord plus vite que la diffusion seule.
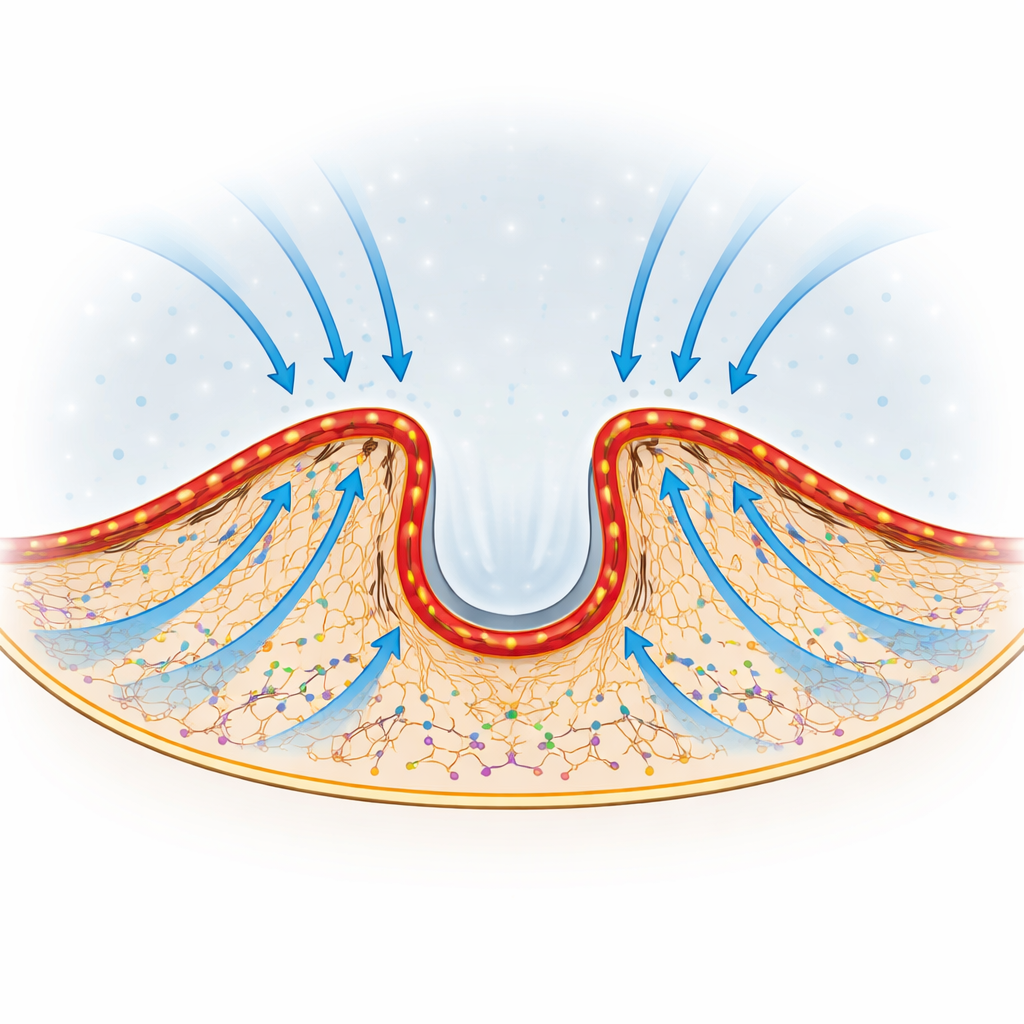
Orienter le flux vers les zones où le bord avance
Peut‑être plus frappant encore, la direction de cet alizé interne peut être modulée. À mesure que les cellules étendent ou rétractent différentes parties de leur bord, la courbure et la position des arcs d’actine–myosine se déplacent. Les auteurs ont observé que l’actine nouvellement activée convergeait préférentiellement vers les régions du bord en protrusion active. Lorsqu’ils ont modifié ou aplati les arcs en inhibant la myosine ou en sectionnant un arc individuel avec un laser focalisé, l’avancée locale du bord a fléchi uniquement devant la zone perturbée. Cela suggère que la forme de la barrière agit comme un ensemble de déflecteurs réglables, redirigeant le flux et l’acheminement des protéines vers la région du bord qui doit pousser en avant.
Pourquoi cela compte pour la forme et le mouvement cellulaires
En révélant un compartiment frontal spécialisé et un alizé interne propulsé par la myosine, ce travail modifie notre vision de la cellule en mouvement. Plutôt que de compter uniquement sur une diffusion lente et désordonnée, les cellules créent un pseudo-organite à leur avant : une zone flexible délimitée par un condensat protéique qui concentre les molécules clés et canalise le flux de fluide. Cet agencement permet aux cellules de redistribuer rapidement les protéines solubles là où elles sont le plus nécessaires, reliant étroitement l’approvisionnement local en protéines aux changements de forme, d’adhérence et de migration. En substance, le front de la cellule est alimenté par un courant interne en constante adaptation, autorisant des réponses rapides et économes en énergie face à l’environnement.»}
Citation: Galbraith, C.G., English, B.P., Boehm, U. et al. Compartmentalized cytoplasmic tradewinds direct soluble proteins. Nat Commun 17, 2589 (2026). https://doi.org/10.1038/s41467-026-70688-6
Mots-clés: migration cellulaire, cytosquelette d'actine, transport intracellulaire, localisation des protéines, flux cytoplasmique