Clear Sky Science · de
Kompartimentalisierte zytoplasmatische Tradewinds lenken lösliche Proteine
Wie Zellen ihre Versorgung an die Vorderfront schicken
Immer wenn eine Zelle über eine Oberfläche kriecht – um eine Wunde zu heilen, das Nervensystem zu verdrahten oder eine Infektion zu verfolgen – muss sie rasch die richtigen Proteine an ihre Vorderkante liefern. Diese Arbeit enthüllt eine verborgene „Tradewind“ im Cytoplasma: einen sanften, aber organisierten internen Flüssigkeitsstrom, der viele unterschiedliche lösliche Proteine zur vorderen Zellkante fegt und der Zelle hilft, sich umzuformen und sich mit überraschender Geschwindigkeit und Präzision zu bewegen.
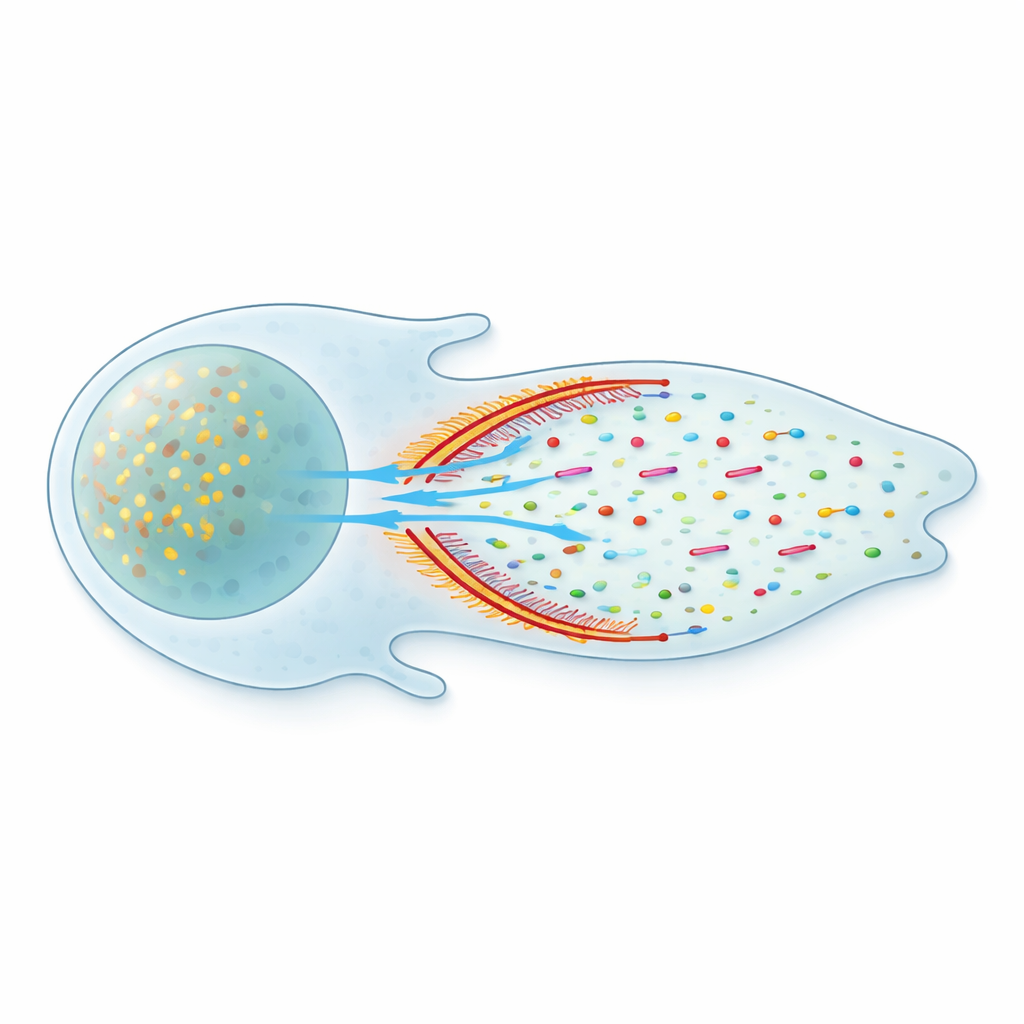
Ein verborgenes Versandproblem innerhalb der Zellen
Innerhalb einer Zelle treiben zahllose Proteine durch ein überfülltes flüssiges Innenleben. Manche reisen in membranumhüllten Paketen entlang molekularer Schienen, doch viele wichtige Proteine schwimmen frei in Lösung. Klassische Lehrbuchabbildungen suggerieren, dass diese freien Moleküle einfach diffundieren – sie wandern zufällig wie Parfüm in der Luft. Dieses Bild wirft ein Rätsel auf: Diffusion ist langsam und richtungslos, dennoch halten bewegte Zellen irgendwie einen stetigen Strom von Bausteinen, etwa Aktinmonomeren, an ihrer Vorderkante bereit, wo ständig neue Strukturen aufgebaut werden.
Die Suche nach einer vorschreitenden Tradewind
Die Autoren gingen dieses Rätsel an, indem sie Methoden entwickelten, einzelne lösliche Proteine in lebenden Zellen mit hoher Präzision zu verfolgen. Sie nutzten Licht, um fluoreszenzmarkierte Proteine vorübergehend zu verdunkeln oder zu aktivieren, und folgten dann, wie sich die neu markierten Moleküle ausbreiteten. In mehreren Zelltypen sahen sie etwas, das sich allein durch Diffusion nicht erklären ließ: Nach dem Bleichen von Aktin im hinteren Bereich der flachen Vorderzone erschien innerhalb von Sekunden eine scharfe dunkle Linie nahe der Front, was zeigte, dass nicht-fluoreszentes Aktin vorwärts getragen worden war – viel schneller als zufällige Bewegung es zulassen würde. Als sie Myosin II – ein Motorprotein, das kontraktile Kräfte erzeugen kann – hemmten, verlangsamte sich diese schnelle Vorwärtsbewegung deutlich, was darauf hinweist, dass aktive Kontraktion hilft, einen nach vorne gerichteten Cytoplasmafluss zu erzeugen, der den Transport verstärkt.
Ein separates Frontkompartiment mit einer weichen Wand
Genauere Untersuchungen zeigten, dass dieser Fluss nicht gleichmäßig durch die gesamte Zelle verläuft. Stattdessen bildet die Vorderseite der Zelle ein eigenes Flüssigkeitskompartiment, getrennt vom übrigen Cytoplasma durch einen gebogenen Streifen dicht gepackter Aktin- und Myosinfilamente. Mit Hilfe von Superauflösungs-Mikroskopie zeigten die Forscher, dass diese Aktin–Myosin-„Bögen“ eine vertikale Barriere bilden, die die Zellschichtdicke überspannt. Fluoreszente Tracer, die auf einer Seite dieser Barriere aktiviert wurden, blieben tendenziell in diesem Bereich; das Überschreiten in die andere Seite verzögerte sich messbar. Dennoch ist die Barriere nicht vollständig dicht – Proteine können hindurchlecken – weshalb die Autoren sie als eine undichte Kondensatstruktur beschreiben, die den molekularen Verkehr formt, aber nicht stoppt.
Nicht-spezifischer Fluss, der viele Frachtstücke bewegt
Innerhalb des Frontkompartiments verhält sich das Cytoplasma wie ein langsamer, gerichteter Strom. Die Forscher beobachteten, dass sich nicht nur Aktinmonomere, sondern auch Aktin-bindende Proteine und Adhäsionskomponenten – darunter Arp3, Vinculin und Paxillin – bevorzugt zur Kante hin bewegten. Selbst inerte fluoreszente Sonden ohne spezifische Bindungspartner wurden auf dieselbe Weise vorwärts getragen. Messungen der molekularen Bewegung zeigten, dass die einfache Diffusion in Vorder- und Körperbereich der Zelle ähnlich war, doch ein zusätzlicher advektiver Anteil – also Flüssigkeitsfluss – war an der Front deutlich stärker. Das bedeutet, dass der Fluss weitgehend unspezifisch ist: Er beschleunigt die Anlieferung jedes löslichen Proteins, das klein genug ist, um sich durch das Aktinnetz zu bewegen, und sorgt so dafür, dass ein breites Werkzeugset von Molekülen die Kante schneller erreicht, als es Diffusion allein könnte.
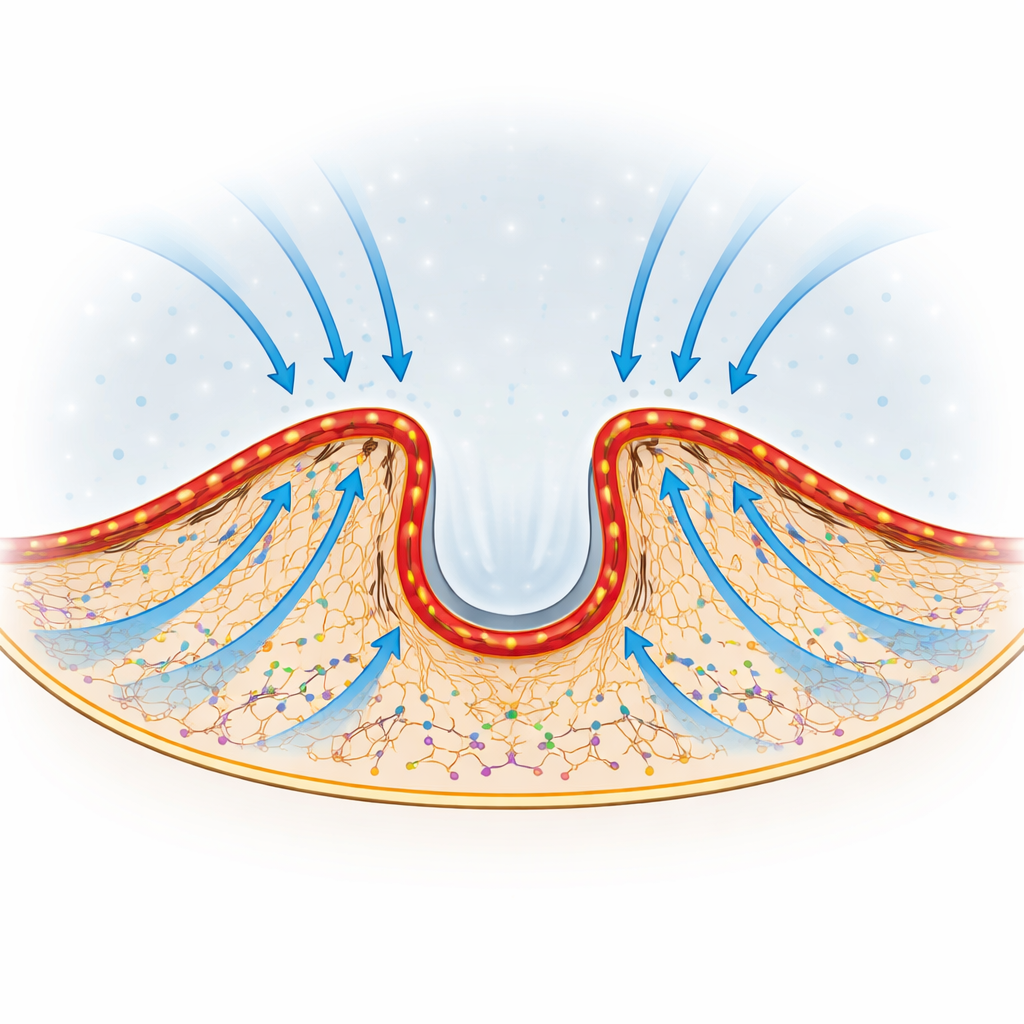
Den Fluss dorthin lenken, wo die Kante vorrückt
Am auffälligsten ist vielleicht, dass die Richtung dieses internen Tradewinds einstellbar ist. Während Zellen verschiedene Bereiche ihrer Kante ausfahren oder zurückziehen, verändern sich die Krümmung und Position der Aktin–Myosin-Bögen. Die Autoren beobachteten, dass neu aktiviertes Aktin bevorzugt zu den Regionen der Kante strömt, die aktiv protrudieren. Wenn sie die Bögen veränderten oder abflachten – etwa durch Hemmung von Myosin oder durch das Durchtrennen eines einzelnen Bogens mit einem fokussierten Laser – stockte die lokale Kantenfortschreitung nur im Bereich vor der gestörten Struktur. Das legt nahe, dass die Form der Barriere wie ein Satz verstellbarer Leitbleche wirkt, die den Fluss und die Proteinanlieferung in diejenige Region umleiten, die voranschieben muss.
Warum das für Zellform und Bewegung wichtig ist
Durch die Enthüllung eines spezialisierten Frontkompartiments und einer myosingetriebenen internen Tradewind verändert diese Arbeit unser Verständnis der bewegten Zelle. Anstatt sich ausschließlich auf langsame, ziellose Diffusion zu verlassen, schaffen Zellen ein Pseudo-Organell an ihrer Vorderkante: eine flexible Zone, begrenzt durch ein Proteinkondensat, das sowohl Schlüsselmoleküle konzentriert als auch den Flüssigkeitsstrom kanalisiert. Diese Anordnung ermöglicht es Zellen, lösliche Proteine schnell dorthin umzuschichten, wo sie am dringendsten gebraucht werden, und koppelt so eng die lokale Proteinanlieferung an Änderungen von Zellform, Adhäsion und Migration. Im Kern wird die Vorderseite der Zelle von einem ständig anpassenden internen Strom versorgt, der schnelle, energieeffiziente Reaktionen auf die Umgebung erlaubt.
Zitation: Galbraith, C.G., English, B.P., Boehm, U. et al. Compartmentalized cytoplasmic tradewinds direct soluble proteins. Nat Commun 17, 2589 (2026). https://doi.org/10.1038/s41467-026-70688-6
Schlüsselwörter: Zellmigration, Aktin-Zytoskelett, intrazellulärer Transport, Proteintlokalisierung, zytoplasmatischer Fluss