Clear Sky Science · it
Allineamento spazio-temporale del trasferimento di lacune e dell’ossidazione dell’acqua per una scissione fotocatalitica dell’acqua altamente efficiente
Convertire luce solare e acqua in combustibile
Dividere l’acqua in idrogeno e ossigeno usando solo la luce solare è un obiettivo a lungo inseguito per l’energia pulita, perché l’idrogeno può fungere da combustibile senza carbonio prodotto direttamente dall’acqua, una risorsa abbondante. Questo lavoro esplora perché un materiale particolare, il titan ato di stronzio drogato con alluminio, si avvicini in modo notevole a questo risultato con quasi nessuna luce sprecata, e rivela come la sua struttura interna guidi con precisione le cariche nei luoghi giusti al momento giusto.

Un cristallo speciale per scindere l’acqua
La scissione complessiva dell’acqua significa usare la luce per guidare entrambe le semireazioni: produrre idrogeno e ossigeno dall’acqua pura senza additivi chimici. Molti fotocatalizzatori eseguono efficacemente una delle due semireazioni, ma pochissimi gestiscono entrambe simultaneamente senza perdere la maggior parte dell’energia assorbita. Il titan ato di stronzio drogato con alluminio (SrTiO3:Al) è un’eccezione sorprendente, raggiungendo efficienze quantiche apparenti vicine al 100%, il che significa che quasi ogni fotone assorbito porta a un cambiamento chimico utile. Gli autori usano campioni che raggiungono oltre il 90% di efficienza come sistema modello per chiedersi: che ruolo svolge esattamente l’alluminio dentro questo cristallo che lo rende così efficace?
Modellare il cristallo dall’esterno verso l’interno
Il gruppo confronta cristalli preparati con diverse procedure e con differenti quantità di alluminio. Scoprono che la performance non dipende da caratteristiche ovvie come la dimensione delle particelle o l’assorbimento della luce. La chiave è, invece, dove vanno a collocarsi gli atomi di alluminio. Nei migliori campioni, l’alluminio è concentrato in un sottile strato vicino alla superficie della particella, mentre il volume interno contiene solo una piccola quantità uniforme. Questa disposizione a gradiente riduce sottilmente il reticolo e, soprattutto, sopprime difetti come vacanze di ossigeno e il titanio in stati di carica indesiderati; questi difetti altrimenti fungerebbero da centri di ricombinazione che dissipano le cariche fotogenerate. Quando l’alluminio è distribuito male — raggruppato solo agli angoli o distribuito troppo uniformemente — l’efficienza nella scissione dell’acqua cala drasticamente.
Guidare e immagazzinare le cariche nello spazio e nel tempo
Utilizzando avanzate immagini di fotovoltaicità di superficie, gli autori mappano come si muovono le cariche all’interno di singole particelle sotto illuminazione. Il gradiente nella concentrazione di alluminio crea un campo elettrico interno che spinge le lacune cariche positivamente dall’interno verso la superficie. Allo stesso tempo, siti legati all’alluminio alla o vicino alla superficie agiscono come trappole che trattengono queste lacune per tempi insolitamente lunghi — estendendo la loro vita da circa centinaia di miliardesimi di secondo a circa un centesimo di secondo. Misure transitorie dettagliate mostrano che questa popolazione di lacune intrappolate a vita lunga quasi non decade su scale temporali microsecondo–millisecondo, il che significa che la ricombinazione con gli elettroni è fortemente soppressa. Gli elettroni vengono invece attratti verso specifiche faccette decorate con cocatalizzatori metallici, dove si produce idrogeno, mentre le lacune si accumulano nei punti dove si formerà ossigeno.
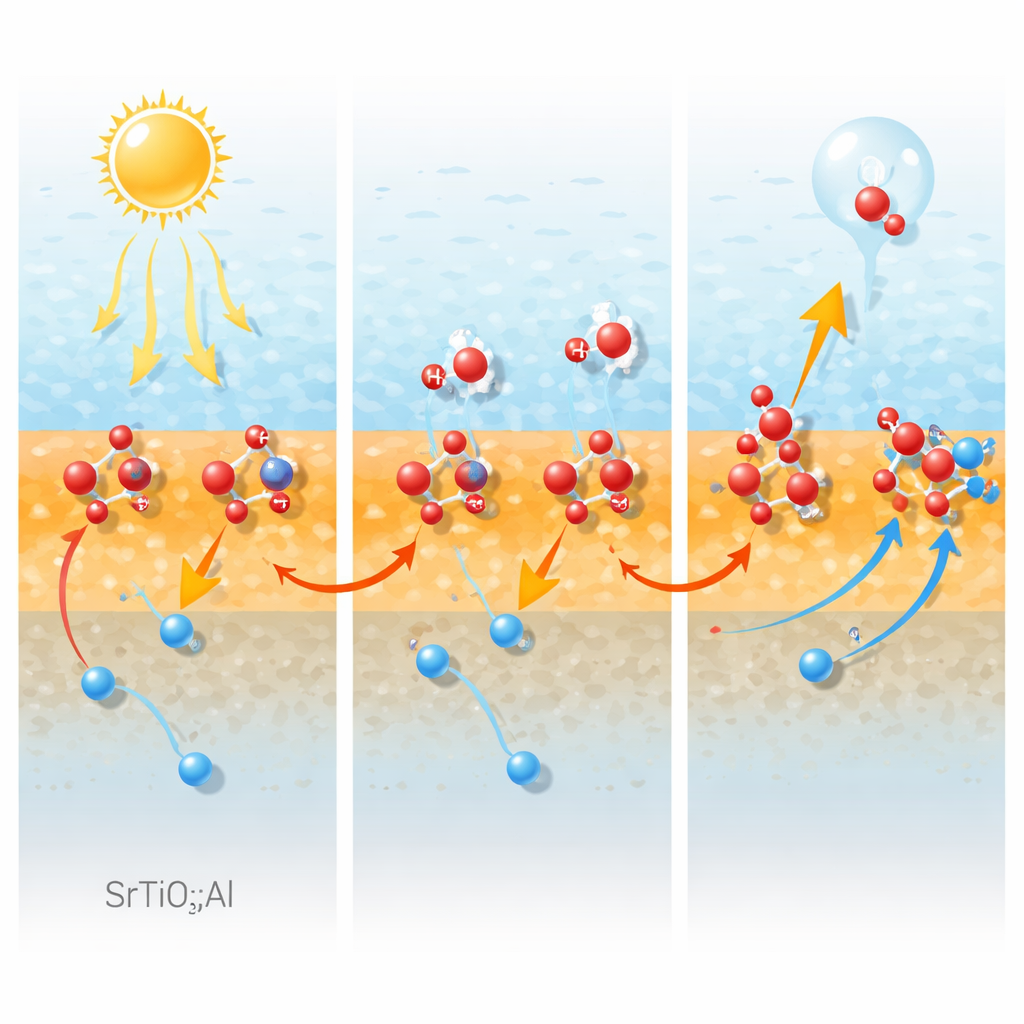
Creare i punti giusti perché l’acqua reagisca
Per capire se questi siti di intrappolamento delle lacune aiutano anche l’acqua stessa, i ricercatori sondano l’ambiente locale dell’alluminio usando risonanza magnetica nucleare ad alto campo e spettroscopia infrarossa. Identificano due tipi principali di centri di alluminio: unità altamente simmetriche sepolte nel volume e unità superficiali meno simmetriche legate a gruppi ossidrile. Questi siti superficiali di alluminio «idrossilati» risultano essere punti di atterraggio ideali per le molecole d’acqua. I loro segnali si indeboliscono quando i campioni vengono disidratati o invecchiati, e questa perdita segue da vicino un calo nell’adsorbimento dell’acqua e nell’attività di evoluzione dell’ossigeno. Ulteriori test mostrano che il materiale può ancora ossidare l’acqua in modo abbastanza efficiente anche senza un cocatalizzatore per l’evoluzione dell’ossigeno aggiunto, e che l’alluminio aumenta notevolmente la capacità intrinseca della superficie di portare a termine la difficoltosa semireazione di formazione dell’ossigeno.
Collegare la danza microscopica al quadro energetico più ampio
Simulazioni computazionali supportano un meccanismo in cui gruppi ossidrile vicini sui siti superficiali contenenti alluminio aiutano le molecole d’acqua ad accoppiarsi e formare legami ossigeno–ossigeno mentre perdono protoni. Allineando, sia nello spazio sia nel tempo, cariche positive a vita lunga con questi siti appositamente configurati per legare l’acqua, il materiale assicura che la lenta reazione multi‑passo di formazione dell’ossigeno possa tenere il passo con il ritmo con cui la luce fornisce cariche. In termini semplici, l’alluminio svolge una doppia funzione: costruisce una rampa interna che muove le cariche verso la superficie e modella i siti stessi in cui l’acqua viene attivata. Questo ruolo duplice spiega come il titan ato di stronzio drogato con alluminio spinga le efficienze di scissione dell’acqua così vicino al limite teorico, e fornisce principi di progettazione per futuri fotocatalizzatori che mirano a trasformare luce e acqua in combustibile pulito con perdite minime.
Citazione: Luo, Y., Chen, R., Dittrich, T. et al. Spatiotemporal alignment of hole transfer and water oxidation for highly efficient photocatalytic water splitting. Nat Commun 17, 2767 (2026). https://doi.org/10.1038/s41467-026-69276-5
Parole chiave: scissione fotocatalitica dell’acqua, idrogeno solare, titanato di stronzio, separazione di carica, evoluzione dell’ossigeno