Clear Sky Science · de
Räumlich‑zeitliche Abstimmung von Löchertransfer und Wasseroxidation für hocheffiziente photokatalytische Wasserspaltung
Sonne und Wasser in Treibstoff verwandeln
Wasser allein mit Sonnenlicht in Wasserstoff und Sauerstoff zu spalten ist ein lange verfolgtes Ziel für saubere Energie, weil Wasserstoff als kohlenstofffreier Brennstoff direkt aus dem reichlich vorhandenen Wasser gewonnen werden kann. Diese Arbeit untersucht, warum ein bestimmtes Material, aluminiumdotiertes Strontiumtitanat, erstaunlich nahe daran kommt, dies mit nahezu keinem Lichtverlust zu erreichen, und zeigt, wie seine innere Struktur Ladungen zur richtigen Zeit an die richtigen Orte lenkt.

Ein spezieller Kristall für die Wasserspaltung
Unter kompletter Wasserspaltung versteht man das Verwenden von Licht, um beide Reaktionshälften voranzutreiben: aus reinem Wasser ohne Zusatzstoffe Wasserstoff und Sauerstoff zu erzeugen. Viele Photokatalysatoren können eine der Hälften effizient leisten, aber nur sehr wenige bewältigen beide gleichzeitig, ohne den Großteil der absorbierten Energie zu verlieren. Aluminiumdotiertes Strontiumtitanat (SrTiO3:Al) ist eine auffällige Ausnahme und erreicht scheinbare Quanteneffizienzen nahe 100 %, das heißt fast jedes absorbierte Photon führt zu einer sinnvollen chemischen Reaktion. Die Autoren verwenden Proben, die über 90 % Effizienz erreichen, als Modellsystem und fragen: Was genau bewirkt Aluminium in diesem Kristall, das ihn so wirkungsvoll macht?
Den Kristall von außen nach innen formen
Das Team vergleicht Kristalle, die mit verschiedenen Herstellungsverfahren und unterschiedlichen Aluminiumgehalten hergestellt wurden. Sie stellen fest, dass die Leistung nicht an offensichtlichen Merkmalen wie Partikelgröße oder Lichtabsorption hängt. Entscheidend ist vielmehr, wo die Aluminiumatome sich anreichern. In den besten Proben ist Aluminium in einer dünnen Schale nahe der Partikeloberfläche konzentriert, während das Volumen nur eine geringe, gleichmäßige Menge enthält. Diese „Gradient“-Anordnung verkleinert das Gitter leicht und unterdrückt entscheidend Defekte wie Sauerstoffleerstellen und Titan in unerwünschten Ladungszuständen; solche Defekte würden sonst als Rekombinationszentren wirken und photogenerierte Ladungen verschwenden. Wenn Aluminium ungünstig verteilt ist — nur in Ecken gehäuft oder zu gleichmäßig verteilt — sinkt die Wasserspaltungseffizienz stark.
Ladungen in Raum und Zeit lenken und speichern
Mit fortschrittlicher Oberflächen‑Photospannungsbildgebung kartieren die Autoren, wie sich Ladungen in einzelnen Partikeln unter Beleuchtung bewegen. Der Gradient in der Aluminiumkonzentration erzeugt ein internes elektrisches Feld, das positiv geladene Löcher aus dem Inneren zur Oberfläche drückt. Gleichzeitig fungieren aluminiumbezogene Stellen an oder nahe der Oberfläche als Fallen, die diese Löcher ungewöhnlich lange halten — ihre Lebensdauer verlängert sich von etwa einhundert Nanosekunden auf etwa ein Hundertstel Sekunde. Detaillierte transiente Messungen zeigen, dass diese langlebige, gefangene Lochpopulation über Mikrosekunden‑ bis Millisekunden‑Zeitskalen kaum zerfällt, was eine starke Unterdrückung der Rekombination mit Elektronen bedeutet. Elektronen werden stattdessen zu bestimmten Flächen gezogen, die mit metallischen Kokatalysatoren versehen sind, wo Wasserstoff erzeugt wird, während Löcher dort akkumulieren, wo Sauerstoff entsteht.
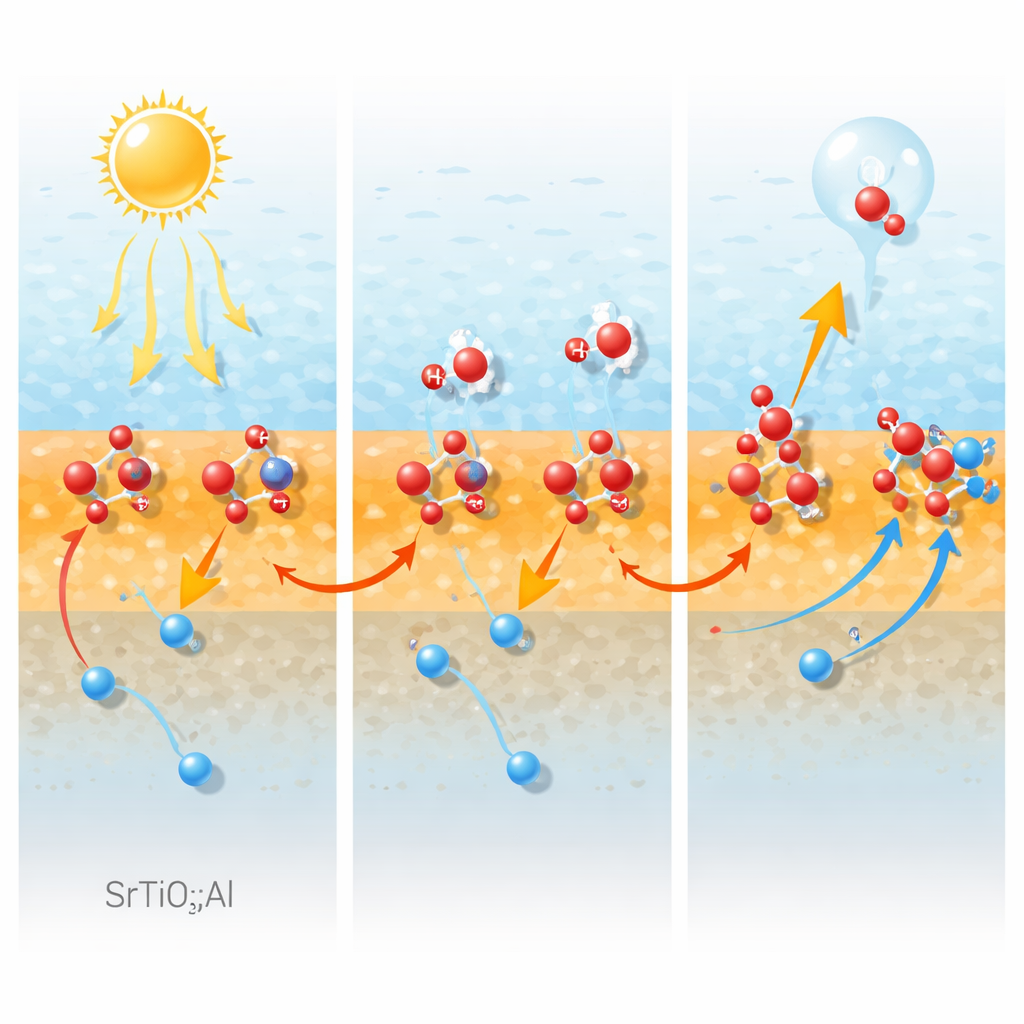
Die richtigen Orte für die Reaktion mit Wasser schaffen
Um zu klären, ob diese Lochfangstellen auch dem Wasser selbst zugutekommen, untersuchen die Forscher die lokale Umgebung des Aluminiums mit hochfeldigem Kernspinresonanz‑ und Infrarotspektroskopie. Sie identifizieren zwei Haupttypen von Aluminiumzentren: hochsymmetrische Einheiten im Volumen und weniger symmetrische Oberflächeneinheiten, die an Hydroxylgruppen gebunden sind. Diese oberflächen‑“hydroxilierten” Aluminiumstellen erweisen sich als bevorzugte Andockstellen für Wassermoleküle. Ihre Signale schwächen sich ab, wenn die Proben dehydriert oder gealtert werden, und dieser Verlust korreliert eng mit einer Abnahme der Wasseradsorption und der Sauerstoffentwicklungsaktivität. Weitere Tests zeigen, dass das Material Wasser recht effizient oxidieren kann, selbst ohne einen zugesetzten Sauerstoffentwicklungskokatalysator, und dass Aluminium die intrinsische Fähigkeit der Oberfläche, die schwierige sauerstoffbildende Halbreaktion auszuführen, deutlich verbessert.
Den mikroskopischen Tanz mit der großen Energiebilanz verknüpfen
Computergestützte Simulationen stützen einen Mechanismus, bei dem benachbarte Hydroxylgruppen auf aluminiumhaltigen Oberflächenstellen helfen, Wassermoleküle zu koppeln und O–O‑Bindungen zu bilden, während Protonen abgegeben werden. Indem langlebige positive Ladungen räumlich und zeitlich mit diesen speziell konfigurierten Wasserbindestellen zusammengebracht werden, stellt das Material sicher, dass die langsame, mehrstufige sauerstoffbildende Reaktion mit der Rate Schritt halten kann, mit der Licht Ladungen liefert. Vereinfacht gesagt erfüllt Aluminium eine doppelte Aufgabe: Es baut eine interne Rampe, die Ladungen zur Oberfläche bewegt, und formt zugleich die Stellen, an denen Wasser aktiviert wird. Diese doppelte Rolle erklärt, wie aluminiumdotiertes Strontiumtitanat die Effizienz der Wasserspaltung so nahe an das theoretische Maximum treibt, und liefert Gestaltungsprinzipien für künftige Photokatalysatoren, die Sonne und Wasser mit minimalen Verlusten in sauberen Treibstoff verwandeln sollen.
Zitation: Luo, Y., Chen, R., Dittrich, T. et al. Spatiotemporal alignment of hole transfer and water oxidation for highly efficient photocatalytic water splitting. Nat Commun 17, 2767 (2026). https://doi.org/10.1038/s41467-026-69276-5
Schlüsselwörter: photokatalytische Wasserspaltung, Solarwasserstoff, Strontiumtitanat, Ladungstrennung, Sauerstoffentwicklung