Clear Sky Science · fr
Alignement spatiotemporel du transfert de trous et de l’oxydation de l’eau pour une scission photocatalytique de l’eau hautement efficace
Transformer le soleil et l’eau en carburant
Décomposer l’eau en hydrogène et en oxygène en n’utilisant que la lumi�re solaire est un objectif de longue date pour l����������������u000 clean energy, car l’hydrogène peut servir de carburant sans carbone produit directement � partir d’une ressource abondante comme l’eau. Cet article examine pourquoi un matériau particulier, le titanate de strontium dopé à l’aluminium, s’en approche remarquablement en n’utilisant presque pas de lumière de façon inutile, et il révèle comment sa structure interne oriente soigneusement les charges vers les bons endroits au bon moment.

Un cristal particulier pour scinder l’eau
La scission globale de l’eau signifie utiliser la lumi�re pour entraîner les deux demi‑réactions : produire de l’hydrogène et de l’oxygène à partir d’eau pure sans additifs chimiques. Beaucoup de photocatalyseurs accomplissent bien une demi‑réaction, mais très peu gèrent les deux simultanément sans perdre la majeure partie de l’énergie absorbée. Le titanate de strontium dopé à l’aluminium (SrTiO3:Al) constitue une exception remarquable, atteignant des efficacités quantiques apparentes proches de 100 %, ce qui signifie que presque chaque photon absorbé conduit à une transformation chimique utile. Les auteurs utilisent des échantillons dépassant 90 % d’efficacité comme système modèle pour se demander : que fait exactement l’aluminium dans ce cristal pour le rendre si efficace ?
Façonner le cristal de l’extérieur vers l’intérieur
L’équipe compare des cristaux préparés par différentes méthodes et contenant des quantités d’aluminium variables. Ils constatent que la performance ne dépend pas de traits évidents comme la taille des particules ou l’absorption de la lumi�re. L’élément clé est plutôt l’emplacement des atomes d’aluminium. Dans les meilleurs échantillons, l’aluminium se concentre dans une fine couche proche de la surface des particules, alors que le volume interne ne contient qu’une faible quantité uniforme. Cet arrangement en « gradient » contracte subtilement le réseau cristallin et, surtout, supprime des défauts tels que des lacunes en oxygène et du titane dans un état de charge indésirable ; ces défauts agiraient autrement comme centres de recombinaison qui gaspillent les charges photogénérées. Quand l’aluminium est mal distribué — regroupé seulement aux arêtes ou trop uniformément réparti —, l’efficacité de la scission de l’eau chute fortement.
Guider et stocker les charges dans le temps et l’espace
À l’aide d’imagerie avancée de photopotentiel de surface, les auteurs cartographient le mouvement des charges à l’intérieur de particules uniques sous illumination. Le gradient de concentration d’aluminium crée un champ électrique interne qui pousse les trous (charges positives) de l’intérieur vers la surface. Parallèlement, des sites liés à l’aluminium à la surface ou à proximité agissent comme des pièges qui retiennent ces trous pendant des durées exceptionnellement longues — allongeant leur durée de vie d’environ une dizaine de nanosecondes à environ un centième de seconde. Des mesures transitoires détaillées montrent que cette population de trous piégés et de longue durée de vie décroît à peine sur des échelles de temps micro‑ à millisecondes, ce qui signifie que la recombinaison avec les électrons est fortement supprimée. Les électrons sont plutôt attirés vers des faces spécifiques décorées par des cocatalyseurs métalliques, où est produit l’hydrogène, tandis que les trous s’accumulent là où se formera l’oxygène.
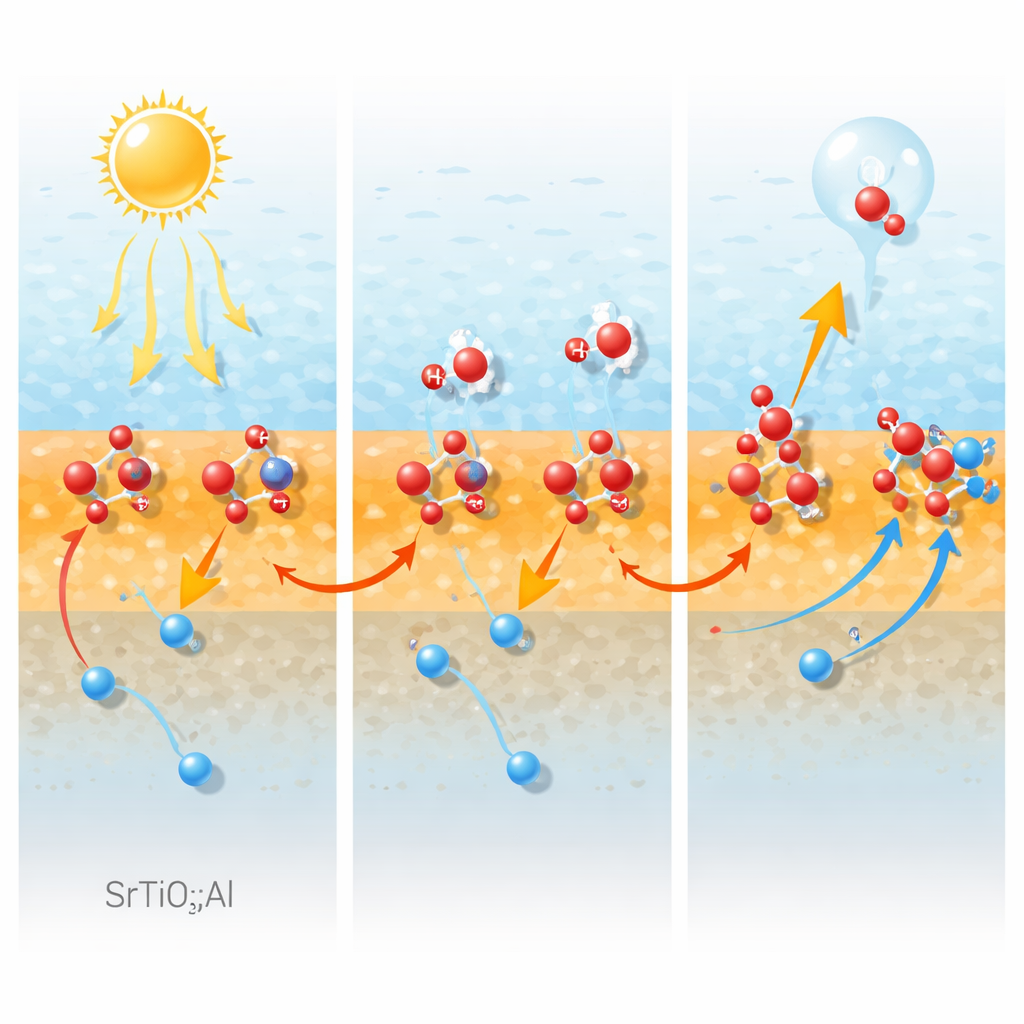
Créer les bons sites pour que l’eau réagisse
Pour savoir si ces sites de piégeage de trous aident aussi la molécule d’eau, les chercheurs sondent l’environnement local de l’aluminium par résonance magnétique nucléaire à champ élevé et spectroscopie infrarouge. Ils identifient deux types principaux de centres d’aluminium : des unités hautement symétriques enfouies dans le volume et des unités de surface moins symétriques liées à des groupes hydroxyle. Ces sites d’aluminium « hydroxylés » de surface s’avèrent être des plateformes privilégiées pour l’adsorption des molécules d’eau. Leurs signaux s’affaiblissent lorsque les échantillons sont déshydratés ou vieillissent, et cette perte suit de près la baisse d’adsorption d’eau et de l’activité d’évolution d’oxygène. D’autres tests montrent que le matériau peut encore oxyder l’eau assez efficacement même sans cocatalyseur d’évolution d’oxygène ajouté, et que l’aluminium renforce grandement la capacité intrinsèque de la surface à accomplir la difficile demi‑réaction de formation d’oxygène.
Relier la danse microscopique au grand enjeu énergétique
Des simulations informatiques étayent un mécanisme dans lequel des groupes hydroxyle voisins sur des sites de surface contenant de l’aluminium aident les molécules d’eau à se coupler et à former des liaisons oxygène‑oxygène tout en perdant des protons. En alignant, à la fois dans l’espace et dans le temps, des charges positives de longue durée de vie avec ces sites spécialement configurés pour lier l’eau, le matériau fait en sorte que la lente réaction multi‑étapes de formation d’oxygène puisse suivre le rythme auquel la lumière fournit les charges. En termes simples, l’aluminium joue un double rôle : il construit une rampe interne qui déplace les charges vers la surface et il façonne les sites mêmes où l’eau est activée. Ce double rôle explique comment le titanate de strontium dopé à l’aluminium porte l’efficacité de la scission de l’eau si proche de la limite théorique, et fournit des principes de conception pour de futurs photocatalyseurs visant à transformer le soleil et l’eau en carburant propre avec des pertes minimales.
Citation: Luo, Y., Chen, R., Dittrich, T. et al. Spatiotemporal alignment of hole transfer and water oxidation for highly efficient photocatalytic water splitting. Nat Commun 17, 2767 (2026). https://doi.org/10.1038/s41467-026-69276-5
Mots-clés: scission photocatalytique de l’eau, hydrogène solaire, titanate de strontium, s paration de charge, oxygen evolution