Clear Sky Science · es
Alineación espacio‑temporal de la transferencia de huecos y la oxidación del agua para una división fotocatalítica del agua de alta eficiencia
Convertir la luz solar y el agua en combustible
Separar el agua en hidrógeno y oxígeno usando únicamente la luz solar es un objetivo largamente perseguido para la energía limpia, porque el hidrógeno puede servir como combustible sin carbono fabricado directamente a partir del abundante agua. Este artículo explora por qué un material concreto, el titanato de estroncio dopado con aluminio, se acerca de forma notable a lograrlo con casi ninguna luz desperdiciada, y revela cómo su estructura interna guía cuidadosamente las cargas a los lugares correctos en los momentos adecuados.

Un cristal especial para dividir el agua
La división completa del agua implica usar la luz para impulsar ambas mitades de la reacción: producir hidrógeno y oxígeno a partir de agua pura sin añadidos químicos. Muchos fotocatalizadores realizan una de las dos mitades de forma eficiente, pero muy pocos manejan ambas simultáneamente sin perder la mayor parte de la energía absorbida. El titanato de estroncio dopado con aluminio (SrTiO3:Al) es una excepción notable, alcanzando eficiencias cuánticas aparentes cercanas al 100%, lo que significa que casi cada fotón absorbido conduce a un cambio químico útil. Los autores usan muestras que alcanzan más del 90% de eficiencia como sistema modelo para preguntar: ¿qué hace exactamente el aluminio dentro de este cristal que lo hace tan eficaz?
Modelando el cristal de afuera hacia adentro
El equipo compara cristales preparados por diferentes rutas y con distintos contenidos de aluminio. Encuentran que el rendimiento no depende de rasgos obvios como el tamaño de partícula o la absorción de luz. En cambio, la clave es dónde acaban los átomos de aluminio. En las mejores muestras, el aluminio se concentra en una delgada envoltura cerca de la superficie de la partícula, mientras que el volumen contiene solo una pequeña cantidad uniforme. Esta disposición en “gradiente” reduce sutilmente la red cristalina y, de forma crucial, suprime defectos como vacantes de oxígeno y titanio en estados de carga indeseados; esos defectos actuarían de otro modo como centros de recombinación que desperdician las cargas fotogeneradas. Cuando el aluminio está mal distribuido —agrupado solo en esquinas o demasiado uniforme—, la eficiencia de la división del agua cae drásticamente.
Guiando y almacenando cargas en espacio y tiempo
Empleando imágenes avanzadas de fotovoltaje superficial, los autores cartografían cómo se mueven las cargas dentro de partículas individuales bajo iluminación. El gradiente en la concentración de aluminio crea un campo eléctrico interno que empuja los huecos, cargados positivamente, desde el interior hacia la superficie. Al mismo tiempo, los sitios relacionados con el aluminio en o cerca de la superficie actúan como trampas que retienen estos huecos durante tiempos inusualmente largos —extendiendo su vida útil desde alrededor de diez mil millones de veces menos (10^-9 s) hasta aproximadamente una centésima de segundo. Medidas transitorias detalladas muestran que esta población de huecos atrapados y de larga vida casi no decae en escalas de microsegundos a milisegundos, lo que significa que la recombinación con electrones está fuertemente suprimida. En su lugar, los electrones son atraídos hacia facetas específicas decoradas con cocatalizadores metálicos, donde se produce el hidrógeno, mientras que los huecos se acumulan donde se formará el oxígeno.
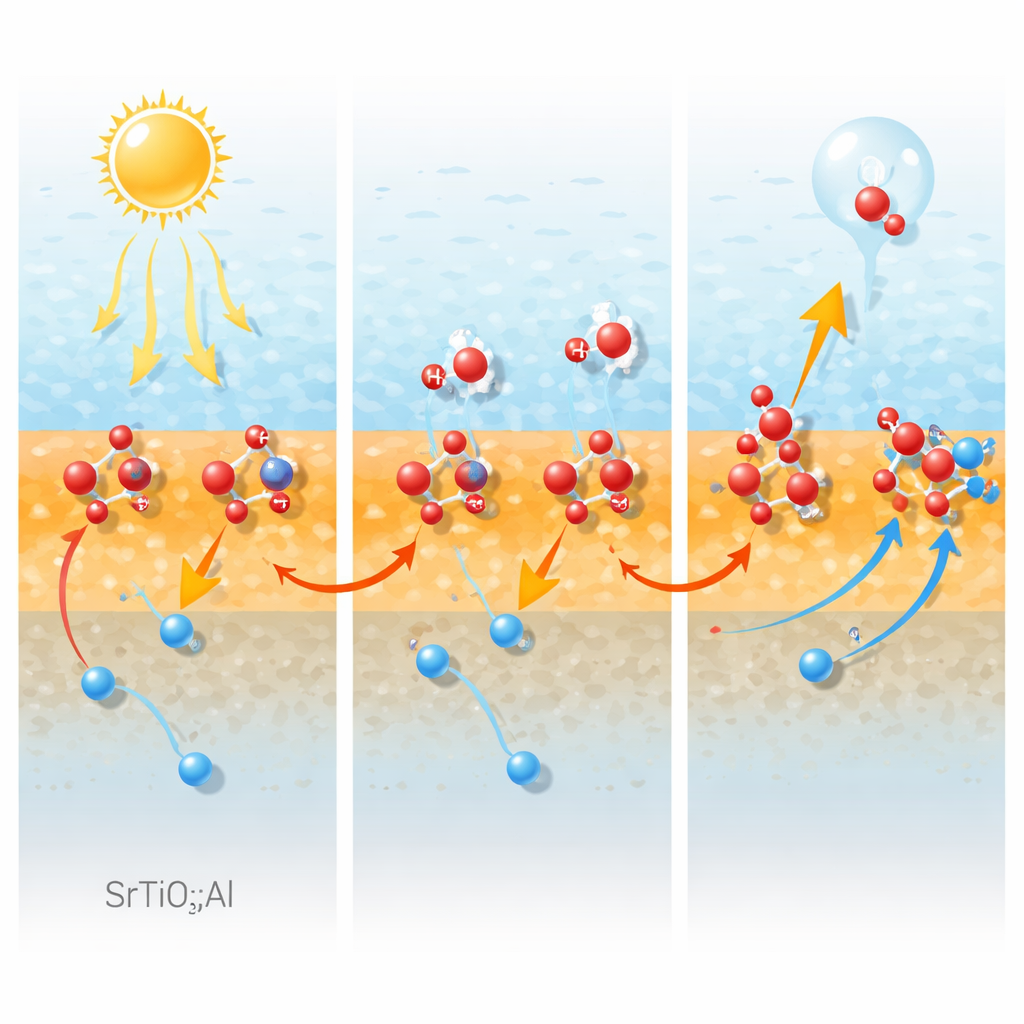
Creando los puntos adecuados para que reaccione el agua
Para entender si estos sitios atrapadores de huecos también ayudan al propio agua, los investigadores sondean el entorno local del aluminio usando resonancia magnética nuclear de alto campo y espectroscopía infrarroja. Identifican dos tipos principales de centros de aluminio: unidades altamente simétricas enterradas en el volumen y unidades superficiales menos simétricas enlazadas a grupos hidroxilo. Estos sitios superficiales «hidroxilados» de aluminio resultan ser plataformas ideales para que aterricen moléculas de agua. Sus señales se debilitan cuando las muestras se deshidratan o envejecen, y esa pérdida sigue de cerca una caída en la adsorción de agua y en la actividad de evolución de oxígeno. Pruebas adicionales muestran que el material puede oxidar agua con bastante eficiencia incluso sin un cocatalizador añadido de evolución de oxígeno, y que el aluminio incrementa en gran medida la capacidad intrínseca de la superficie para llevar a cabo la difícil mitad de formación de oxígeno.
Vinculando la danza microscópica con el gran panorama energético
Simulaciones computacionales apoyan un mecanismo en el que grupos hidroxilo vecinos en sitios superficiales que contienen aluminio ayudan a que las moléculas de agua se acoplen y formen enlaces oxígeno‑oxígeno mientras ceden protones. Al alinear, tanto en espacio como en tiempo, cargas positivas de larga vida con estos sitios especialmente configurados para unir agua, el material asegura que la lenta y multinivel reacción de formación de oxígeno pueda seguir el ritmo al que la luz suministra cargas. En términos sencillos, el aluminio desempeña una doble función: construye una rampa interna que lleva las cargas a la superficie y a la vez moldea los propios sitios donde se activa el agua. Este papel dual explica cómo el titanato de estroncio dopado con aluminio empuja las eficiencias de división del agua tan cerca del límite teórico, y ofrece principios de diseño para futuros fotocatalizadores que aspiren a convertir la luz solar y el agua en combustible limpio con pérdidas mínimas.
Cita: Luo, Y., Chen, R., Dittrich, T. et al. Spatiotemporal alignment of hole transfer and water oxidation for highly efficient photocatalytic water splitting. Nat Commun 17, 2767 (2026). https://doi.org/10.1038/s41467-026-69276-5
Palabras clave: división fotocatalítica del agua, hidrógeno solar, titanato de estroncio, separación de cargas, evolución del oxígeno