Clear Sky Science · it
Oltre il privilegio immunitario: il cervello come interfaccia immunologica dinamica
Perché il sistema di sicurezza del cervello è importante
Per decenni i manuali di biologia hanno insegnato che il cervello viveva dietro porte chiuse, in gran parte invisibile alle difese immunitarie del corpo. Questo articolo ribalta quella semplificazione. Spiega come il cervello scambi costantemente segnali, cellule e rifiuti con il resto del corpo — e come questo traffico nascosto influenzi tutto, dalle infezioni e dalla sclerosi multipla all’Alzheimer e ai tumori cerebrali. Comprendere questa nuova immagine del “controllo alle frontiere” del cervello potrebbe portare a terapie più intelligenti che placano l’infiammazione dannosa pur potenziando la capacità del corpo di proteggere e riparare i neuroni.
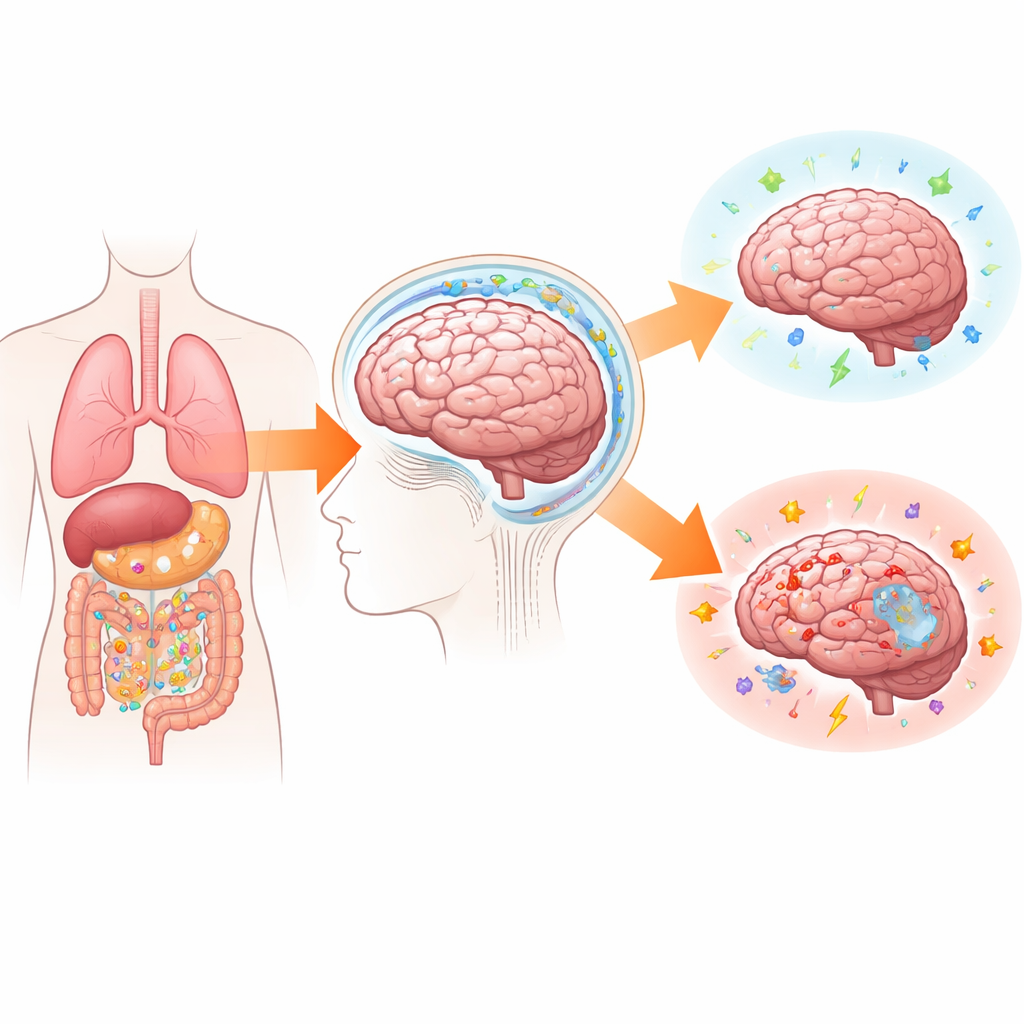
La recinzione del cervello è un cancello intelligente
La barriera emato-encefalica è spesso paragonata a una muraglia che tiene fuori gli invasori. In realtà si comporta più come un valico di frontiera intelligente. Sottile strati di cellule vascolari saldamente connesse sono avvolti da cellule di supporto che decidono quali molecole e quali cellule immunitarie possono passare. Quando il cervello è sano, passa solo un traffico limitato. Durante infezioni o lesioni, quelle stesse cellule esibiscono siti appiccicosi di ancoraggio e rilasciano “odori” chimici che guidano cellule immunitarie selezionate all’interno. Allo stesso tempo, un sistema di “plumbing” riconosciuto di recente — il sistema glinfatico — fa fluire liquido attraverso il tessuto cerebrale, lavando via proteine di scarto che altrimenti possono accumularsi in malattie come l’Alzheimer. Questo fluido, che trasporta frammenti di detriti e potenziali segnali di allarme, lascia il cervello lungo percorsi speciali che si connettono ai centri immunitari del corpo.
Tubi di scarico nascosti e posti di osservazione
Uno dei cambiamenti più netti nel modo di pensare è venuto con la scoperta di veri vasi linfatici — canali di drenaggio — che corrono nelle robuste membrane esterne del cervello. Questi vasi raccolgono liquido, cellule immunitarie e frammenti molecolari dal tessuto cerebrale e li convogliano ai linfonodi del collo, dove le cellule del sistema immunitario pattugliano alla ricerca di problemi. Nei dintorni, ampi spazi pieni di sangue nella membrana cranica agiscono come “stazioni di frontiera” dove le cellule immunitarie campionano costantemente il materiale che arriva dal fluido cerebrale. Il cranio stesso non è solo osso: il suo midollo interno invia cellule immunitarie direttamente in queste membrane attraverso piccoli canali, creando un serbatoio locale che può rispondere rapidamente alla sofferenza cerebrale senza fare affidamento esclusivamente su cellule che viaggiano nel flusso sanguigno.
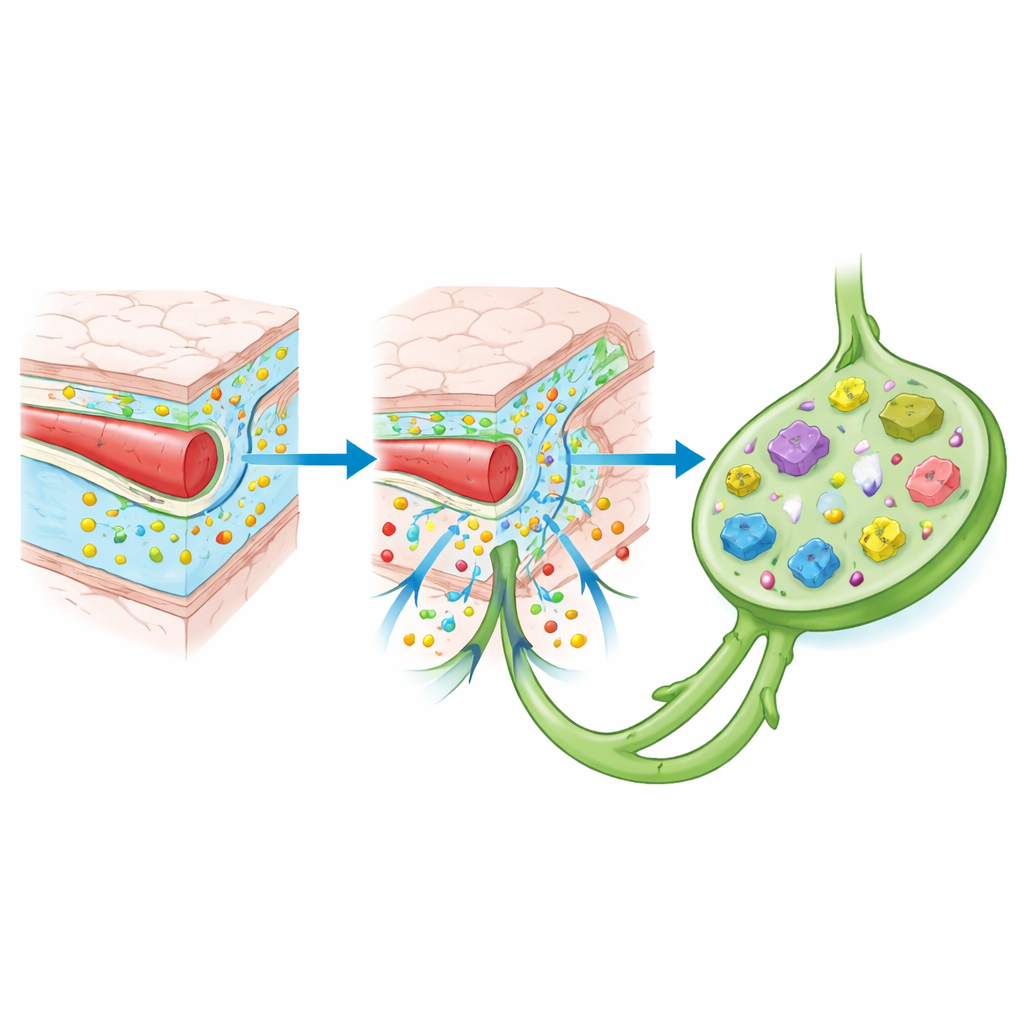
Custodi residenti e influenze a lunga distanza
All’interno del cervello, le cellule di supporto residenti fungono anche da sentinelle immunitarie. Le microglia, le cellule immunitarie proprie del cervello, estendono e ritirano continuamente i loro rami, percependo danni, infezioni o accumuli proteici. Gli astrociti, cellule di supporto a forma di stella, aiutano a mantenere la barriera emato-encefalica e rilasciano messaggeri chimici che possono sia alimentare l’infiammazione sia contribuire a risolverla. Insieme decidono se chiamare cellule immunitarie esterne e quanto potente debba essere la loro risposta. È notevole che lo stato di queste cellule sia influenzato da segnali provenienti da lontano: il microbioma intestinale, i ritmi del sonno, l’invecchiamento e l’infiammazione generale del corpo alterano tutti il “tono” dell’immunità cerebrale agendo su queste zone di confine.
Quartieri cerebrali diversi, regole diverse
Il cervello non è una sola zona immunitaria uniforme. Le membrane protettive, gli spazi pieni di liquido, il midollo spinale e la sostanza profonda del cervello seguono ciascuno regole leggermente diverse su cosa può passare e su quanto forte rispondono. Alcune regioni si riempiono di cellule immunitarie dopo una lesione, mentre altre rimangono più protette. La connessione intestino-cervello aggiunge un ulteriore livello: i microbi dell’intestino producono piccole molecole che rimodellano le cellule immunitarie nel sangue e, indirettamente, nel cervello. Squilibri in questi microbi sono stati collegati a un peggioramento dell’infiammazione in disturbi come la sclerosi multipla e il morbo di Parkinson. Questo mosaico di compartimenti e influenze esterne significa che i trattamenti futuri potrebbero dover mirare a regioni cerebrali specifiche o a percorsi di fluido, anziché fare affidamento solo su farmaci sistemici diffusi in tutto il corpo.
Malattia, terapia e un nuovo manuale operativo
Quando questo sistema finemente regolato va fuori equilibrio, i risultati possono essere drammatici. Nella sclerosi multipla, cellule immunitarie fuorviate attraversano il cervello e il midollo spinale, privando le fibre nervose della loro guaina isolante. In infezioni come la meningite o la malaria cerebrale, ondate di cellule immunitarie e molecole infiammatorie possono causare gonfiore e danno tissutale. Nell’Alzheimer e nel Parkinson, un’attività immunitaria cronica e interrotta intorno ai depositi proteici può sia aiutare a ripulire i detriti sia, se non controllata, danneggiare i neuroni. Le terapie moderne sfruttano già questa nuova comprensione: farmaci che bloccano l’ingresso delle cellule immunitarie possono rallentare la sclerosi multipla, e terapie immunitarie per i tumori cerebrali mirano a risvegliare o reindirizzare le cellule immunitarie all’interno dell’ambiente unico del cervello. La sfida è sfruttare le azioni immunitarie utili — eliminare infezioni, rimuovere proteine tossiche, uccidere cellule tumorali — senza spostare l’equilibrio verso danni duraturi.
Cosa significa questa nuova visione per tutti noi
Il messaggio centrale dell’articolo è che il cervello non è un santuario fuori limite ma una parte strettamente regolata della rete immunitaria dell’intero corpo. I percorsi di drenaggio dei fluidi, i vasi linfatici nelle membrane cerebrali e le cellule di supporto residenti insieme creano un sistema che campiona costantemente lo stato di salute del cervello e lo segnala al resto del corpo. Nella vita quotidiana questo sistema aiuta a preservare la chiarezza mentale e la stabilità delle funzioni nervose; nella malattia può proteggere o distruggere. Mappando questi punti di controllo e imparando come modulare la loro attività — tramite farmaci, stile di vita o persino cambiamenti del microbioma intestinale — i ricercatori sperano di progettare terapie che rallentino la neurodegenerazione, migliorino il recupero dopo lesioni e rendano le terapie immunitarie contro il cancro più sicure ed efficaci.
Citazione: Kobeissy, F., Salzet, M. Beyond immune privilege: the brain as a dynamic immunological interface. Cell Death Dis 17, 408 (2026). https://doi.org/10.1038/s41419-026-08561-z
Parole chiave: immunità cerebrale, barriera emato-encefalica, sistema glinfatico, vasi linfatici meningei, neuroinfiammazione