Clear Sky Science · es
Más allá del privilegio inmunitario: el cerebro como interfaz inmunológica dinámica
Por qué importa el sistema de seguridad del cerebro
Durante décadas, los manuales de biología enseñaron que el cerebro vivía tras puertas cerradas, en gran parte invisible para las defensas inmunitarias del cuerpo. Este artículo derriba esa historia simple. Explica cómo el cerebro intercambia constantemente señales, células y desechos con el resto del organismo —y cómo este tráfico oculto modela todo, desde infecciones y esclerosis múltiple hasta el Alzheimer y el cáncer cerebral. Comprender esta nueva imagen del “control fronterizo” del cerebro podría conducir a tratamientos más inteligentes que calmen la inflamación dañina a la vez que potencien la capacidad del cuerpo para proteger y reparar las neuronas.
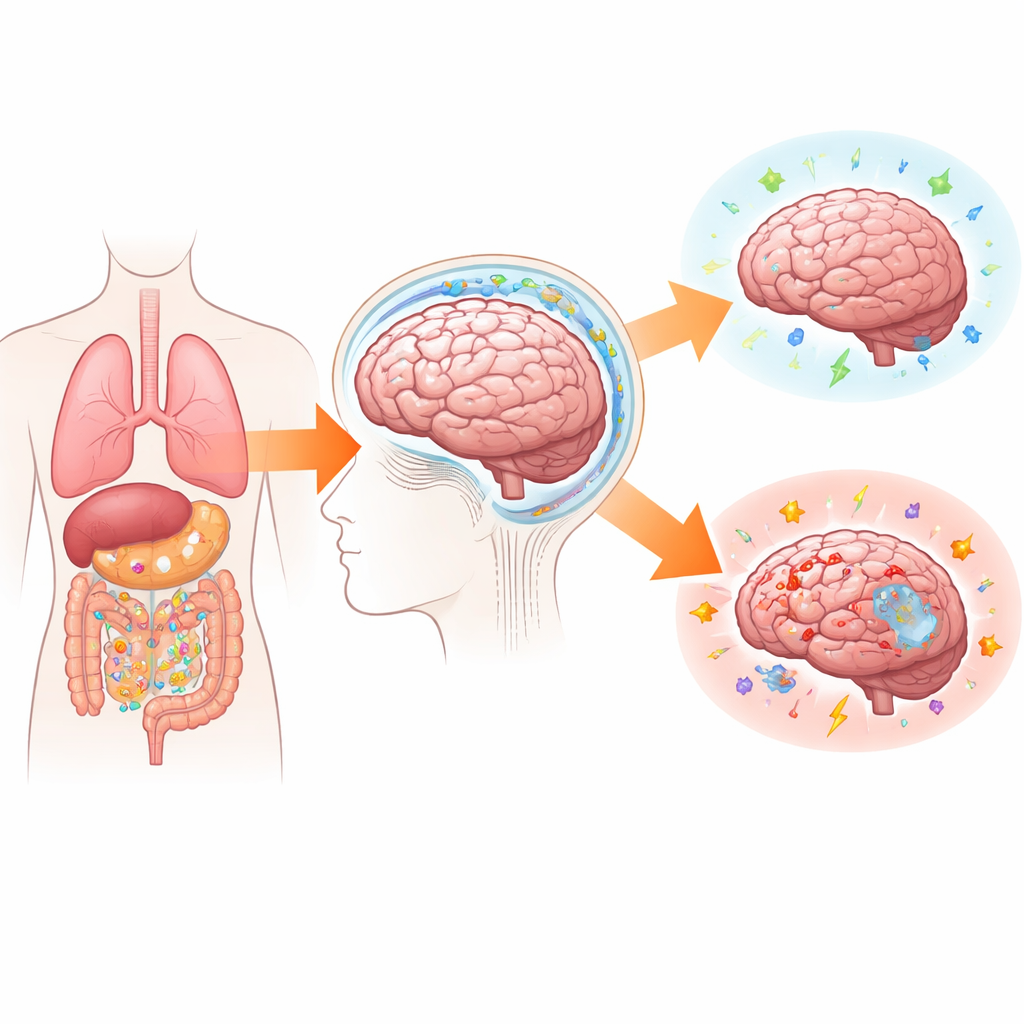
La valla del cerebro es una puerta inteligente
La barrera hematoencefálica suele compararse con un muro de fortaleza que mantiene a los invasores fuera. En realidad, se comporta más bien como un puesto fronterizo inteligente. Finas capas de células vasculares fuertemente unidas están envueltas por células de soporte que deciden qué moléculas y células inmunitarias pueden pasar. Cuando el cerebro está sano, sólo pasa un tráfico limitado. Durante una infección o lesión, esas mismas células exhiben sitios adhesivos y liberan “aromas” químicos que guían a células inmunitarias seleccionadas hacia el interior. Al mismo tiempo, un sistema de drenaje reconocido recientemente —el sistema glinfático— hace circular líquido a través del tejido cerebral, arrastrando proteínas de desecho que, de otro modo, pueden acumularse en enfermedades como el Alzheimer. Este líquido, que transporta fragmentos y posibles señales de alarma, sale del cerebro por rutas especiales que conectan con los centros inmunitarios del cuerpo.
Tuberías ocultas y puestos de vigilancia
Un cambio de paradigma de lo más llamativo vino con el descubrimiento de vasos linfáticos reales —canales de drenaje— que recorren las resistentes cubiertas externas del cerebro. Estos vasos recogen líquido, células inmunitarias y restos moleculares del tejido cerebral y los dirigen a los ganglios linfáticos del cuello, donde las células inmunitarias vigilan la presencia de problemas. Cerca, amplios espacios llenos de sangre en el revestimiento craneal actúan como “estaciones fronterizas” donde las células inmunitarias muestrean constantemente el material que llega desde el líquido cerebral. El cráneo en sí no es sólo hueso: su médula interna envía células inmunitarias directamente a estas cubiertas a través de diminutos conductos, creando un reservorio local que puede responder rápidamente al estrés cerebral sin depender únicamente de las células que viajan por la sangre.
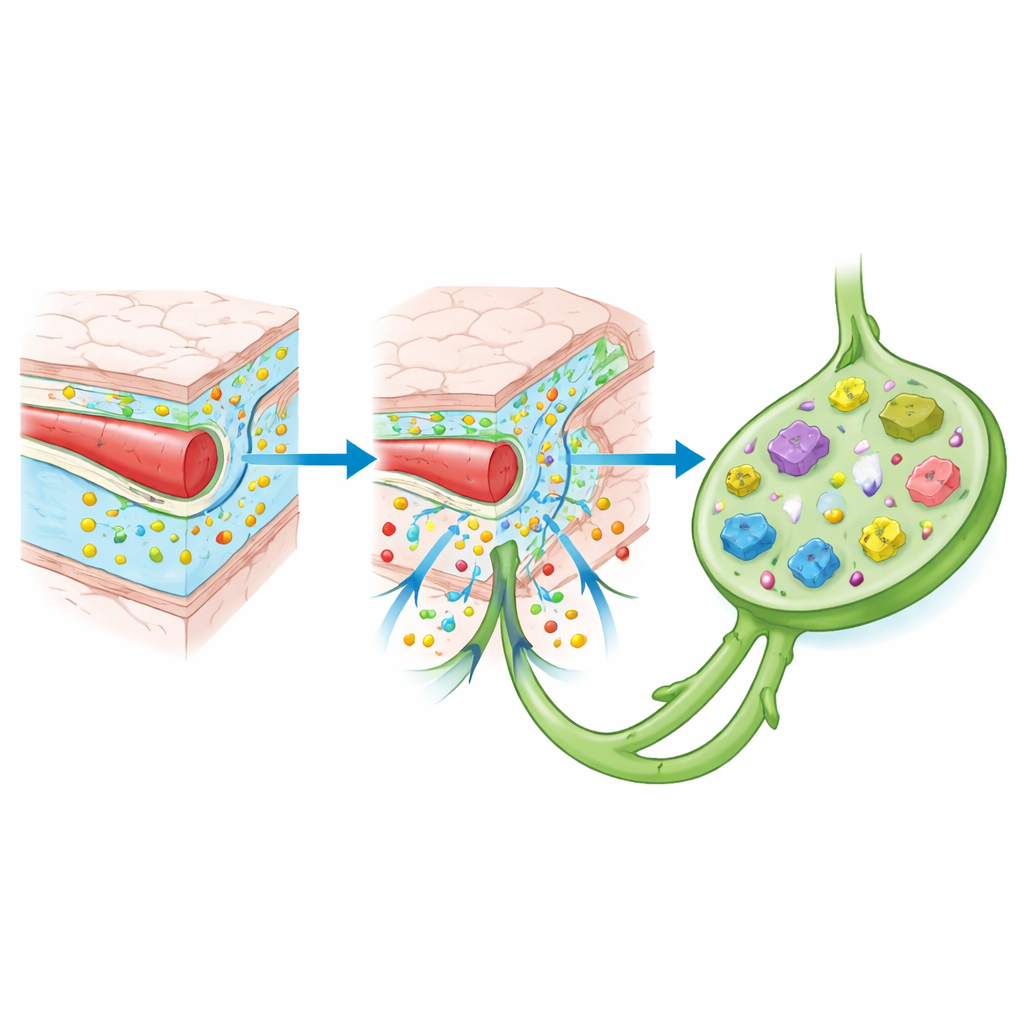
Celadores residentes e influencias a larga distancia
Dentro del cerebro, las células de soporte residentes hacen las veces de centinelas inmunitarios. Las microglías, las propias células inmunitarias del cerebro, extienden y retraen constantemente sus ramificaciones, detectando daño, infección o acumulación de proteínas. Los astrocitos, células de soporte con forma de estrella, ayudan a mantener la barrera hematoencefálica y liberan mensajeros químicos que pueden avivar la inflamación o ayudar a resolverla. Juntas, deciden si se reclutan células inmunitarias externas y cuán potente será su respuesta. De forma llamativa, el estado de estas células está influido por señales lejanas: el microbioma intestinal, los patrones de sueño, el envejecimiento y la inflamación corporal general modifican el “tono” de la inmunidad cerebral actuando en estas zonas fronterizas.
Distritos cerebrales distintos, reglas distintas
El cerebro no es una única zona inmunitaria uniforme. Las capas protectoras, los espacios llenos de líquido, la médula espinal y el tejido cerebral profundo siguen cada uno reglas ligeramente diferentes sobre qué puede pasar y con qué intensidad responden. Algunas regiones se llenan de células inmunitarias tras una lesión, mientras que otras se mantienen más resguardadas. La conexión intestino‑cerebro aporta otra capa: los microbios intestinales producen pequeñas moléculas que remodelan las células inmunitarias en la sangre y, de forma indirecta, en el cerebro. Los desequilibrios en estos microbios se han relacionado con una peor inflamación en trastornos como la esclerosis múltiple y la enfermedad de Parkinson. Este mosaico de compartimentos e influencias externas significa que las terapias futuras podrían necesitar dirigirse a regiones cerebrales o rutas de líquido específicas, en lugar de confiar sólo en fármacos de alcance general en todo el cuerpo.
Enfermedad, terapia y un nuevo manual de juego
Cuando este sistema cuidadosamente afinado falla, los resultados pueden ser dramáticos. En la esclerosis múltiple, células inmunitarias mal dirigidas cruzan al cerebro y a la médula espinal, despojando de aislamiento las fibras nerviosas. En infecciones como la meningitis o la malaria cerebral, oleadas de células inmunitarias y moléculas inflamatorias pueden causar hinchazón y daño tisular. En el Alzheimer y el Parkinson, la actividad inmunitaria crónica y latente alrededor de depósitos proteicos puede tanto ayudar a limpiar residuos como, si no se controla, dañar las neuronas. Los tratamientos modernos ya explotan este nuevo entendimiento: fármacos que bloquean la entrada de células inmunitarias pueden frenar la esclerosis múltiple, y las terapias inmunitarias para tumores cerebrales intentan despertar o redirigir células inmunitarias dentro del entorno único del cerebro. El reto es aprovechar las acciones inmunitarias útiles —eliminar infecciones, remover proteínas tóxicas, destruir células tumorales— sin inclinar la balanza hacia el daño persistente.
Qué significa esta nueva visión para todos nosotros
El mensaje central del artículo es que el cerebro no es un santuario fuera de alcance, sino una parte estrechamente regulada de la red inmunitaria del cuerpo. Las vías de drenaje de fluidos, los vasos linfáticos en las cubiertas del cerebro y las células de soporte residentes crean en conjunto un sistema que muestrea constantemente la salud cerebral y la comunica al resto del organismo. En la vida cotidiana, este sistema ayuda a preservar la claridad mental y la función neuronal estable; en la enfermedad, puede proteger o destruir. Al mapear estos puntos de control y aprender a influir en ellos —mediante fármacos, cambios en el estilo de vida o incluso alteraciones del microbioma intestinal— los investigadores esperan diseñar terapias que ralenticen la neurodegeneración, mejoren la recuperación tras lesiones y hagan que los tratamientos inmunitarios contra el cáncer sean más seguros y eficaces.
Cita: Kobeissy, F., Salzet, M. Beyond immune privilege: the brain as a dynamic immunological interface. Cell Death Dis 17, 408 (2026). https://doi.org/10.1038/s41419-026-08561-z
Palabras clave: inmunidad cerebral, barrera hematoencefálica, sistema glinfático, vasos linfáticos meníngeos, neuroinflamación