Clear Sky Science · fr
Au-delà du privilège immunitaire : le cerveau comme interface immunologique dynamique
Pourquoi le système de sécurité du cerveau compte
Pendant des décennies, les manuels de biologie présentaient le cerveau comme vivant derrière des portes verrouillées, largement invisible aux défenses immunitaires du corps. Cet article renverse ce récit simpliste. Il explique comment le cerveau échange en permanence signaux, cellules et déchets avec le reste de l’organisme — et comment ce trafic caché influence tout, des infections et de la sclérose en plaques à la maladie d’Alzheimer et aux cancers du cerveau. Comprendre cette nouvelle image du « contrôle aux frontières » du cerveau pourrait conduire à des traitements plus intelligents, capables d’apaiser l’inflammation néfaste tout en renforçant la capacité du corps à protéger et réparer les neurones.
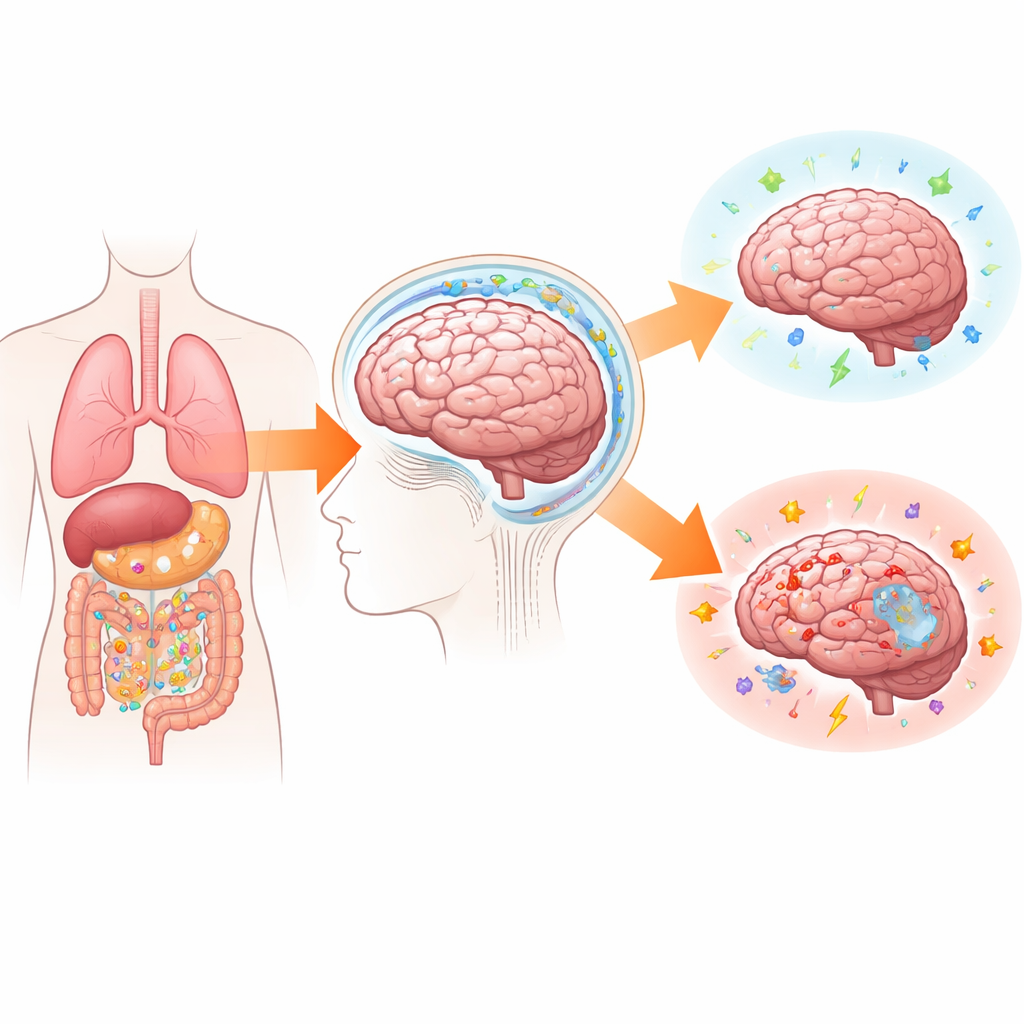
La clôture du cerveau est une porte intelligente
La barrière hémato‑encéphalique est souvent comparée à un mur de forteresse qui bloque les envahisseurs. En réalité, elle se comporte davantage comme un poste frontière intelligent. De minces couches de cellules vasculaires étroitement liées sont entourées de cellules de soutien qui décident quelles molécules et quels cellules immunitaires peuvent passer. Lorsque le cerveau est sain, seuls des échanges limités ont lieu. Lors d’une infection ou d’une lésion, ces mêmes cellules exposent des sites d’accueil adhésifs et libèrent des « parfums » chimiques qui guident des cellules immunitaires sélectionnées à l’intérieur. Parallèlement, un système de plomberie récemment reconnu — le système glymphatique — fait circuler un fluide à travers le tissu cérébral, éliminant des protéines de déchet qui, sinon, peuvent s’accumuler dans des maladies comme Alzheimer. Ce liquide, transportant débris et signaux d’alerte potentiels, quitte le cerveau par des voies spéciales qui se connectent aux carrefours immunitaires du corps.
Conduits d’évacuation cachés et postes de surveillance
Un des changements de paradigme les plus marquants a été la découverte de véritables vaisseaux lymphatiques — canaux de drainage — parcourant les enveloppes extérieures résistantes du cerveau. Ces vaisseaux collectent le liquide, les cellules immunitaires et les fragments moléculaires issus du tissu cérébral et les dirigent vers les ganglions lymphatiques du cou, où les cellules immunitaires guettent les signes de problème. À proximité, de larges espaces remplis de sang dans la muqueuse crânienne agissent comme des « postes-frontière » où les cellules immunitaires échantillonnent en permanence le matériel provenant des fluides cérébraux. Le crâne lui‑même n’est pas que de l’os : sa moelle interne envoie des cellules immunitaires directement dans ces enveloppes par de minuscules canaux, créant un réservoir local capable de réagir rapidement à la détresse cérébrale sans dépendre uniquement des cellules circulant dans le sang.
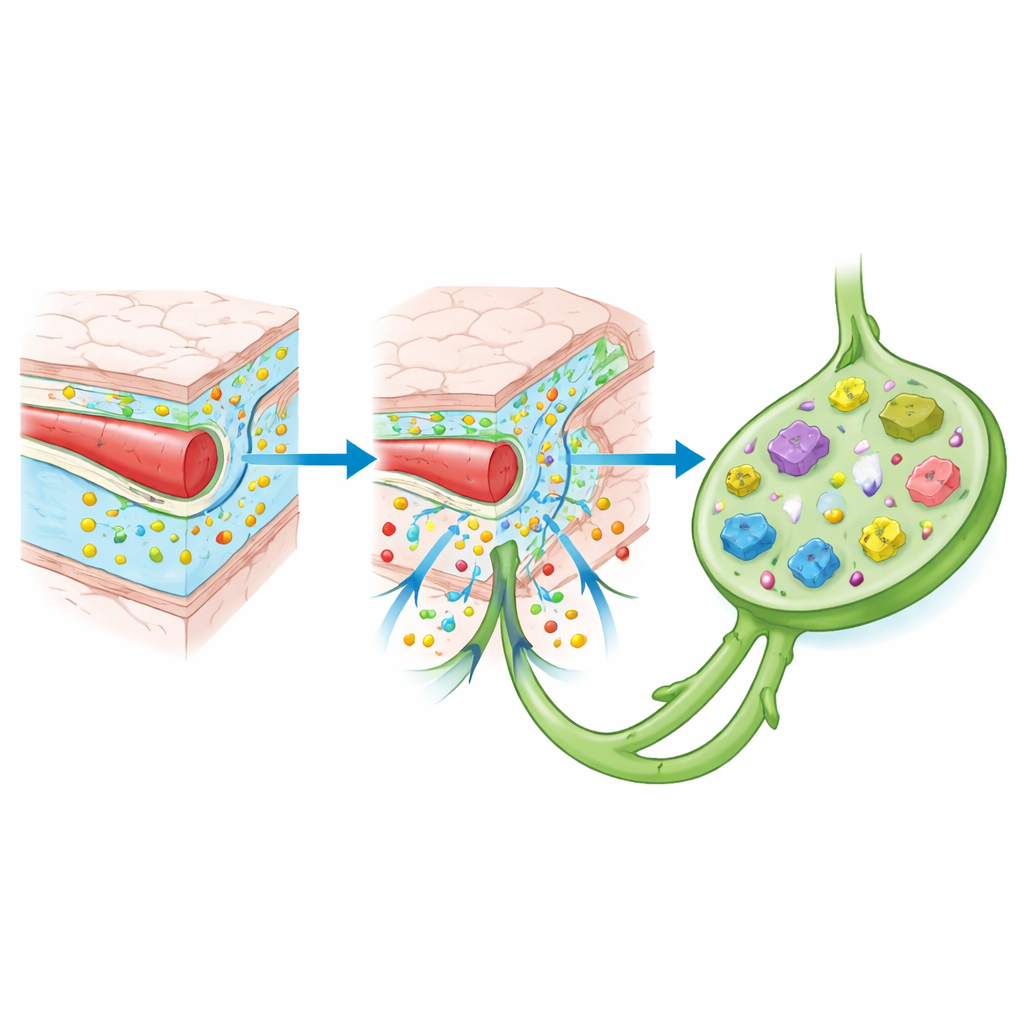
Gardiens résidents et influences à distance
À l’intérieur du cerveau, les cellules de soutien résidentes jouent aussi le rôle de sentinelles immunitaires. Les microglies, les propres cellules immunitaires du cerveau, étendent et rétractent constamment leurs prolongements, détectant dommages, infections ou accumulation de protéines. Les astrocytes, cellules de soutien en forme d’étoile, contribuent à maintenir la barrière hémato‑encéphalique et libèrent des messagers chimiques qui peuvent soit attiser l’inflammation, soit aider à la résorber. Ensemble, elles décident si des cellules immunitaires extérieures doivent être appelées et quelle sera l’intensité de la réponse. Fait remarquable, l’état de ces cellules est influencé par des signaux lointains : le microbiote intestinal, les cycles de sommeil, le vieillissement et l’inflammation corporelle générale modulent tous le « ton » de l’immunité cérébrale en agissant sur ces zones frontières.
Différents quartiers du cerveau, règles différentes
Le cerveau n’est pas une zone immunitaire uniforme. Les couches protectrices, les espaces remplis de liquide, la moelle épinière et le tissu cérébral profond suivent chacun des règles légèrement différentes quant à ce qui peut passer et à la vigueur de la réponse. Certaines régions se remplissent de cellules immunitaires après une lésion, tandis que d’autres restent plus gardées. La connexion intestin‑cerveau ajoute une couche supplémentaire : les microbes intestinaux produisent de petites molécules qui reconfigurent les cellules immunitaires dans le sang et, indirectement, dans le cerveau. Des déséquilibres de ces microbes ont été associés à une inflammation aggravée dans des troubles comme la sclérose en plaques et la maladie de Parkinson. Ce patchwork de compartiments et d’influences externes signifie que les traitements futurs devront peut‑être cibler des régions cérébrales ou des voies fluides spécifiques, plutôt que de s’appuyer uniquement sur des médicaments systémiques.
Maladie, thérapie et un nouveau mode d’emploi
Lorsque ce système finement réglé se dérègle, les conséquences peuvent être dramatiques. Dans la sclérose en plaques, des cellules immunitaires mal dirigées traversent le cerveau et la moelle épinière, dépouillant les fibres nerveuses de leur gaine isolante. Lors d’infections comme la méningite ou le paludisme cérébral, des vagues de cellules immunitaires et de molécules inflammatoires peuvent provoquer gonflement et lésions tissulaires. Dans la maladie d’Alzheimer et la maladie de Parkinson, une activité immunitaire chronique et sourde autour des dépôts protéiques peut à la fois aider à éliminer les débris et, si elle devient incontrôlée, nuire aux neurones. Les traitements modernes exploitent déjà cette nouvelle compréhension : des médicaments qui bloquent l’entrée des cellules immunitaires peuvent ralentir la sclérose en plaques, et des thérapies immunitaires contre les tumeurs cérébrales visent à réveiller ou rediriger les cellules immunitaires dans l’environnement unique du cerveau. Le défi consiste à exploiter les actions immunitaires utiles — éliminer les infections, retirer les protéines toxiques, tuer les cellules tumorales — sans faire basculer l’équilibre vers des dommages durables.
Ce que cette nouvelle vision signifie pour nous tous
Le message central de l’article est que le cerveau n’est pas un sanctuaire interdit, mais une partie étroitement régulée du réseau immunitaire global du corps. Les voies de drainage des fluides, les vaisseaux lymphatiques des enveloppes cérébrales et les cellules de soutien résidentes forment ensemble un système qui évalue constamment l’état du cerveau et en informe le reste de l’organisme. Dans la vie quotidienne, ce système aide à préserver la clarté de la pensée et la stabilité des fonctions nerveuses ; en cas de maladie, il peut protéger ou détruire. En cartographiant ces points de contrôle et en apprenant à les infléchir — par des médicaments, des changements de mode de vie ou même des modifications du microbiote intestinal — les chercheurs espèrent concevoir des thérapies qui ralentissent la neurodégénérescence, améliorent la récupération après une lésion et rendent les traitements immunothérapeutiques contre le cancer plus sûrs et plus efficaces.
Citation: Kobeissy, F., Salzet, M. Beyond immune privilege: the brain as a dynamic immunological interface. Cell Death Dis 17, 408 (2026). https://doi.org/10.1038/s41419-026-08561-z
Mots-clés: immunité cérébrale, barrière hémato‑encéphalique, système glymphatique, vaisseaux lymphatiques méningés, neuroinflammation