Clear Sky Science · it
La classificazione basata sulle firme mutazionali svela nuovi sottotipi di tumore orale con pattern molecolari distinti
Perché questa nuova visione del cancro orale è importante
I tumori orali, in particolare quelli che insorgono nella parte mobile della lingua, vengono diagnosticati sempre più spesso in persone che non fumano, non bevono molto e non sono positive per il papillomavirus umano (HPV). Questo mette in crisi la narrazione consolidata secondo cui tabacco, alcool e HPV sono i principali responsabili. Lo studio riassunto qui esplora il DNA di questi tumori per individuare pattern nascosti di danno e riparazione, rivelando che sta emergendo una forma di cancro orale finora sottovalutata, con una biologia propria e probabilmente esigenze specifiche di prevenzione e cura.
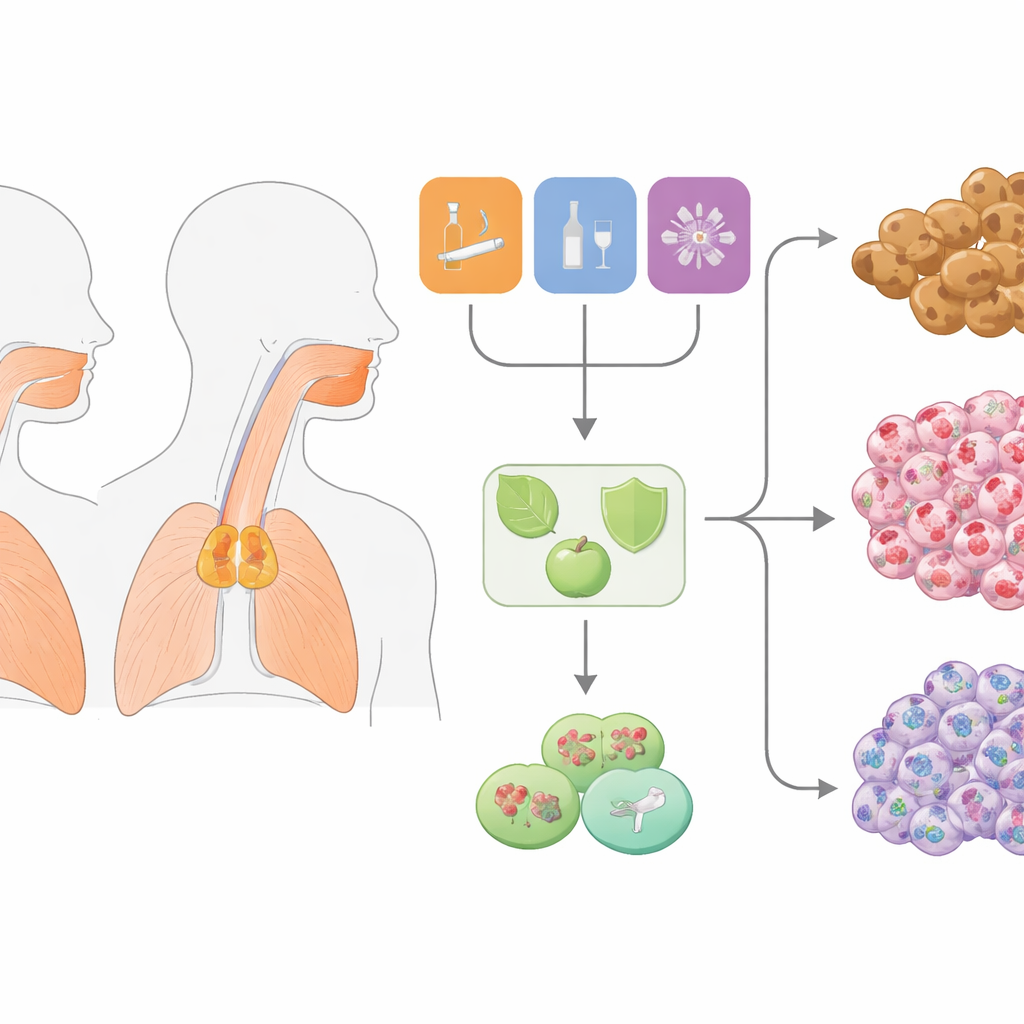
Esaminare il DNA del cancro per indizi nascosti
Ogni cellula tumorale porta con sé la storia degli agenti che hanno danneggiato il suo DNA nel tempo. Cause diverse lasciano “impronte” differenti nel genoma. I ricercatori hanno analizzato il DNA di 347 tumori della testa e del collo, principalmente della cavità orale e della laringe, utilizzando dataset pubblici di The Cancer Genome Atlas. Invece di partire dai fattori di rischio noti, hanno lasciato che fosse il DNA a parlare. Esaminando migliaia di mutazioni per tumore, hanno estratto pattern ricorrenti, o “firme mutazionali”, che riflettono se il danno è derivato dal fumo di sigaretta, dall’alcool, da cambiamenti chimici interni o da particolari enzimi che modificano il DNA. Questo approccio non supervisionato ha raggruppato i tumori in quattro cluster principali, ognuno dominato da un particolare tipo di processo mutazionale.
Quattro gruppi basati sul DNA, solo alcuni collegati a tabacco e alcool
Due cluster si sono chiaramente allineati con i fattori di rischio tradizionali. Un gruppo arricchito per laringe mostrava firme nette associate al fumo, con numeri di mutazioni molto elevati. Un altro cluster, presente soprattutto nei tumori della cavità orale di fumatori e bevitori, evidenziava un pattern che in precedenza era stato attribuito all’alcool, ma qui appare più convincente come risultato degli effetti combinati di tabacco e alcool e di specifiche sedi della bocca, come il pavimento orale. È significativo che la maggior parte dei tumori laringei rientrasse nel gruppo dominato dal tabacco, mentre i tumori della cavità orale erano distribuiti tra tutti e quattro i cluster. Questo dimostra che anche quando le persone sono esposte agli stessi agenti esterni, parti diverse di testa e collo rispondono con processi mutazionali e livelli di danno complessivi distinti.
Una nuova classe di tumori orali senza i fattori di rischio classici
Gli altri due cluster erano arricchiti in pazienti senza fattori di rischio identificati (NIRF): non fumatori, non bevitori e HPV-negativi. Molti di questi tumori sono insorti sulla lingua mobile, anche in adulti più giovani e in donne. Il loro DNA non mostrava evidenti cicatrici riconducibili a tabacco o alcool. Invece, un gruppo NIRF presentava alti livelli di un lento processo mutazionale “a orologio” che si accumula naturalmente nel tempo man mano che le cellule si dividono e le basi metilate del DNA subiscono cambiamenti spontanei. Il secondo gruppo NIRF mostrava lo stesso pattern a orologio più uno strato aggiuntivo di intensa mutagenesi guidata dagli enzimi APOBEC — proteine cellulari che normalmente aiutano a difendersi da virus e altre minacce ma che possono anche “mancare il bersaglio” e danneggiare il DNA della cellula stessa.
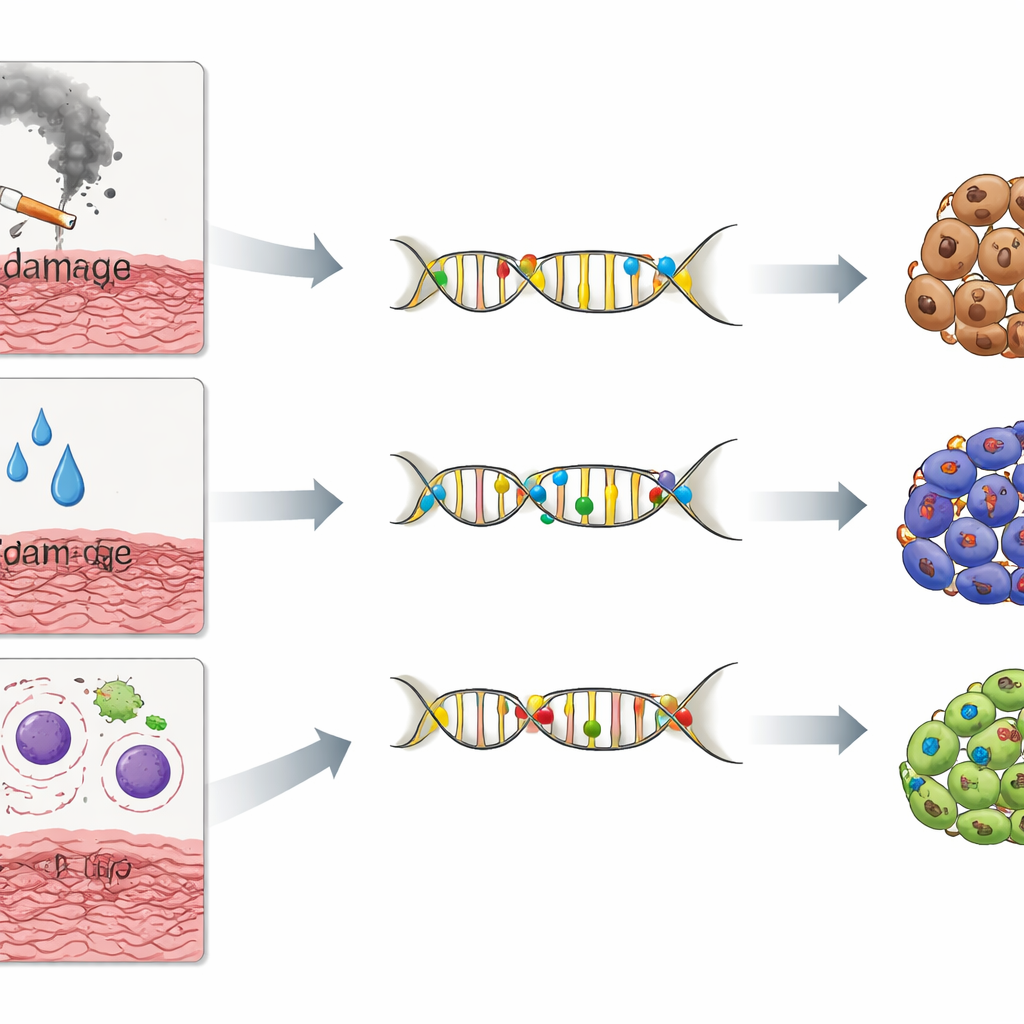
Fuga dal sistema immunitario, microbi e comportamento tissutale alterato
Oltre alle mutazioni, questi tumori NIRF presentavano cambiamenti distintivi in geni driver del cancro e nel modo in cui i geni venivano attivati o disattivati. Geni coinvolti nella presentazione di frammenti tumorali al sistema immunitario e nell’innesco della morte cellulare erano frequentemente alterati, suggerendo sofisticate strategie di elusione immunitaria. I pattern di metilazione del DNA in questi cluster somigliavano a quelli dei non fumatori, rafforzando l’idea che il tabacco non fosse il principale fattore. Allo stesso tempo, l’attività genica legata alla differenziazione di tipo epidermico e alla produzione di cheratina era aumentata, e le vie associate alla difesa antimicrobica e alle risposte a componenti batterici, inclusa la lipopolisaccaride, risultavano fortemente attivate. Quando i ricercatori hanno esaminato al microscopio due tumori della lingua, hanno osservato alti livelli di proteine cheratiniche, marcatori antimicrobici e segnali che indicano la presenza di materiale batterico nelle regioni tumorali, a sostegno di un legame tra cambiamenti tissutali, microbi e risposte immunitarie locali.
Cosa significa per i pazienti e per le cure future
In termini chiari, questo lavoro mostra che un numero crescente di tumori orali insorge senza fumo, consumo eccessivo di alcool o HPV, ed è invece modellato da processi di danno al DNA endogeni e da come l’epitelio orale e il sistema immunitario rispondono a sfide microbiche. Questi tumori NIRF costituiscono un’entità molecolarmente distinta con pattern unici di fuga immunitaria, danno al DNA e comportamento tissutale. Riconoscerli come gruppo separato è importante: potrebbero rispondere meno bene alle terapie immunitarie attuali che dipendono da una presentazione antigenica intatta, ma potrebbero essere vulnerabili a farmaci che prendono di mira lo stress di replicazione o specifici cambiamenti epigenetici. I risultati sottolineano anche la necessità di individuare trigger ambientali o biologici oltre tabacco e alcool — come irritazioni croniche, alterazioni del microbioma o sottili alterazioni immunitarie — per migliorare la prevenzione, la diagnosi e il trattamento di questa forma emergente di cancro orale.
Citazione: Deneuve, S., Fervers, B., Bruno, J.S. et al. Mutational signature-based classification uncovers emerging oral cancer subtypes with distinct molecular patterns. Int J Oral Sci 18, 38 (2026). https://doi.org/10.1038/s41368-026-00437-4
Parole chiave: carcinoma della lingua orale, firme mutazionali, tumore in non fumatori non bevitori, carcinoma squamocellulare testa-collo, microbioma tumorale