Clear Sky Science · fr
Une classification basée sur les signatures mutationnelles révèle de nouveaux sous-types de cancers buccaux aux motifs moléculaires distincts
Pourquoi cette nouvelle vision du cancer buccal est importante
Les cancers buccaux, en particulier ceux qui apparaissent sur la partie mobile de la langue, sont de plus en plus diagnostiqués chez des personnes qui ne fument pas, ne consomment pas d’alcool en excès et ne sont pas porteuses du papillomavirus humain (HPV). Cela remet en question le récit classique selon lequel le tabac, l’alcool et le HPV sont les principaux coupables. L’étude résumée ici analyse l’ADN de ces tumeurs pour déceler des schémas cachés de dommages et de réparation, révélant l’émergence d’une forme de cancer buccal jusqu’alors sous-estimée, avec sa propre biologie et, probablement, ses propres besoins en matière de prévention et de traitement.
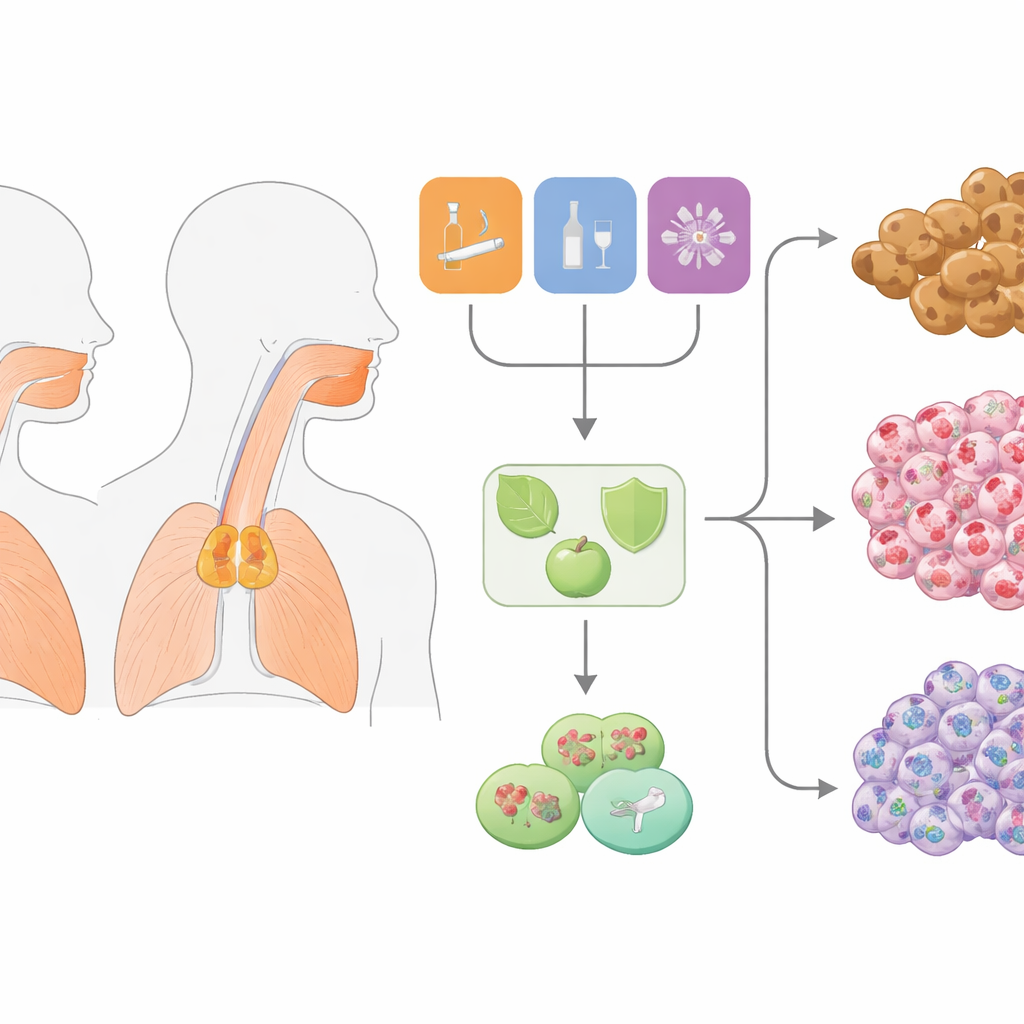
Explorer l’ADN du cancer à la recherche d’indices cachés
Chaque cellule cancéreuse porte l’histoire des agressions qu’a subies son ADN au fil du temps. Diffentes causes laissent différentes « empreintes » dans le génome. Les chercheurs ont analysé l’ADN de 347 tumeurs de la tête et du cou, principalement de la cavité buccale et du larynx, en utilisant des jeux de données publics du Cancer Genome Atlas. Plutôt que de partir des facteurs de risque connus, ils ont laissé l’ADN parler. En examinant des milliers de mutations par tumeur, ils ont extrait des motifs récurrents, ou « signatures mutationnelles », qui reflètent si les dommages proviennent de la fumée du tabac, de l’alcool, de changements chimiques internes ou d’enzymes éditrices d’ADN particulières. Cette approche non supervisée a regroupé les tumeurs en quatre grands clusters, chacun dominé par un type particulier de processus mutationnel.
Quatre groupes basés sur l’ADN, seulement certains liés au tabac et à l’alcool
Deux clusters s’alignent clairement sur les facteurs de risque traditionnels. Un groupe enrichi en tumeurs du larynx portait des signatures fortes liées à la fumée de tabac, avec des nombres de mutations très élevés. Un autre cluster, trouvé principalement dans des tumeurs de la cavité buccale chez des fumeurs et buveurs, montrait un motif auparavant attribué à l’alcool, mais ici plus vraisemblablement lié aux effets combinés du tabac et de l’alcool et à des sous-sites buccaux spécifiques comme le plancher de la bouche. Fait marquant, la plupart des cancers du larynx appartenaient au groupe dominé par le tabac, tandis que les cancers de la cavité buccale étaient répartis sur les quatre clusters. Cela montre que, même lorsque des personnes sont exposées aux mêmes agents externes, différentes parties de la tête et du cou réagissent par des processus mutationnels et des niveaux de dommages distincts.
Une nouvelle classe de cancers buccaux sans facteurs de risque classiques
Les deux autres clusters étaient enrichis en patients sans facteurs de risque identifiés (NIRF) : non-fumeurs, non-buveurs et HPV-négatifs. Beaucoup de ces tumeurs sont apparues sur la langue mobile, y compris chez de jeunes adultes et des femmes. Leur ADN ne présentait pas de traces marquées liées au tabac ou à l’alcool. À la place, un groupe NIRF montrait des niveaux élevés d’un processus de mutation lent, dit « en horloge », qui s’accumule naturellement avec le temps à mesure que les cellules se divisent et que des bases d’ADN méthylées se modifient spontanément. Le second groupe NIRF présentait ce même motif en horloge plus une couche supplémentaire d’intense mutagenèse conduite par les enzymes APOBEC — des protéines cellulaires qui aident normalement à lutter contre les virus et autres menaces mais qui peuvent aussi mal agir et endommager l’ADN de la cellule elle-même.
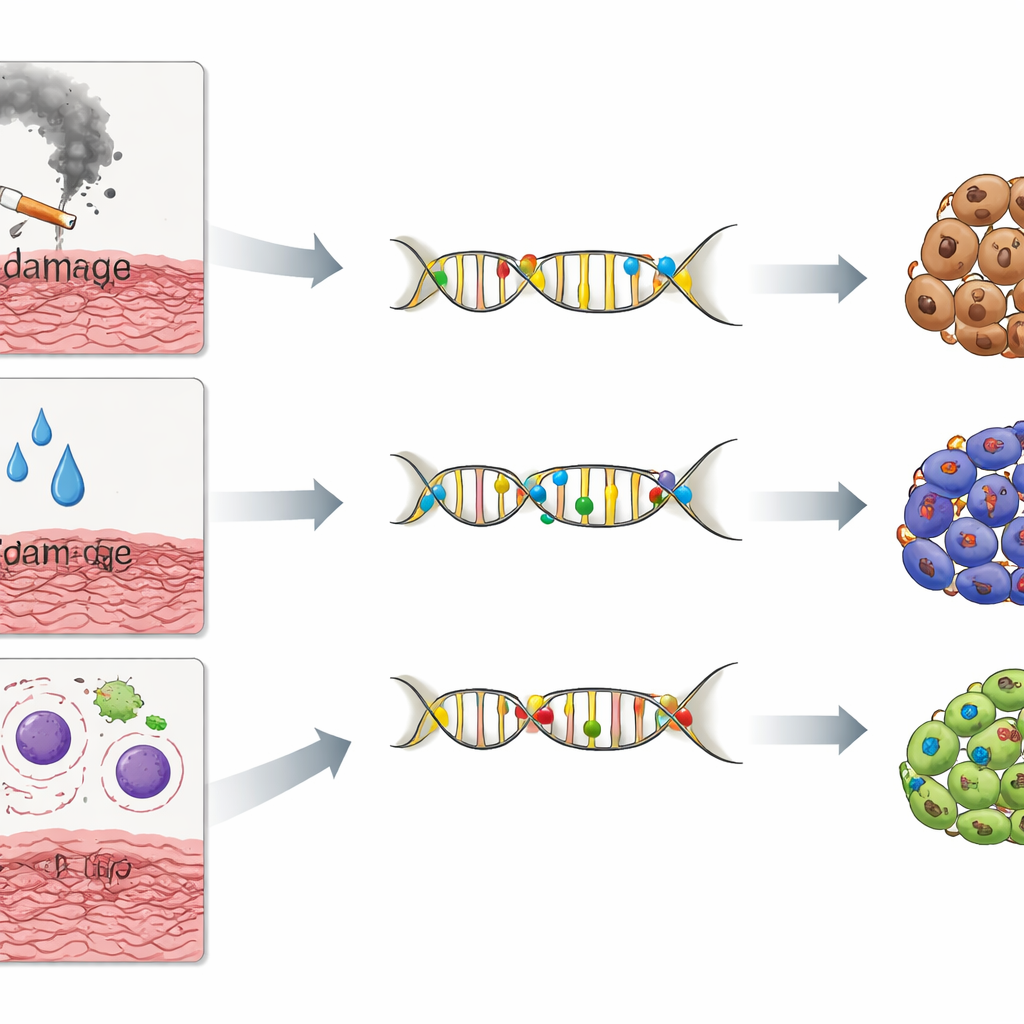
Évasion immunitaire, microbes et comportement tissulaire altéré
Au-delà des mutations, ces tumeurs NIRF présentaient des altérations distinctives des gènes suppresseurs et des oncogènes, ainsi que des changements dans la façon dont les gènes sont activés ou désactivés. Des gènes impliqués dans la présentation d’antigènes tumoraux au système immunitaire et dans le déclenchement de la mort cellulaire étaient fréquemment altérés, ce qui indique des mécanismes sophistiqués d’évasion immunitaire. Les schémas de méthylation de l’ADN dans ces clusters ressemblaient à ceux de non-fumeurs, renforçant l’idée que le tabac n’était pas le principal moteur. Parallèlement, l’activité génique liée à une différenciation de type cutané et à la production de kératine était renforcée, et des voies associées à la défense antimicrobienne et aux réponses aux composants bactériens, y compris le lipopolysaccharide, étaient fortement activées. Lorsque les chercheurs ont examiné deux tumeurs de la langue au microscope, ils ont observé des niveaux élevés de protéines kératiniques, de marqueurs antimicrobiens et des signaux suggérant la présence de matière bactérienne dans les régions tumorales, soutenant un lien entre les changements tissulaires, les microbes et les réponses immunitaires locales.
Ce que cela signifie pour les patients et les soins futurs
Concrètement, ce travail montre qu’un nombre croissant de cancers buccaux survient sans tabagisme, consommation excessive d’alcool ou HPV, et est plutôt façonné par des processus internes de dommage de l’ADN et par la façon dont la muqueuse buccale et le système immunitaire réagissent aux défis microbiens. Ces tumeurs NIRF forment une entité moléculairement distincte avec des schémas uniques d’évasion immunitaire, de dommages à l’ADN et de comportement tissulaire. Les reconnaître comme un groupe à part est important : elles pourraient ne pas répondre aussi bien aux thérapies immunitaires actuelles qui reposent sur une présentation d’antigènes intacte, mais pourraient être sensibles à des médicaments ciblant le stress de réplication ou des altérations épigénétiques spécifiques. Les résultats soulignent aussi la nécessité d’identifier des déclencheurs environnementaux ou biologiques au-delà du tabac et de l’alcool — tels que l’irritation chronique, des variations du microbiome ou des perturbations immunitaires subtiles — afin de mieux prévenir, détecter et traiter cette forme émergente de cancer buccal.
Citation: Deneuve, S., Fervers, B., Bruno, J.S. et al. Mutational signature-based classification uncovers emerging oral cancer subtypes with distinct molecular patterns. Int J Oral Sci 18, 38 (2026). https://doi.org/10.1038/s41368-026-00437-4
Mots-clés: cancer de la langue orale, signatures mutationnelles, cancer chez non-fumeurs non-buveurs, carcinome épidermoïde de la tête et du cou, microbiome tumoral