Clear Sky Science · he
נתיב Nrf2/SLC7A11/GPX4, מטרה פוטנציאלית של אורידונין בעיכוב פרופרוטוזה במהלך התקדמות פציעת איסכמיה-רפרפוזיה מוחית
מדוע שבץ יכול לפגוע פעמיים
כשאדם חווה שבץ איסכמי, קריש חוסם את זרימת הדם לחלק מהמוח. הרופאים ממהרים לפתוח את הכלי, אך עצם שיחזור הזרימה עלול לגרום גל נזק משלו — תופעה הנקראת פציעת רפרפוזיה. המחקר בודק האם אורידונין, תרכובת טבעית ממערכת צמחים בתרופה הסינית המסורתית, יכול להגן על תאי המוח מהמיתון השני הזה של נזק על ידי הרגעת צורת מוות תאית הרסנית המונעת על ידי ברזל.
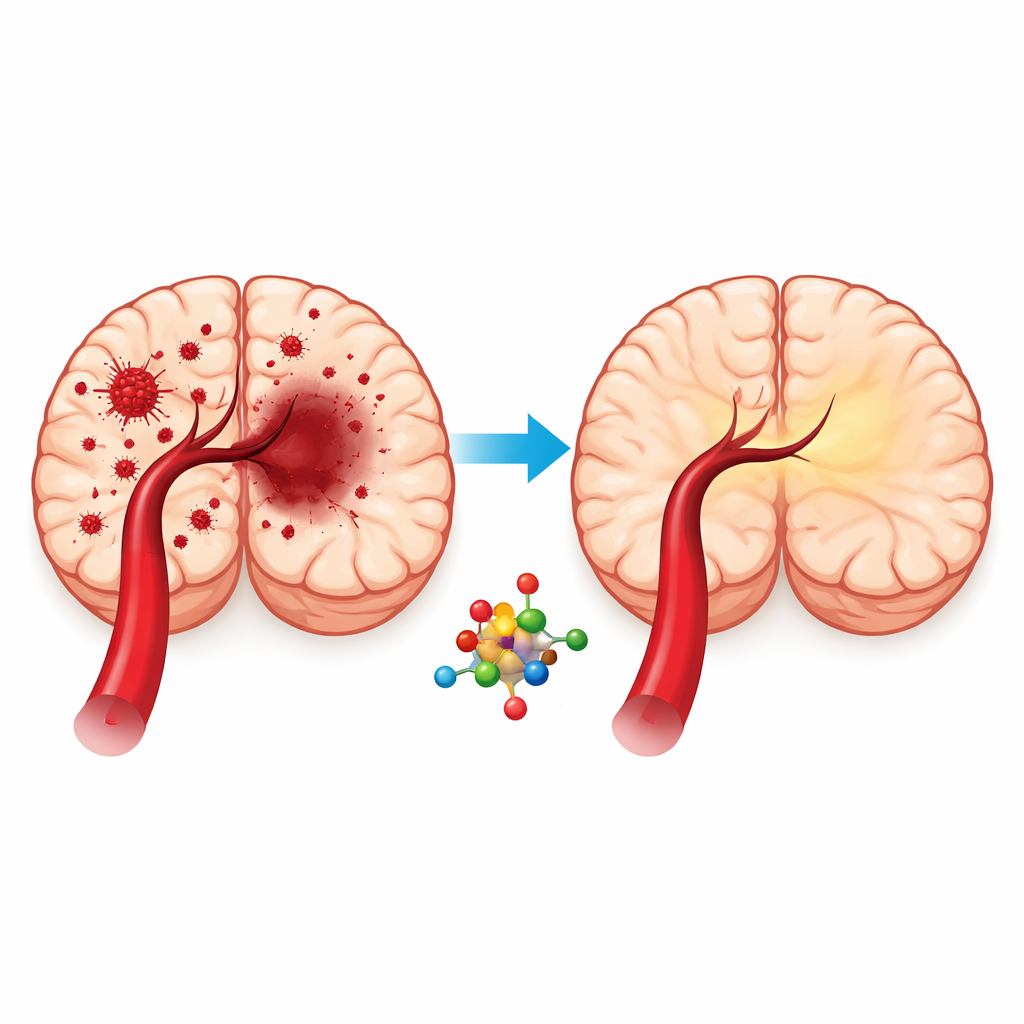
תרכובת צמחית תחת המיקרוסקופ
אורידונין מוּצא מהצמח Rabdosia rubescens, המשמש זמן רב ברפואה הסינית המסורתית וכבר ידוע בתכונותיו הנוגדות דלקת ונוגדות החמצון. החוקרים חשדו כי הוא עשוי גם להגן על המוח בתוך חלון הקריטי לאחר שבץ. כדי לבדוק זאת השתמשו בשני מודלים משלימים: חולדות שעברו חסימה קצרה בעורק מרכזי במוח ואחריה שיחזור זרימת דם, ותאי-עצם מדומים בתרבית שנחשפו לתקופה ללא חמצן וסוכר ואחריה החזרה של חמצן. יחד המערכות הללו מדמות את מה שקורה לרקמת המוח כאשר קריש גורם למחסור דם ואז פתאום מתבצע שיחזור זרימה קליני.
כשברזל וחמצונים הופכים קטלניים
הקבוצה התמקדה בפרופרוטוזה, סוג מוות תאי שהוכר לאחרונה ומוזן על ידי הצטברות ברזל וחמצון בלתי נשלט של שומנים בממברנות התאים. בחולדות, תקופות ארוכות יותר של שיחזור זרימה הובילו לציוני נוירולוגיה גרועים יותר, לאזורי שבץ גדולים יותר ולנוירונים מתים ומופרעים יותר. רקמת המוח הצטברה בברזל וסימנים כימיים לנזק חמצוני, בעוד המיטוכונדריה — אברוני האנרגיה של התא — נעשו מעוותים ומלאי חללים. במקביל נחלש בהדרגה מסלול איתות מגן מרכזי, הכולל את החלבונים Nrf2, SLC7A11 ו‑GPX4. מסלול זה בדרך כלל מסייע לשמור על ברזל וחמצונים תחת שליטה; כשפעילותו ירדה, סמני פרופרוטוזה עלו, מה שמעיד כי הפרופרוטוזה הוטלה בכוח לאחר הרפרפוזיה.
כיצד אורידונין משנה את התמונה
מתן אורידונין לפני חסימת העורק שינה תוצאות אלה במינון תלוי. בעלי החיים שקיבלו מינונים גבוהים יותר נהנו משיחזור זרימה טוב יותר, מאזורי שבץ קטנים יותר ומהתנהגות נוירולוגית קצרת-טווח משופרת. הנוירונים שלהם שמרו על מבנה נורמלי יותר והיו פחות משקעים של ברזל, והאותות הביוכימיים של פרופרוטוזה — מולקולות חמצון תגובתיות, עודף ברזל ותוצרי פירוק שומניים — פחתו. הן במוח החולדות והן בתאים בתרבית, אורידונין הגדיל את רמות Nrf2, SLC7A11 ו‑GPX4 תוך דיכוי חלבונים המקדמים פרופרוטוזה. המיטוכונדריות נראו בריאות ושלמות יותר במיקרוסקופ אלקטרונים, מה שמרמז כי התרכובת סייעה לשמר את מכונת התאים המרכזית במצבי הלחץ של הרפרפוזיה.
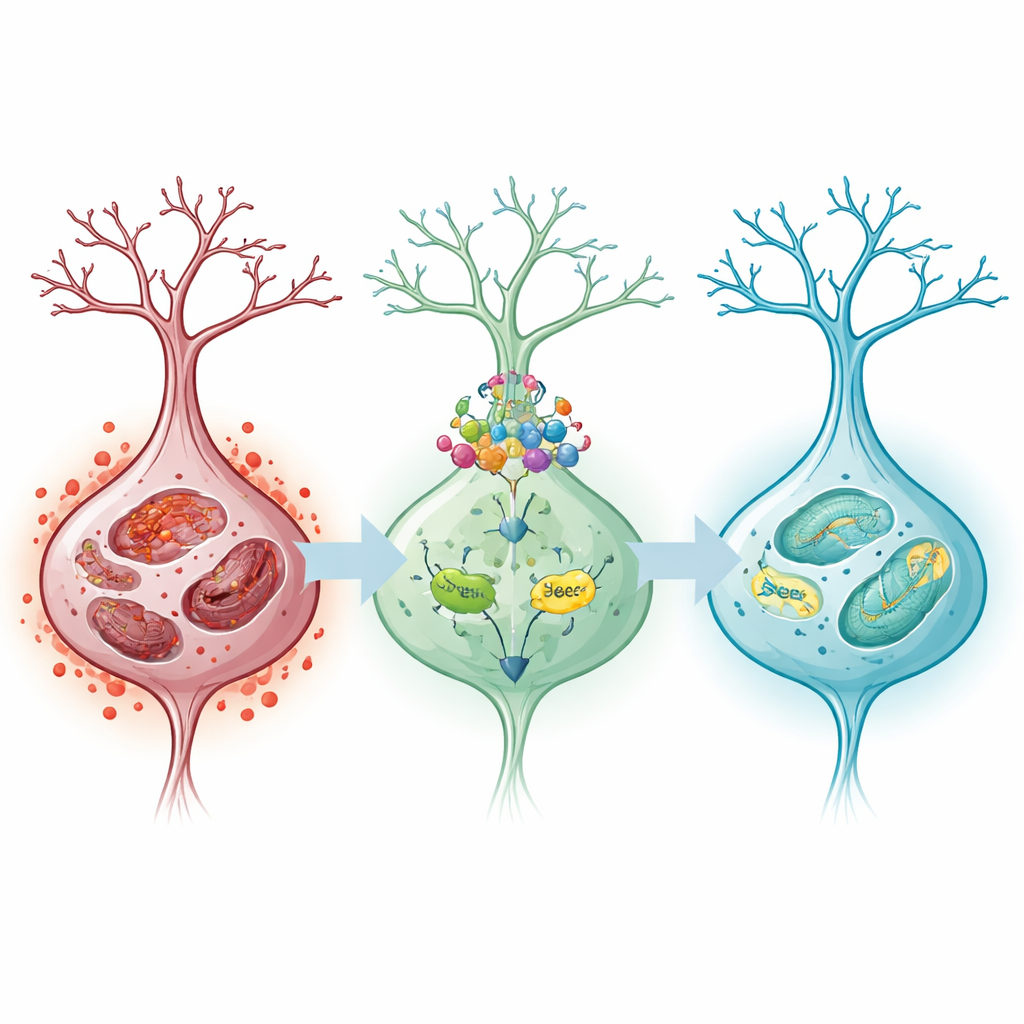
בחינת מתג ההגנה של התא
כדי לבדוק האם מסלול ההגנה הזה אכן מרכזי לפעולת האורידונין, החוקרים הפחיתו באופן בררני את Nrf2 בתאי-העצם המדומים. כאשר Nrf2 דוכא, אורידונין כבר לא יכול היה להשיב במלואו את האיזון בין ברזל לנוגדי החמצון: מולקולות מזיקות ורמות ברזל עלו שוב, הישרדות התאים ירדה ומות התאים גדל. ההיפוך הזה מצביע על כך שהיתרונות של אורידונין תלוים במידה רבה ביכולתו של Nrf2 להפעיל הגנות יורשות, כולל SLC7A11 ו‑GPX4, אשר יחד מסייעות לשמור על גלוטתיון — נוגד חמצון תאי קריטי — ולמנוע חמצון של שומני ממברנה.
מה משמעות הדבר לטיפול בשבץ בעתיד
לקרב־אדם, המסר המרכזי הוא שעבודה זו מזהה מולקולה טבעית המסייעת לתאי המוח לעמוד בסערה הכימית האלימה שמתרחשת לאחר שיחזור זרימת הדם אחרי שבץ. על ידי חיזוק מעגל הגנה פנימי ששולט בטיפול בברזל ובמאגרים נוגדי החמצון, אורידונין מקטין סוג ספציפי של מוות תאי התלוי בברזל ומגביל נזק מוחי מוקדם במודלים של בעלי חיים ותאים. המחקר עדיין לא מוכיח שאורידונין בטוח או יעיל באדם, ולא בוחן התאוששות לטווח ארוך, אך הוא מציע מתווה מבטיח: מיקוד במסלול Nrf2–SLC7A11–GPX4 לדיכוי פרופרוטוזה עשוי יום אחד להשלים טיפולים לפיצוץ או הסרה של קרישים, ולהפוך את שיחזור הזרימה שהציל חיים להצלה בטוחה יותר במקום חרב פיפיות.
ציטוט: Zhang, D., Shao, L., He, M. et al. Nrf2/SLC7A11/GPX4 pathway, a potential target of oridonin in inhibiting ferroptosis during cerebral ischemia-reperfusion injury progression. Sci Rep 16, 14597 (2026). https://doi.org/10.1038/s41598-026-38658-6
מילות מפתח: שבץ איסכמי, פציעת רפרפוזיה, פרופרוטוזה, אורידונין, הגנה עצבית