Clear Sky Science · es
Vía Nrf2/SLC7A11/GPX4, un posible objetivo del oridonin para inhibir la ferroptosis durante la progresión de la lesión por isquemia-reperfusión cerebral
Por qué un ictus puede hacer daño dos veces
Cuando una persona sufre un ictus isquémico, un coágulo bloquea el flujo sanguíneo hacia una parte del cerebro. Los médicos se apresuran a reabrir el vaso, pero el propio acto de restablecer la circulación puede provocar una nueva oleada de daño, un fenómeno denominado lesión por reperfusión. Este estudio explora si el oridonin, un compuesto natural procedente de una hierba medicinal china tradicional, puede proteger las células cerebrales de ese segundo golpe de daño al calmar una forma destructiva de muerte celular impulsada por el hierro.
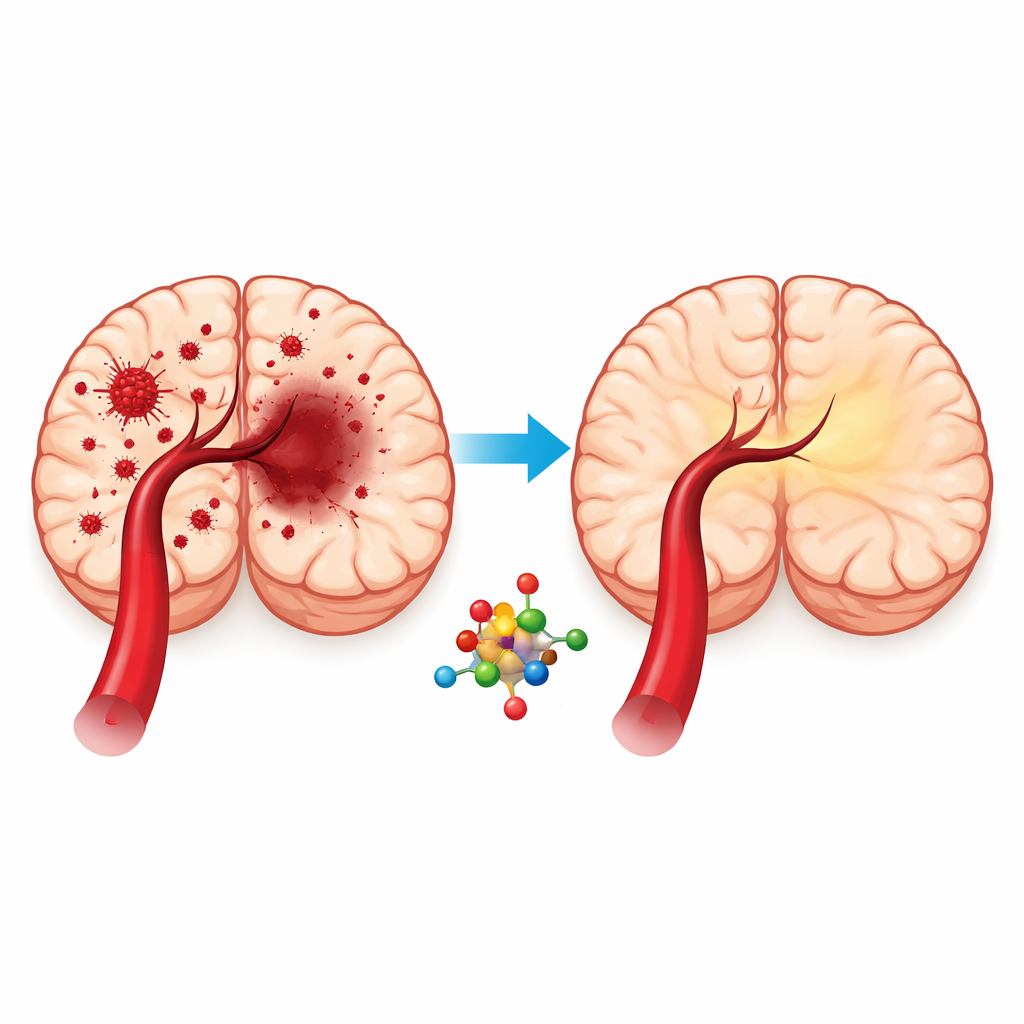
Un compuesto vegetal bajo el microscopio
El oridonin se extrae de la planta Rabdosia rubescens, empleada desde hace tiempo en la medicina tradicional china y ya conocida por sus efectos antiinflamatorios y antioxidantes. Los investigadores sospecharon que también podría proteger el cerebro durante la ventana crítica tras un ictus. Para poner a prueba esta idea emplearon dos modelos complementarios: ratas sometidas a una breve oclusión de una arteria cerebral importante seguida de la restauración del flujo sanguíneo, y células de tipo nervioso en cultivo expuestas a un periodo sin oxígeno ni glucosa seguido de reoxigenación. En conjunto, estos sistemas imitan lo que ocurre en el tejido cerebral cuando un coágulo deja una zona sin sangre y luego se reperfunde de forma repentina en la clínica.
Cuando el hierro y los oxidantes se vuelven letales
El equipo se centró en la ferroptosis, un tipo de muerte celular reconocido recientemente y alimentado por la acumulación de hierro y la oxidación descontrolada de los lípidos en las membranas celulares. En las ratas, periodos más largos de reperfusión se asociaron con peores puntuaciones neurológicas, infartos cerebrales mayores y neuronas más desorganizadas y en proceso de muerte. El tejido cerebral acumuló hierro y marcadores químicos de daño oxidativo, mientras que las mitocondrias —los orgánulos energéticos de la célula— se volvieron distorsionadas y vacuolizadas. Al mismo tiempo, una vía protectora clave, que involucra las proteínas Nrf2, SLC7A11 y GPX4, se debilitó de forma sostenida. Esta vía normalmente ayuda a las células a controlar el hierro y los oxidantes; cuando su actividad cayó, aumentaron los marcadores pro‑ferroptosis, indicando que la ferroptosis participó de forma destacada tras la reperfusión.
Cómo cambia el panorama el oridonin
El tratamiento previo de las ratas con oridonin antes de la oclusión arterial modificó estos resultados de forma dependiente de la dosis. Los animales que recibieron dosis más altas tuvieron una mejor restauración del flujo sanguíneo, áreas de ictus más pequeñas y un comportamiento neurológico a corto plazo mejorado. Sus neuronas conservaron una estructura más normal y presentaron menos depósitos de hierro, y las señales bioquímicas de la ferroptosis —moléculas reactivas de oxígeno, sobrecarga de hierro y productos de degradación lipídica— se redujeron. Tanto en cerebros de rata como en células en cultivo, el oridonin aumentó los niveles de Nrf2, SLC7A11 y GPX4 mientras atenuaba proteínas que promueven la ferroptosis. Bajo el microscopio electrónico, las mitocondrias parecían más sanas e intactas, lo que sugiere que el compuesto ayudó a preservar la maquinaria celular central durante el estrés de la reperfusión.
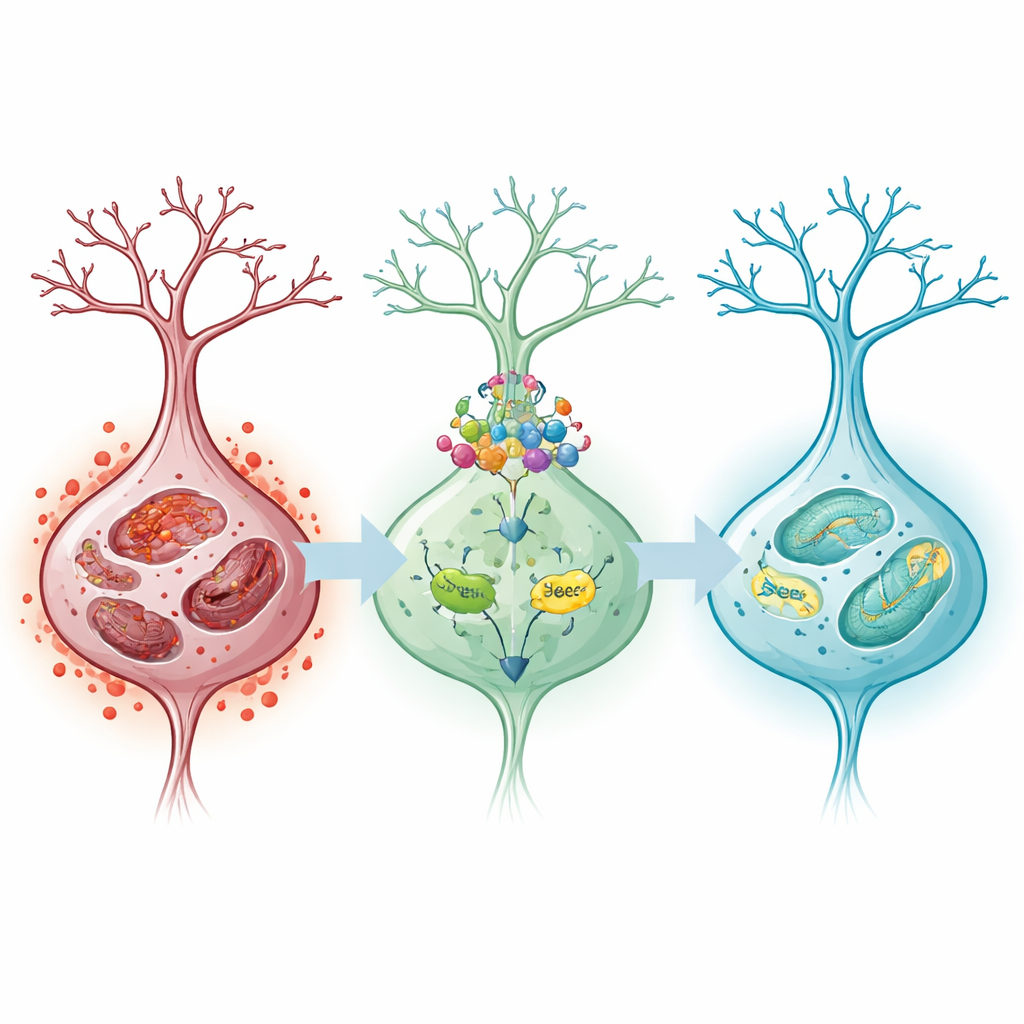
Sondeando el interruptor de defensa celular
Para investigar si esta vía protectora era realmente central en la acción del oridonin, los investigadores redujeron selectivamente Nrf2 en las células de tipo nervioso en cultivo. Cuando Nrf2 se silenciaba, el oridonin ya no pudo restaurar por completo el equilibrio entre hierro y antioxidantes: las moléculas dañinas y los niveles de hierro volvieron a aumentar, la supervivencia celular cayó y la muerte celular se incrementó. Esta reversión indicó que los beneficios del oridonin dependen en gran medida de la capacidad de Nrf2 para activar defensas aguas abajo, incluidas SLC7A11 y GPX4, que conjuntamente ayudan a mantener el glutatión, un antioxidante celular crucial, y a prevenir la peroxidación de los lípidos de las membranas.
Qué podría significar esto para la atención futura del ictus
Para un público general, el mensaje central es que este trabajo identifica una molécula natural que ayuda a las células cerebrales a capear la violenta tormenta química que sigue a la restauración del flujo sanguíneo tras un ictus. Al reforzar un circuito de defensa interno que controla el manejo del hierro y las reservas antioxidantes, el oridonin reduce una forma específica de muerte celular dependiente del hierro y limita el daño cerebral temprano en modelos animales y celulares. El estudio no demuestra aún que el oridonin sea seguro o eficaz en personas, ni aborda la recuperación a largo plazo, pero ofrece un plano prometedor: dirigir la vía Nrf2–SLC7A11–GPX4 para domar la ferroptosis podría algún día complementar las terapias para disolver o eliminar el coágulo, convirtiendo la reperfusión salvadora en un rescate más seguro en lugar de una espada de doble filo.
Cita: Zhang, D., Shao, L., He, M. et al. Nrf2/SLC7A11/GPX4 pathway, a potential target of oridonin in inhibiting ferroptosis during cerebral ischemia-reperfusion injury progression. Sci Rep 16, 14597 (2026). https://doi.org/10.1038/s41598-026-38658-6
Palabras clave: ictus isquémico, lesión por reperfusión, ferroptosis, oridonina, neuroprotección