Clear Sky Science · ar
مسار Nrf2/SLC7A11/GPX4، هدف محتمل للأوريدونين في تثبيط الفيروبتوزيس أثناء تقدم إصابة نقص تروية-إعادة تروية الدماغ
لماذا يمكن أن تؤذي السكتة مرتين
عندما يصاب الشخص بسكتة إقفارية، يسد خثرة تدفق الدم إلى جزء من الدماغ. يسارع الأطباء إلى إعادة فتح الوعاء، لكن فعل استعادة التدفق نفسه قد يسبب موجة من الأضرار، ظاهرة تُسمى إصابة إعادة التروية. تستقصي هذه الدراسة ما إذا كان الأوريدونين، مركب طبيعي موجود في نبات طبي صيني تقليدي، يمكن أن يحمي خلايا الدماغ من هذه الضربة الثانية عبر تهدئة نوع مدمر من موت الخلايا المعتمد على الحديد.
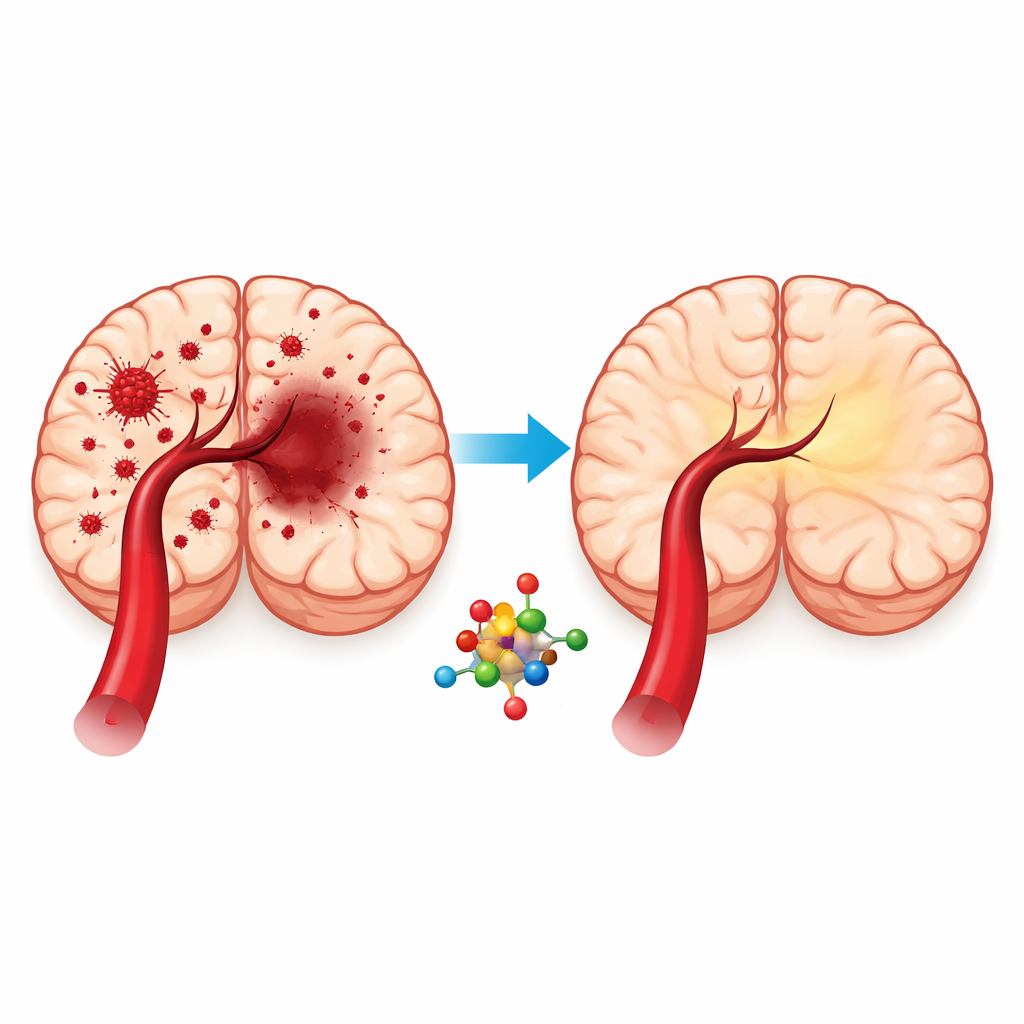
مركب نباتي تحت المجهر
يُستخرج الأوريدونين من العشبة Rabdosia rubescens، المستخدمة منذ زمن طويل في الطب الصيني التقليدي والمعروفة بالفعل بخصائصها المضادة للالتهاب والمضادة للأكسدة. اشتبه الباحثون في أنه قد يحمي الدماغ أيضاً خلال النافذة الحرجة بعد السكتة. لاختبار هذه الفكرة، استخدموا نموذجيْن متممَيْن: جرذان خضعت لانسداد قصير لشريان دماغي رئيسي تلاه استعادة تدفق الدم، وخلايا عصبية شبيهة مزروعة تعرَّضت لفترة من انعدام الأكسجين والجلوكوز تلتها إعادة تأكسج. معاً، تحاكي هذه الأنظمة ما يحدث لأنسجة الدماغ عندما تحرم من الدم ثم تُعاد ترويتها فجأة في العيادة.
عندما يصبح الحديد والأكسدة قاتلين
ركز الفريق على الفيروبتوزيس، نوع حديث من موت الخلايا تغذيه تراكمات الحديد والأكسدة الهائلة للدهون في أغشية الخلايا. في الجرذان، أدت فترات أطول من استعادة التدفق إلى درجات عصبية أسوأ ومناطق احتشاء دماغي أكبر ونخاع عصبي أكثر اضطراباً وموتاً. تراكمت في أنسجة الدماغ معالم الحديد وعلامات كيميائية للأذى التأكسدي، في حين أصبحت المتقدرات—عضيات الطاقة في الخلايا—مشوّهة وممتلئة فجوات. في الوقت نفسه، ضعف مسار إشاراتي وقائي رئيسي يتضمن البروتينات Nrf2 وSLC7A11 وGPX4. هذا المسار عادة يساعد الخلايا على ضبط الحديد والمواد المؤكسدة؛ وعندما انخفض نشاطه ارتفعت علامات مؤيدة للفيروبتوزيس، دلالة على أن الفيروبتوزيس انخرط بقوة بعد إعادة التروية.
كيف يغير الأوريدونين المعطيات
أدى المعالجة المسبقة للجرذان بالأوريدونين قبل انسداد الشريان إلى تغيير هذه النتائج بشكل مرتبط بالجرعة. الحيوانات التي تلقت جرعات أعلى شهدت استعادة أفضل لتدفق الدم، ومناطق سكتة أصغر، وسلوك عصبي قصير المدى محسن. احتفظت خلاياها العصبية ببنية أكثر طبيعية وبتراكمات حديد أقل، كما انخفضت الإشارات الكيميائية الحيوية للفيروبتوزيس—الجزيئات التفاعلية المحتوية على الأكسجين، وارتفاع الحديد، ومنتجات تحلل الدهون. في كل من أدمغة الجرذان والخلايا المزروعة، زاد الأوريدونين من مستويات Nrf2 وSLC7A11 وGPX4 بينما قلل من بروتينات تروِّج للفيروبتوزيس. بدت المتقدرات أكثر صحة وسلامة تحت المجهر الإلكتروني، ما يوحي بأن المركب ساعد في الحفاظ على الآليات الخلوية الأساسية أثناء ضغوط إعادة التروية.
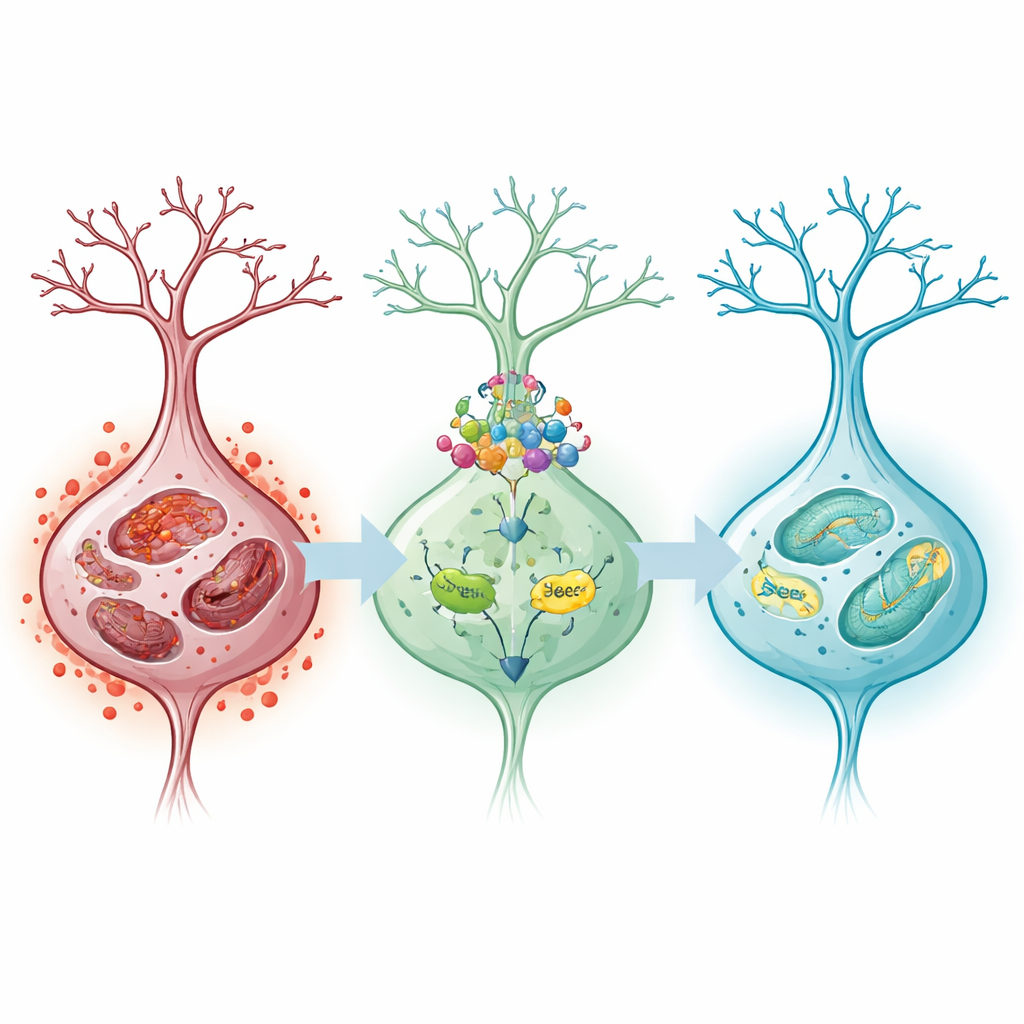
استكشاف مفتاح دفاع الخلية
لاختبار ما إذا كان هذا المسار الوقائي مركزيًا فعلاً لعمل الأوريدونين، خفض الباحثون بشكل انتقائي Nrf2 في الخلايا العصبية الشبيهة المزروعة. عندما تم إسكات Nrf2، لم يعد بإمكان الأوريدونين استعادة توازن الحديد والمضادات الأكسدة بالكامل: ارتفعت الجزيئات الضارة ومستويات الحديد مجددًا، انخفضت بقاء الخلايا، وزاد موت الخلايا. أشارت هذه الرجعة إلى أن فوائد الأوريدونين تعتمد بقوة على قدرة Nrf2 على تشغيل الدفاعات اللاحقة، بما في ذلك SLC7A11 وGPX4، اللذان يساعدان معًا في الحفاظ على الغلوتاثيون، المضاد الأكسدة الخلوي الحاسم، ومنع تأكسد دهون الأغشية.
ماذا قد يعني هذا لرعاية السكتة في المستقبل
بالنسبة لغير المتخصص، الرسالة الأساسية هي أن هذا العمل يحدد جزيئًا طبيعيًا يساعد خلايا الدماغ على اجتياز العاصفة الكيميائية العنيفة التي تلي استعادة تدفق الدم بعد السكتة. عبر تعزيز دائرة دفاعية داخلية تتحكم في التعامل مع الحديد ومخزون المضادات الأكسدة، يقلل الأوريدونين من نوع محدد من موت الخلايا المعتمد على الحديد ويحد من الضرر المبكر للدماغ في نماذج الحيوان والخلايا. لا تثبت الدراسة بعد أن الأوريدونين آمن أو فعال في البشر، ولا تتناول التعافي على المدى الطويل، لكنها تقدم مخططًا واعدًا: استهداف مسار Nrf2–SLC7A11–GPX4 للحد من الفيروبتوزيس قد يكمل يومًا علاجات إذابة الخثرة وإزالتها، محولًا إعادة التروية المنقذة للحياة إلى إنقاذ أكثر أمانًا بدلاً من سلاح ذو حدين.
الاستشهاد: Zhang, D., Shao, L., He, M. et al. Nrf2/SLC7A11/GPX4 pathway, a potential target of oridonin in inhibiting ferroptosis during cerebral ischemia-reperfusion injury progression. Sci Rep 16, 14597 (2026). https://doi.org/10.1038/s41598-026-38658-6
الكلمات المفتاحية: السكتة الإقفارية, إصابة إعادة التروية, الفيروبتوزيس, الأوريدونين, الحماية العصبية