Clear Sky Science · fr
Identifier les indications les plus prometteuses pour de nouveaux traitements en oncologie
Pourquoi trouver les bons patients est important
Les médicaments anticancéreux modernes peuvent sauver des vies, mais déterminer quels groupes précis de patients en bénéficieront est lent, coûteux et incertain. Chaque nouveau médicament doit être testé dans des types et sous-types de cancer spécifiques, et choisir les mauvais peut faire perdre des années de recherche et des millions de dollars — pendant que les patients attendent. Cette étude présente une méthode fondée sur les données pour guider ces choix plus tôt et de manière plus systématique, en utilisant des informations provenant de millions de patients réels plutôt que de s'appuyer principalement sur des intuitions et des découvertes fortuites.
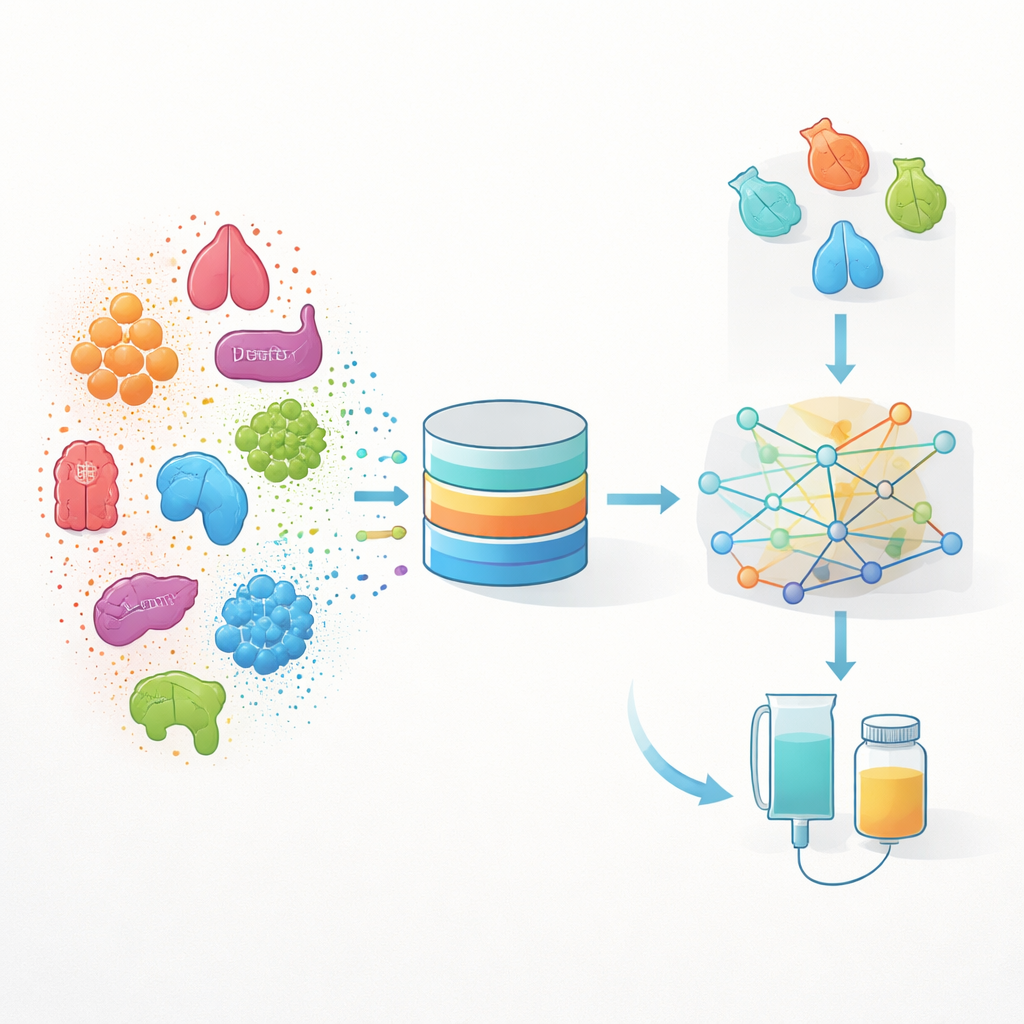
Transformer les données médicales de tous les jours en une carte
Les auteurs construisent une approche qu'ils appellent INSPIRE, pour « INdication Selection and Prioritization In Real-world data and Evaluation ». Plutôt que de partir uniquement d'expériences en laboratoire, INSPIRE apprend à partir de grands ensembles de données du monde réel recueillis lors des soins courants aux États-Unis — dossiers médicaux électroniques et feuilles de remboursement pour plus de deux millions de personnes atteintes de cancer. Ces dossiers laissent une longue trace d'événements pour chaque patient : diagnostics, traitements, analyses biologiques, prélèvements tumoraux, et plus encore. L'équipe transforme chacun de ces événements en une « caractéristique » mathématique puis utilise l'apprentissage automatique pour les placer dans un espace commun où les événements médicaux qui ont tendance à survenir chez des patients similaires se retrouvent proches les uns des autres.
Aller au-delà des libellés généraux de cancer
La plupart des systèmes hospitaliers et de facturation décrivent les maladies à l'aide de codes administratifs qui insistent sur la localisation de la tumeur (par exemple, quelle partie du poumon) plutôt que sur son aspect au microscope. Pour le développement de médicaments anticancéreux, cela est souvent insuffisant, car deux tumeurs dans le même organe peuvent se comporter très différemment et répondre à des thérapies distinctes. INSPIRE s'attaque à ce problème en travaillant directement avec les comptes rendus de pathologie — les descriptions détaillées du tissu tumoral. À partir de ces rapports, la méthode construit des catégories de cancer finement définies, comme des sous-types spécifiques de cancer du poumon, et distingue la maladie à un stade précoce de la maladie avancée et métastatique. Elle « diffuse » ensuite ces informations tumorales le long de la chronologie du patient afin qu'elles puissent être reliées aux traitements, aux résultats d'examens et à d'autres événements survenant ultérieurement.
Tester la méthode sur une immunothérapie majeure
Pour vérifier si INSPIRE aurait pu aider à orienter des décisions dans le monde réel, les chercheurs se sont concentrés sur les médicaments bloquant PD‑1, un point de contrôle immunitaire ciblé par des immunothérapies anticancéreuses largement utilisées. Ils ont reconstitué la situation où ces médicaments étaient encore nouveaux en n'utilisant que des données de 2012 à 2015 et en excluant tous les patients ayant reçu un médicament anti–PD‑1 ou ayant passé le test biomarqueur correspondant. Ils ont choisi trois cancers qui furent parmi les premiers à obtenir l'approbation pour le traitement par PD‑1 comme maladies « de référence ». INSPIRE a ensuite mesuré la similarité de chaque autre sous‑type de cancer des données par rapport à ces références, en se basant sur les motifs des parcours patients, et a produit une liste classée d'indications prometteuses sans savoir lesquelles seraient plus tard approuvées officiellement.
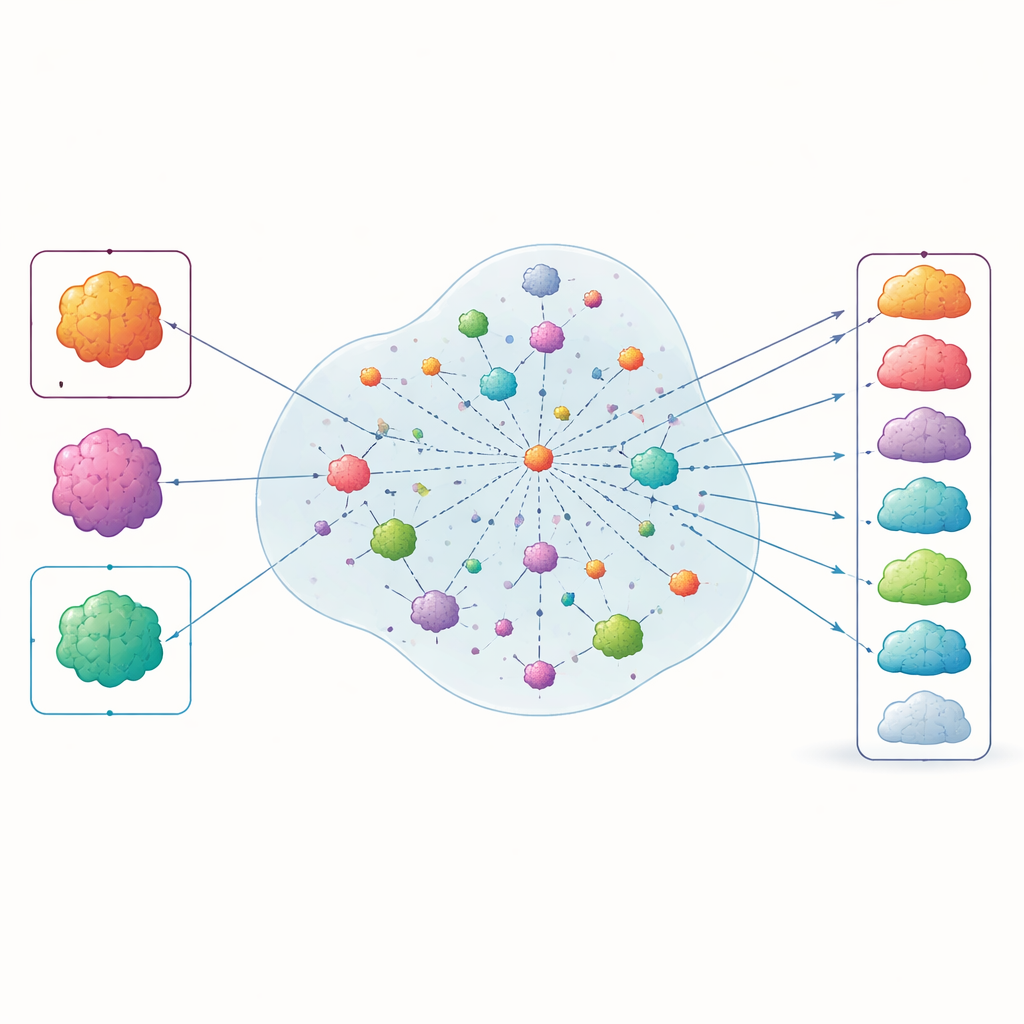
Ce que les classements ont révélé
Quand les auteurs ont « révélés » les résultats et comparé la liste classée d'INSPIRE aux approbations que les régulateurs ont accordées après 2015, environ 70 % des indications cancéreuses qui ont finalement reçu l'approbation pour PD‑1 figuraient parmi les 50 premières places. Les cancers où les médicaments PD‑1 ont échoué à plusieurs reprises en essais tendaient à se classer plus bas. La méthode a montré une performance similaire lorsque les chercheurs ont élargi la fenêtre temporelle pour inclure des années plus récentes et lorsqu'ils ont fait varier les paramètres internes du modèle, ce qui suggère que l'approche est assez robuste. Des analyses ont également indiqué que la carte interne des caractéristiques d'INSPIRE regroupait des éléments médicalement liés — comme les types tumoraux, les traitements et les biomarqueurs — soutenant l'idée qu'elle capture une structure clinique significative plutôt que des motifs aléatoires.
Comment cela pourrait changer le développement des médicaments anticancéreux
INSPIRE n'a pas pour but de remplacer la science de laboratoire ou le jugement clinique, mais d'ajouter une ligne de preuve supplémentaire. En pratique, une entreprise ou un groupe académique développant un nouveau médicament anticancéreux pourrait fournir un petit nombre de types tumoraux pour lesquels il existe déjà des preuves solides de l'efficacité du médicament. INSPIRE utiliserait alors la carte de données du monde réel pour mettre en évidence d'autres sous‑types de cancer qui présentent des similitudes en termes de présentation, d'évolution et de traitements des patients. Ces indications pourraient être priorisées pour des études biologiques complémentaires et, éventuellement, pour des essais cliniques. En améliorant les chances de choisir d'emblée les bons cancers à tester, des approches comme INSPIRE pourraient raccourcir les délais de développement, réduire les coûts et permettre aux patients d'accéder plus rapidement à des thérapies efficaces.
Citation: Eckhoff, M., Klingelschmitt, S., Van Ruijssevelt, L. et al. Finding the most promising indications for novel treatments in oncology. npj Precis. Onc. 10, 135 (2026). https://doi.org/10.1038/s41698-026-01352-x
Mots-clés: développement de médicaments anticancéreux, données du monde réel, apprentissage automatique en oncologie, immunothérapie, sélection d'indications thérapeutiques