Clear Sky Science · ar
العثور على المؤشرات الأكثر وعدًا للعلاجات الجديدة في علم الأورام
لماذا من المهم العثور على المرضى المناسبين
يمكن أن تكون أدوية السرطان الحديثة منقذة للحياة، لكن تحديد المجموعات الدقيقة من المرضى التي ستستفيد منها عملية بطيئة ومكلفة ومليئة بعدم اليقين. يجب اختبار كل دواء جديد في أنواع فرعية محددة من السرطان، واختيار الأنواع الخاطئة قد يضيع سنوات من البحث وملايين الدولارات—بينما ينتظر المرضى. تقدم هذه الدراسة طريقة قائمة على البيانات لتوجيه تلك الاختيارات في وقت أبكر وبشكل أكثر منهجية، باستخدام معلومات من ملايين المرضى الواقعيين بدلاً من الاعتماد بشكل أساسي على الحدس والاكتشافات العرضية.
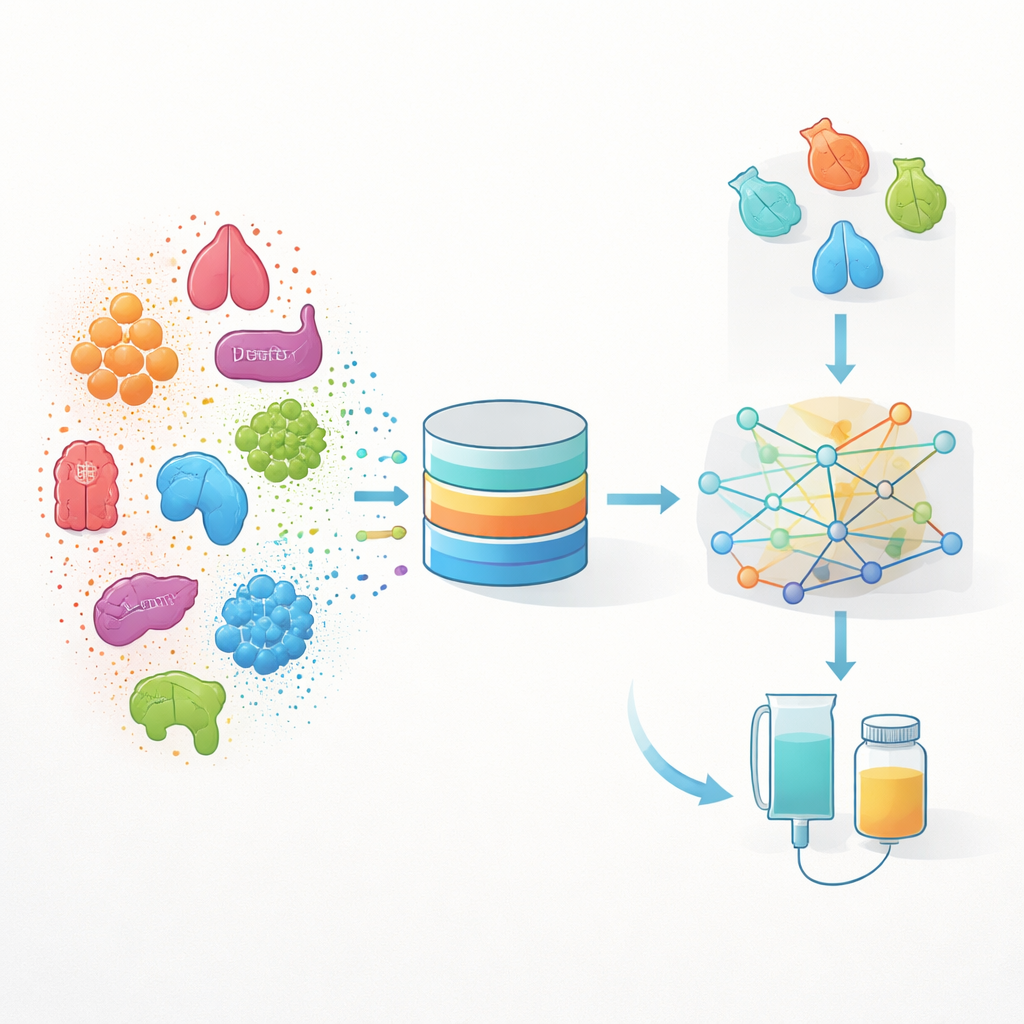
تحويل بيانات الرعاية الروتينية إلى خريطة
بنى المؤلفون نهجًا يسمونه INSPIRE، وهو اختصار لـ "اختيار وتحديد أولويات المؤشرات في البيانات الواقعية والتقييم". بدلاً من البدء بتجارب مختبرية فقط، يتعلم INSPIRE من مجموعات بيانات واقعية واسعة جُمعت أثناء الرعاية الروتينية في الولايات المتحدة—سجلات الصحة الإلكترونية ومطالبات التأمين لأكثر من مليوني شخص مصاب بالسرطان. تحتوي هذه السجلات على تسلسل طويل من الأحداث لكل مريض: التشخيصات والعلاجات والاختبارات المخبرية وعينات الأورام والمزيد. يحول الفريق كل واحد من هذه الأحداث إلى "مَيزة" رياضية ثم يستخدم التعلم الآلي لوضعها في فضاء مشترك حيث تقع الأحداث الطبية التي تميل إلى الحدوث لدى مرضى مماثلين بالقرب من بعضها البعض.
النظر أبعد من تسميات السرطان العامة
تصف معظم أنظمة المستشفيات والفوترة الأمراض باستخدام رموز إدارية تؤكد مكان وجود الورم (على سبيل المثال، أي جزء من الرئة) بدلاً من كيف يظهر تحت المجهر. في تطوير أدوية السرطان، غالبًا ما يكون هذا غير دقيق بما يكفي، لأن ورمين في نفس العضو يمكن أن يتصرّفا بشكل مختلف للغاية ويستجيبا لعلاجات مختلفة. يتعامل INSPIRE مع هذا بالعمل مباشرة مع تقارير الباثولوجيا—الوصف التفصيلي لأنسجة الورم. من هذه التقارير، يبني الأسلوب فئات سرطانية دقيقة مثل الأنواع الفرعية المحددة لسرطان الرئة ويفصل الأمراض المبكرة عن الأمراض المتقدمة والمنتشرة. ثم "ينشر" هذه المعلومات المتعلقة بالورم عبر خط الزمن الخاص بالمريض لتتم ربطها بالعلاجات ونتائج الاختبارات والأحداث الأخرى التي تحدث لاحقًا.
اختبار الطريقة على علاج مناعي رئيسي
لمعرفة ما إذا كان INSPIRE قد ساعد في توجيه قرارات العالم الواقعي، ركز الباحثون على الأدوية التي تمنع PD‑1، وهو نقطة تفتيش مناعية تستهدفها علاجات مناعية للسرطان مستخدمة على نطاق واسع. مثلوا الوضع الذي كانت فيه هذه الأدوية لا تزال جديدة باستخدام بيانات من 2012 إلى 2015 فقط واستبعاد جميع المرضى الذين تلقوا دواءً مضادًا لـ PD‑1 أو خضعوا لاختبار العلامة الحيوية المرتبطة. اختاروا ثلاثة سرطانات كانت من بين أولى التي حصلت على موافقة لعلاج PD‑1 كأمراض "مرجعية". ثم قاس INSPIRE مدى تشابه كل نوع ورم فرعي آخر في البيانات مع هذه المراجع، بناءً على أنماط مسارات المرضى، وأنتج قائمة مرتبة من المؤشرات الواعدة دون أن يعرف أيها سيحصل لاحقًا على الموافقة الرسمية.
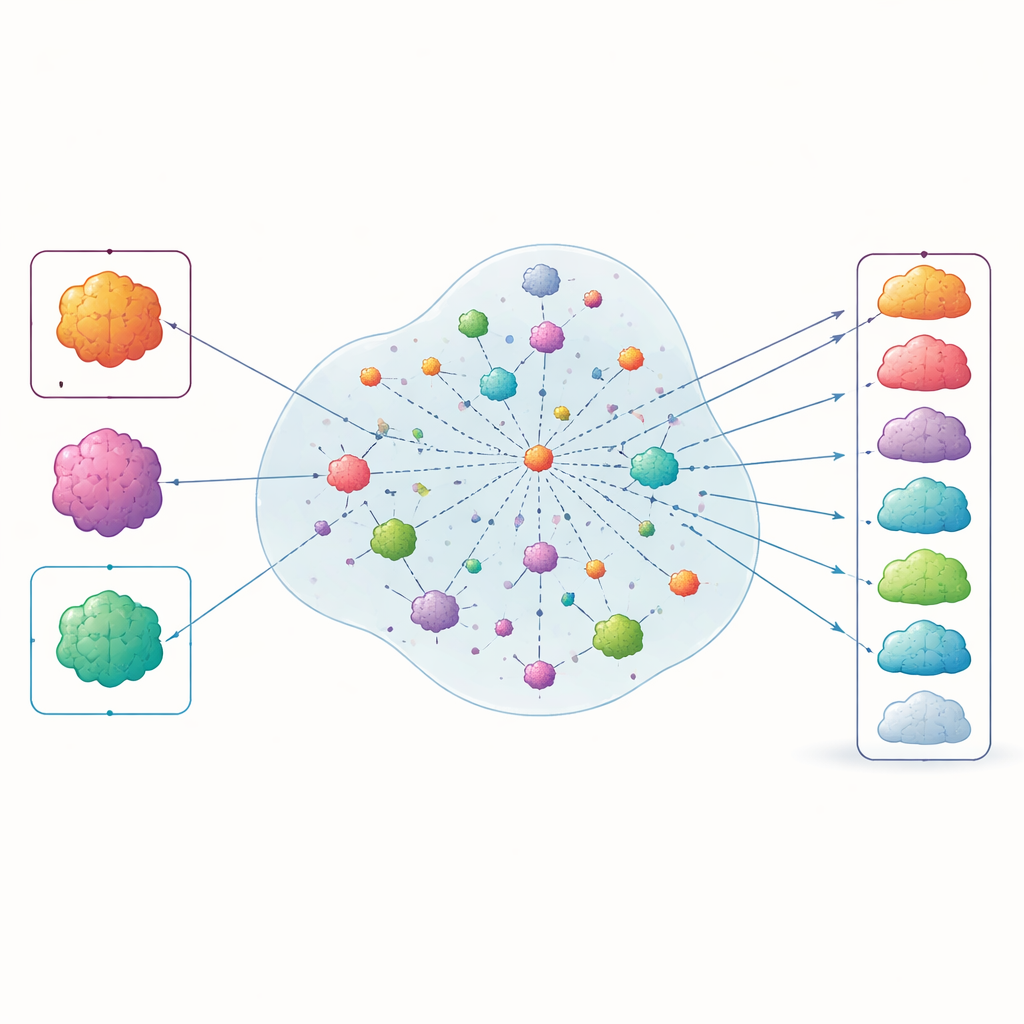
ما الذي كشفته الترتيبات
عندما "كشف" المؤلفون النتائج وقارنوا قائمة INSPIRE المرتبة بالموافقات التي منحتها الجهات المنظمة بعد 2015، ظهر نحو 70 في المئة من مؤشرات السرطان التي حصلت لاحقًا على موافقة PD‑1 في المراكز الخمسين الأولى. أما السرطانات التي فشلت فيها أدوية PD‑1 مرارًا في التجارب فكانت تميل إلى الترتيب في مراتب أدنى. أظهر الأسلوب أداءً مشابهًا عندما وسع الباحثون نافذة الزمن لتشمل سنوات أحدث وعندما غيروا المعلمات الداخلية للنموذج، مما يشير إلى أن النهج متين إلى حدّ ما. أشارت التحليلات أيضًا إلى أن خريطة الميزات الداخلية لدى INSPIRE جمعت عناصر طبية ذات صلة—مثل أنواع الأورام والعلاجات والعلامات الحيوية—مما يدعم الفكرة بأنه يلتقط بنية سريرية ذات معنى بدلاً من أنماط عشوائية.
كيف قد يغيّر هذا تطوير أدوية السرطان
INSPIRE لا يقصد به أن يحل محل العلم المختبري أو الحكم السريري، بل أن يضيف خط أدلة آخر. عمليًا، يمكن لشركة أو مجموعة أكاديمية تطور دواءً جديدًا للسرطان أن تدخل عددًا صغيرًا من أنواع الأورام التي توجد بها بالفعل أدلة قوية على فاعلية الدواء. سيستخدم INSPIRE بعد ذلك خريطة البيانات الواقعية لتسليط الضوء على أنواع ورم فرعية أخرى تبدو مماثلة من حيث كيفية ظهور المرضى، وتقدّمهم، وما يتلقونه من علاج. يمكن إعطاء تلك المؤشرات أولوية لدراسات بيولوجية إضافية—and في نهاية المطاف لتجارب سريرية. من خلال تحسين فرص اختيار أنواع السرطان الصحيحة للاختبار أولًا، يمكن لنهج مثل INSPIRE أن يقصر جداول تطوير الأدوية، ويخفض التكاليف، ويساعد المرضى على الوصول إلى علاجات فعالة في وقت أقرب.
الاستشهاد: Eckhoff, M., Klingelschmitt, S., Van Ruijssevelt, L. et al. Finding the most promising indications for novel treatments in oncology. npj Precis. Onc. 10, 135 (2026). https://doi.org/10.1038/s41698-026-01352-x
الكلمات المفتاحية: تطوير أدوية السرطان, البيانات الواقعية, التعلّم الآلي في علم الأورام, العلاج المناعي, اختيار مؤشرات العلاج