Clear Sky Science · fr
Une association positive entre la protéine Tau phosphorylée 217 (pTau217) et les corrélations neuronales est empêchée par l’allèle du complexe majeur d’histocompatibilité DRB1*13:01
Pourquoi les premiers changements cérébraux comptent
Beaucoup s’inquiètent de la perte de mémoire et de la démence, mais les tout premiers changements dans le cerveau peuvent commencer des décennies avant l’apparition des symptômes. Cette étude a examiné des motifs subtils d’activité cérébrale en parallèle avec des analyses sanguines, le profil génétique et des antécédents d’infections virales chez des femmes âgées non démentes. L’objectif était de déterminer si certains marqueurs sanguins de la maladie d’Alzheimer se rapportent à la souplesse de la communication entre réseaux cérébraux, et si le système immunitaire peut atténuer des effets délétères bien avant le diagnostic de la maladie.
Une fenêtre sur le cerveau en action
Pour étudier le fonctionnement cérébral, les chercheurs ont utilisé la magnétocéphalographie, une technique qui enregistre en temps réel de très faibles signaux magnétiques émis par le cerveau. À partir de ces signaux, ils ont calculé la force avec laquelle différentes régions cérébrales s’activent ensemble, une mesure qu’ils appellent interactions neuronales synchrones. Les cerveaux sains présentent un équilibre : les régions peuvent coopérer quand nécessaire tout en restant indépendantes. Quand les connexions deviennent trop verrouillées, la communication perd de sa flexibilité, ce qui a été associé à de moins bonnes performances cognitives dans des travaux antérieurs. L’équipe a étudié 348 enregistrements cérébraux provenant de 175 femmes et a associé ces données à des analyses sanguines détaillées et à des scores cognitifs.
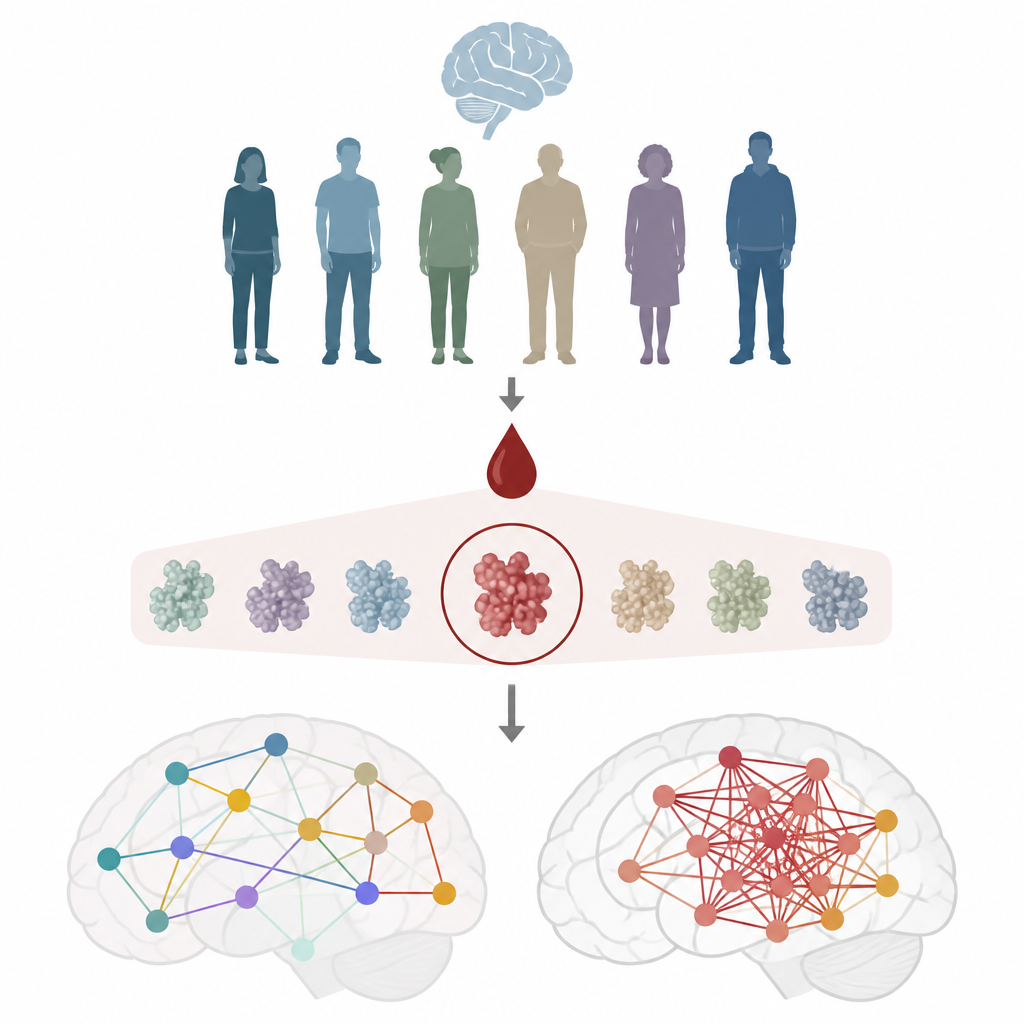
Un marqueur sanguin se distingue
Les échantillons sanguins ont été testés pour sept protéines liées à la maladie d’Alzheimer et aux lésions nerveuses, incluant différentes formes d’amyloïde et de tau, ainsi qu’une protéine des fibres nerveuses. Un seul marqueur, une forme modifiée de la protéine tau appelée pTau217, suivait de manière consistante les modifications des réseaux cérébraux. Des niveaux plus élevés de pTau217 étaient associés à des corrélations cérébrales plus fortes et plus rigides et à des performances légèrement inférieures à un test cognitif standard, même si les participantes étaient globalement en bonne santé cognitive. D’autres marqueurs couramment utilisés, tels que les ratios d’amyloïde ou la tau totale, n’ont pas montré cette relation claire avec l’activité cérébrale, soulignant le lien particulier de pTau217 avec les dysfonctionnements cérébraux précoces.
Virus et bouclier immunitaire protecteur
L’histoire est devenue plus complexe lorsque l’équipe a pris en compte les infections passées et les gènes immunitaires. Beaucoup de virus courants peuvent atteindre le cerveau et déclencher une inflammation. Les femmes présentant des anticorps indiquant une exposition antérieure au virus herpès simplex de type 1 ou à un groupe d’éléments viraux anciens appelés HERVK montraient un lien plus fort entre pTau217 et le rigidification des réseaux cérébraux. Autrement dit, chez celles ayant ces antécédents d’infection, l’augmentation de pTau217 était plus fortement corrélée à une activité cérébrale moins flexible. Pourtant ce schéma disparaissait en grande partie chez les femmes porteuses d’une variante particulière du gène immunitaire connue sous le nom de HLA DRB1*13:01. Des modélisations informatiques ont suggéré que ce gène peut lier particulièrement bien des fragments de protéines virales, ce qui laisse penser qu’il pourrait aider le système immunitaire à éliminer ou contrôler ces influences virales.
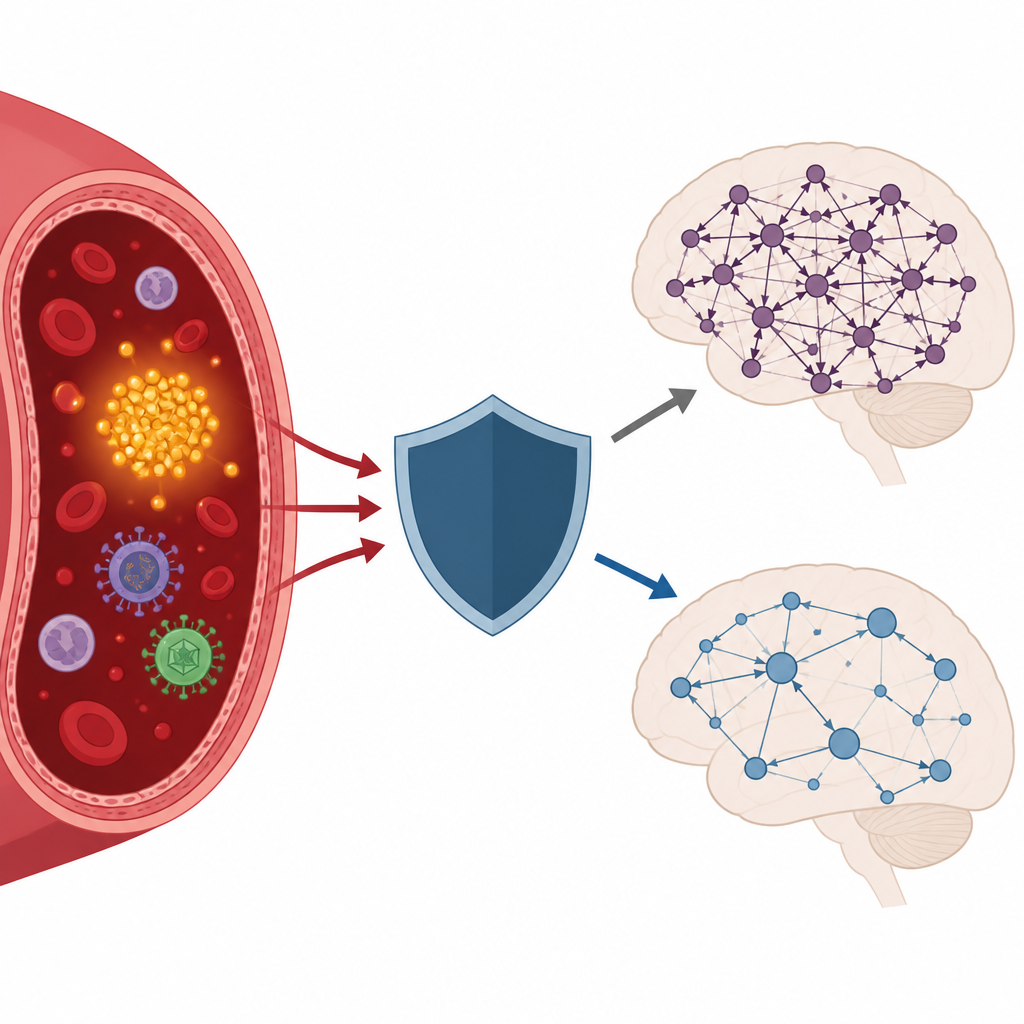
Gènes qui nuisent et gènes qui protègent
Les chercheurs ont également testé un autre gène de risque bien connu pour la maladie d’Alzheimer, ApoE. Contrairement au gène HLA, ApoE n’a pas modifié la relation entre pTau217 et les mesures des réseaux cérébraux dans ce groupe. Cela suggère que, du moins à ces stades précoces, des gènes immunitaires qui influent sur la façon dont l’organisme gère les traces virales peuvent jouer un rôle plus direct dans la protection de la communication cérébrale que le statut ApoE seul. Fait important, lorsque l’une des deux variantes apparentées HLA DRB1*13:01 ou DRB1*13:02 était présente, l’effet délétère combiné d’un pTau217 élevé et de réseaux cérébraux rigides sur les scores cognitifs n’était plus observable.
Ce que cela signifie pour la santé du cerveau
Pris ensemble, les résultats suggèrent que les taux sanguins de pTau217 reflètent des perturbations subtiles du fonctionnement des réseaux cérébraux chez des femmes non démentes et que ces perturbations s’accompagnent d’une légère baisse des capacités cognitives. L’exposition passée à certains virus semble intensifier ce lien, tandis que des gènes immunitaires spécifiques peuvent presque l’éteindre, agissant comme un bouclier protecteur pour le cerveau. Pour un lecteur non spécialiste, le message clé est que le risque de démence peut émerger d’une interaction à long terme entre l’histoire infectieuse, des marqueurs sanguins de stress neuronal et les défenses immunitaires de l’organisme. Comprendre cet équilibre pourrait un jour aider à identifier plus tôt les personnes à risque et à orienter des stratégies de prévention adaptées à leur profil immunitaire et infectieux.
Citation: James, L.M., Stratigopoulos, G., Leuthold, A.C. et al. A positive association between phosphorylated Tau217 (pTau217) and neural correlations is prevented by human leukocyte antigen allele DRB1*13:01. Sci Rep 16, 15026 (2026). https://doi.org/10.1038/s41598-026-44894-7
Mots-clés: pTau217, réseaux cérébraux, risque d’Alzheimer, HLA DRB1*13:01, infections virales