Clear Sky Science · de
Eine positive Assoziation zwischen phosphoryliertem Tau217 (pTau217) und neuronalen Korrelationen wird durch das humane Leukozytenantigen-Allel DRB1*13:01 verhindert
Warum frühe Veränderungen im Gehirn wichtig sind
Viele Menschen sorgen sich um Gedächtnisverlust und Demenz, doch die frühesten Veränderungen im Gehirn können Jahrzehnte vor dem Auftreten von Symptomen beginnen. Diese Studie untersuchte subtile Muster neuronaler Aktivität zusammen mit Bluttests, genetischen Daten und früheren Virusinfektionen bei älteren Frauen ohne Demenz. Ziel war es zu klären, ob bestimmte Blutmarker für Alzheimer mit der Flexibilität der Kommunikation in Gehirnnetzwerken zusammenhängen und ob das Immunsystem schädliche Effekte lange vor einer klinischen Diagnose abschwächen kann.
Ein Blick in das arbeitende Gehirn
Um die Gehirnfunktion zu untersuchen, nutzten die Forschenden Magnetoenzephalographie, eine Technik, die winzige magnetische Signale des Gehirns in Echtzeit aufzeichnet. Aus diesen Signalen berechneten sie, wie stark verschiedene Hirnregionen gemeinsam feuern, ein Maß, das sie synchrone neuronale Interaktionen nennen. Gesunde Gehirne zeigen ein Gleichgewicht: Regionen können zusammenarbeiten, wenn es nötig ist, sind aber auch in der Lage, unabhängig zu agieren. Wenn Verbindungen zu stark verkrampfen, geht Kommunikation an Flexibilität verloren, was in früheren Arbeiten mit schlechteren kognitiven Testergebnissen in Verbindung gebracht wurde. Das Team analysierte 348 Gehirnscans von 175 Frauen und kombinierte diese Daten mit detaillierten Bluttests und kognitiven Ergebnissen.
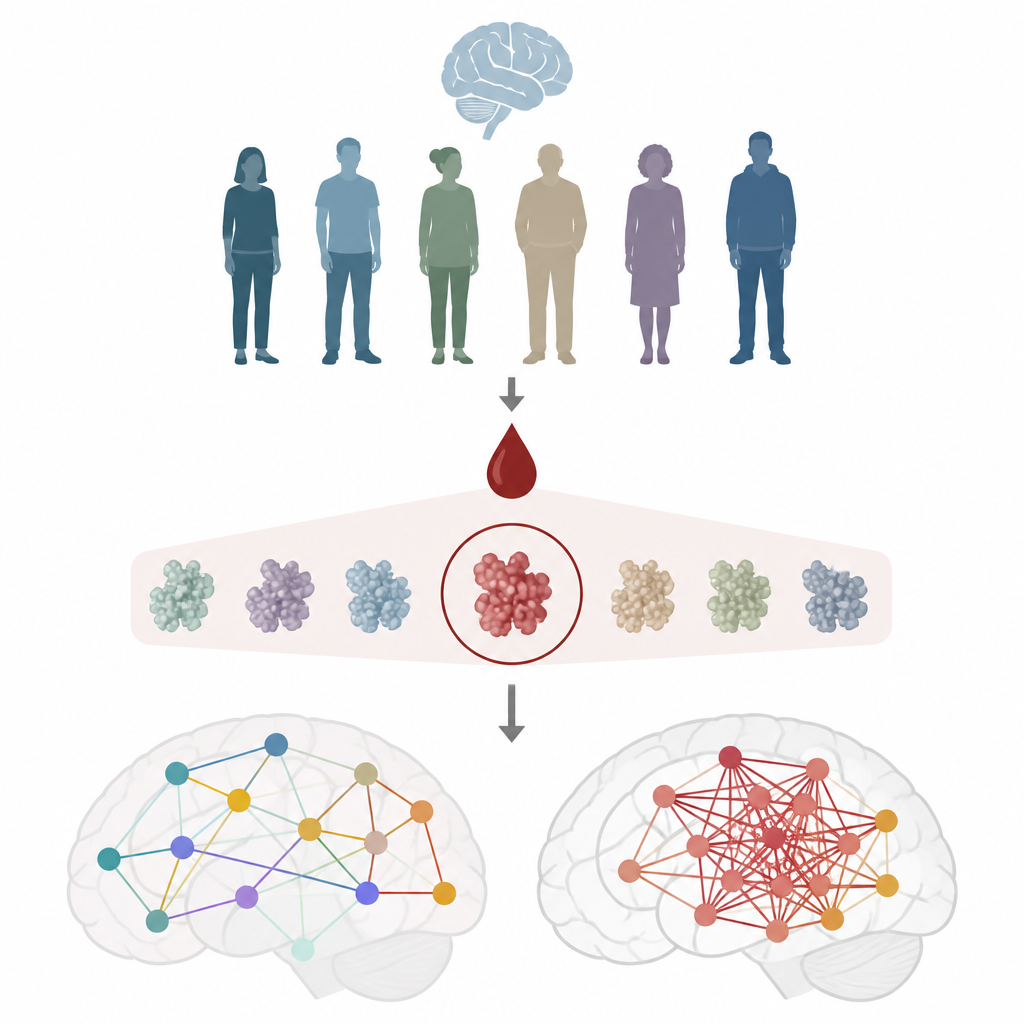
Ein Blutmarker sticht heraus
In Blutproben wurden sieben Proteine getestet, die mit Alzheimer und Nervenschädigung in Verbindung stehen, darunter verschiedene Formen von Amyloid und Tau sowie ein Protein der Nervenfasern. Nur ein Marker, eine modifizierte Form von Tau namens pTau217, korrelierte beständig mit Veränderungen in den Gehirnnetzwerken. Höhere pTau217-Werte standen im Zusammenhang mit stärkeren, starrer wirkenden neuronalen Korrelationen und mit leicht schlechteren Leistungen in einem standardisierten kognitiven Test, obwohl die Teilnehmenden insgesamt kognitiv weitgehend gesund waren. Andere verbreitete Marker, wie Amyloid-Verhältnisse oder Gesamt-Tau, zeigten diese klare Beziehung zur Gehirnaktivität nicht, was die besondere Verbindung von pTau217 zu frühen Hirnfunktionen unterstreicht.
Viren und ein schützender Immunschild
Die Geschichte wurde komplexer, als das Team frühere Infektionen und Immun-Gene berücksichtigte. Viele verbreitete Viren können das Gehirn erreichen und Entzündungen auslösen. Frauen, die Antikörper aufwiesen, die auf eine frühere Exposition gegenüber Herpesvirus Typ 1 oder gegenüber einer Gruppe alter viraler Elemente namens HERVK hindeuteten, zeigten eine stärkere Verbindung zwischen pTau217 und verfestigten Gehirnnetzwerken. Mit anderen Worten: Bei Personen mit solcher Infektionsvorgeschichte war ein Anstieg von pTau217 stärker mit weniger flexibler Gehirnaktivität verknüpft. Dieses Muster verschwand jedoch weitgehend bei Frauen, die eine bestimmte Variante des Immungens HLA DRB1*13:01 trugen. Computermodelle deuteten darauf hin, dass dieses Gen Stücke viraler Proteine besonders gut binden kann, was nahelegt, dass es dem Immunsystem helfen könnte, diese viralen Einflüsse zu beseitigen oder zu kontrollieren.
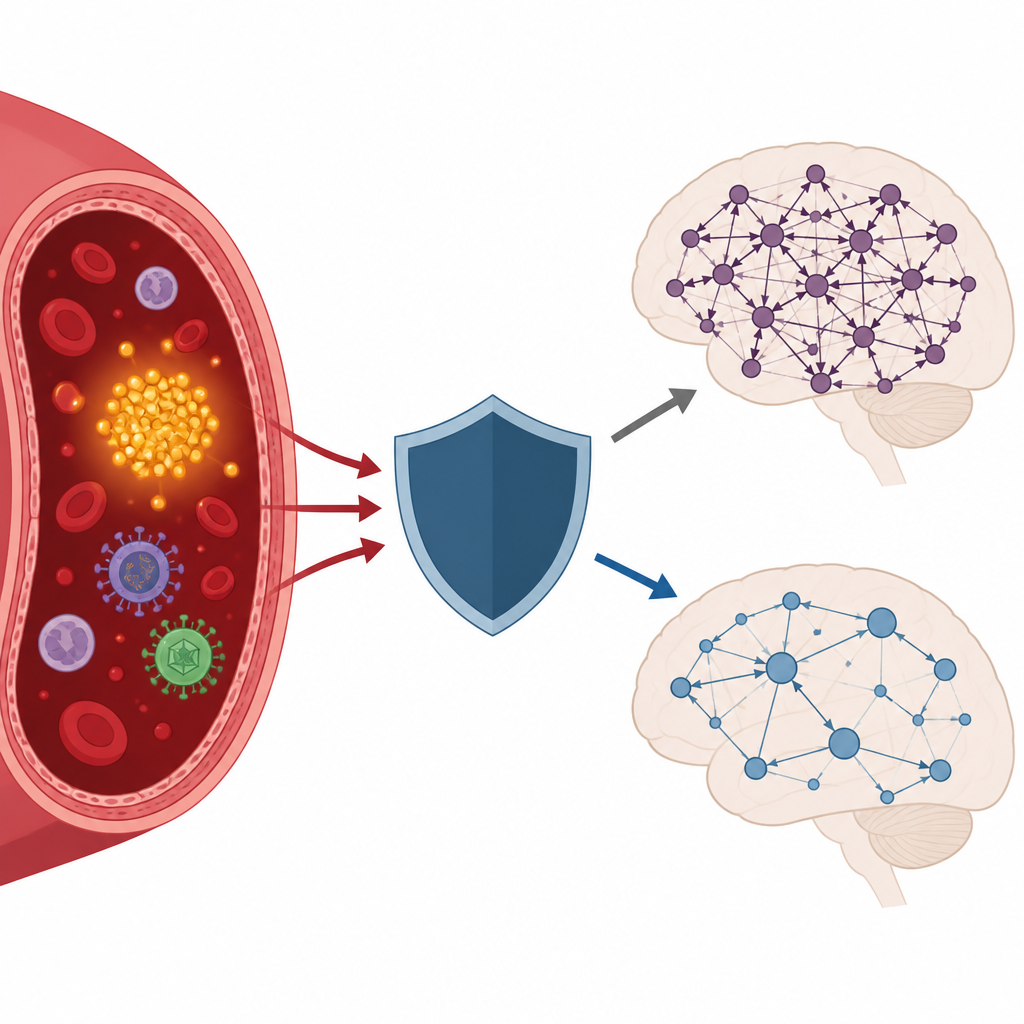
Gene, die schaden, und Gene, die schützen
Die Forschenden untersuchten außerdem ein weiteres bekanntes Alzheimer-Risikogen, ApoE. Im Gegensatz zum HLA-Gen veränderte ApoE in dieser Gruppe nicht die Beziehung zwischen pTau217 und den Maßen der Gehirnnetzwerke. Das deutet darauf hin, dass zumindest in diesen frühen Stadien Immun-Gene, die beeinflussen, wie der Körper mit viralen Spuren umgeht, eine direktere Rolle beim Schutz der Gehirnkommunikation spielen könnten als der ApoE-Status allein. Wichtig ist, dass wenn eine der beiden verwandten HLA-Varianten DRB1*13:01 oder DRB1*13:02 vorhanden war, der schädliche kombinierte Effekt von hohem pTau217 und starren Gehirnnetzwerken auf die kognitiven Werte nicht mehr nachweisbar war.
Was das für die Gehirngesundheit bedeutet
Insgesamt deuten die Ergebnisse darauf hin, dass Blutspiegel von pTau217 subtile Störungen in der Funktionsweise von Gehirnnetzwerken bei alltäglichen, nicht-demenzkranken Frauen widerspiegeln und dass diese Störungen mit leicht schlechteren Denkfähigkeiten verbunden sind. Eine frühere Exposition gegenüber bestimmten Viren scheint diese Verbindung zu verstärken, während spezifische Immun-Gene sie nahezu abschalten können und so wie ein Schutzschild für das Gehirn wirken. Für Laien ist die Kernbotschaft, dass Demenzrisiko aus einem langfristigen Zusammenspiel von Infektionsgeschichte, Blutmarkern für neuronalen Stress und den Immunabwehrkräften des Körpers entstehen kann. Dieses Gleichgewicht besser zu verstehen, könnte eines Tages helfen, Menschen mit erhöhtem Risiko früher zu identifizieren und Präventionsstrategien zu entwickeln, die auf ihr Immun- und Infektionsprofil zugeschnitten sind.
Zitation: James, L.M., Stratigopoulos, G., Leuthold, A.C. et al. A positive association between phosphorylated Tau217 (pTau217) and neural correlations is prevented by human leukocyte antigen allele DRB1*13:01. Sci Rep 16, 15026 (2026). https://doi.org/10.1038/s41598-026-44894-7
Schlüsselwörter: pTau217, Gehirnnetzwerke, Alzheimer-Risiko, HLA DRB1*13:01, virale Infektionen