Clear Sky Science · fr
Variation génétique des populations caractérisée par séquençage en pools indépendants successifs : le Cyprus Genome Project
Pourquoi l’ADN d’une petite île compte
Imaginez devoir diagnostiquer et traiter une maladie en vous appuyant sur des cartes qui décrivent principalement d’autres personnes, d’autres régions. C’est la situation à laquelle de nombreux pays sont confrontés en génétique moderne. Cette étude comble cette lacune pour Chypre en construisant la première carte de référence génétique à grande échelle réalisée spécifiquement à partir de personnes vivant sur l’île. En regroupant astucieusement l’ADN de 10 000 volontaires, les chercheurs ont créé une méthode rentable et respectueuse de la vie privée pour établir quelles variations génétiques sont communes ou rares chez les Chypriotes — et comment ces profils diffèrent des moyennes mondiales sur lesquelles les cliniciens se reposent généralement.
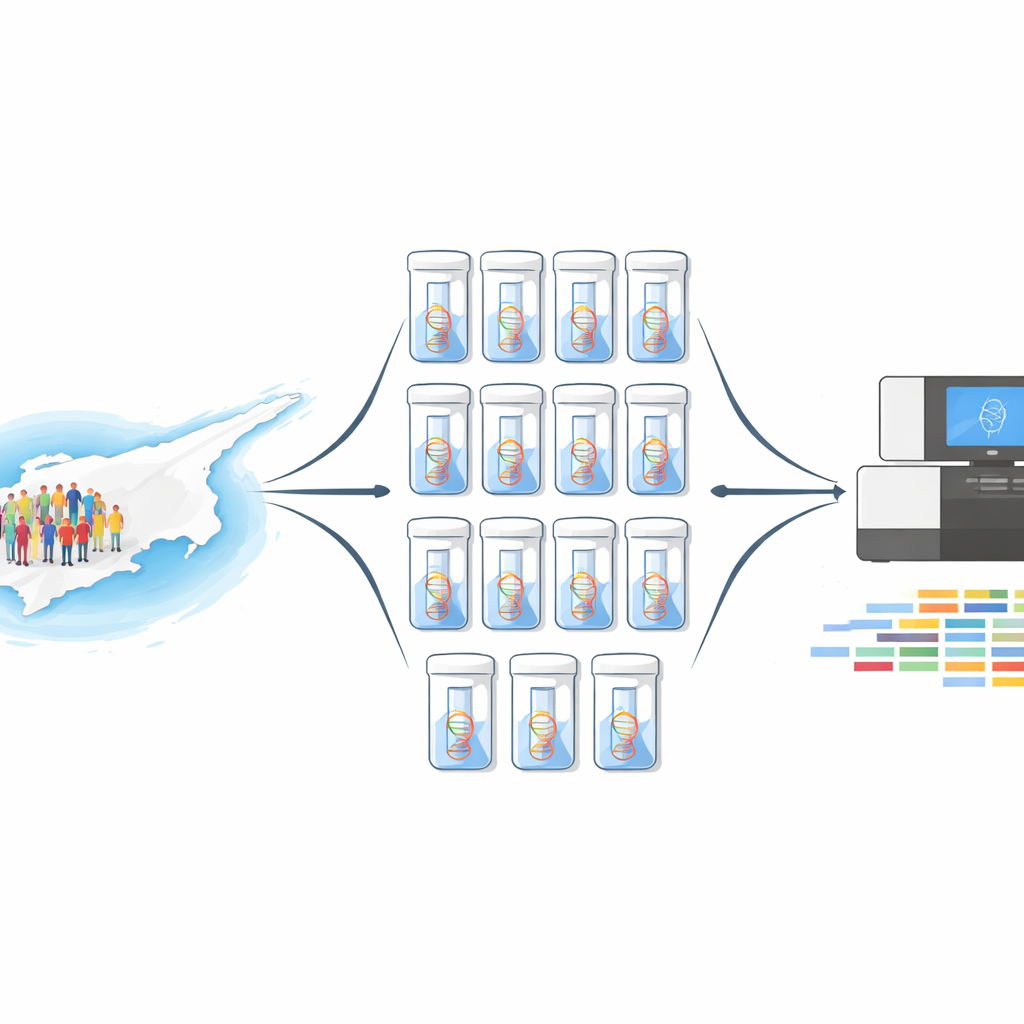
Une nouvelle façon d’examiner des milliers de personnes à la fois
Séquenencer le génome complet de 10 000 individus un par un serait extrêmement coûteux et long. À la place, l’équipe a utilisé une méthode dite de pooling d’ADN. Ils ont combiné des quantités égales d’ADN provenant de 1 000 donneurs volontaires de moelle osseuse en un seul mélange, et ont répété l’opération dix fois, créant ainsi dix pools indépendants. Chaque pool a ensuite été séquencé deux fois : une fois par séquençage de l’exome entier, qui explore toutes les régions codant pour des protéines, et une fois avec un panel ciblé de 813 gènes d’importance médicale. Ce dispositif a permis d’obtenir à la fois une large couverture du génome et une profondeur très importante sur les gènes les plus pertinents pour la maladie.
Séparer les vrais signaux du bruit
Le pooling d’ADN comporte des compromis. S’il protège l’identité des individus et réduit les coûts, il rend aussi plus difficile la détection des changements très rares et la distinction entre un signal faible et une erreur instrumentale. Pour y remédier, les auteurs ont intégré des garde‑fous solides dans leur étude. Ils ont exigé que tout variant génétique rapporté soit soutenu par au moins 20 lectures de séquençage et apparaisse dans au moins trois des dix pools indépendants. Pour un sous‑ensemble à haute confiance, ils ont demandé des milliers de lectures totales à travers les pools. Ils ont également vérifié que la distribution des fréquences des variants était cohérente entre les pools et comparé leurs résultats aux bases de données internationales et à des études chypriotes plus petites. Un excellent accord statistique a montré que l’approche par pools pouvait estimer la fréquence de chaque variant avec une grande précision.
Ce qui distingue l’ADN chypriote
À partir des données groupées, le projet a répertorié plus de quatre millions de variants génétiques, dont plus de 100 000 n’apparaissent pas dans les grandes ressources internationales telles que gnomAD et ClinVar. Beaucoup de ces différences ont une portée clinique. Certaines modifications génétiques associées à des troubles sanguins ou des problèmes de saignement, par exemple, sont plusieurs dizaines de fois plus fréquentes à Chypre que dans les bases de données mondiales, ce qui suggère qu’elles pourraient mériter d’être incluses dans des programmes nationaux de dépistage. À l’inverse, l’équipe a aussi identifié des variants qui paraissent extrêmement rares au niveau mondial mais qui sont relativement fréquents chez des donneurs chypriotes en bonne santé. Sans données locales, de telles variantes pourraient être à tort suspectées de causer une maladie simplement parce qu’elles sont peu communes ailleurs.
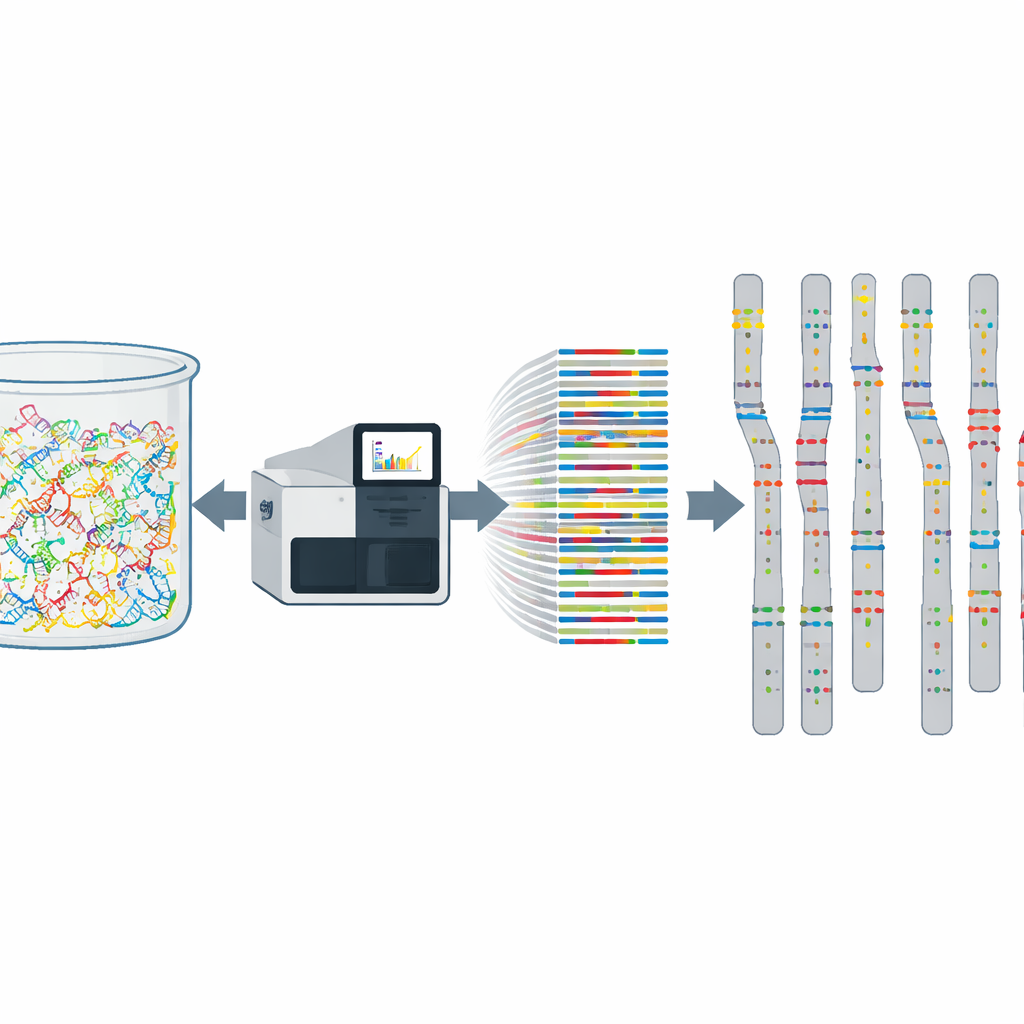
Repenser les scores de risque et les tests génétiques
La nouvelle carte montre aussi que certains variants associés à un risque élevé qui sont courants au niveau mondial sont beaucoup plus rares à Chypre, et inversement. Ce décalage a des conséquences pratiques. Beaucoup d’outils modernes, comme les scores de risque polygéniques qui estiment la probabilité de développer des affections telles que le cancer ou les maladies cardiovasculaires, supposent que les fréquences des variants dans la population cible ressemblent à celles de la population de référence utilisée pour construire l’outil. Les données chypriotes révèlent que cette hypothèse échoue souvent. En conséquence, les scores de risque et les panels diagnostiques basés sur des données étrangères peuvent surestimer ou sous‑estimer le risque pour les patients chypriotes, sauf s’ils sont recalibrés à l’aide de cette nouvelle référence locale.
Comment cette ressource peut façonner les soins futurs
Pour le grand public, l’essentiel est que ce projet transforme le contexte génétique de Chypre d’un angle mort en une carte détaillée. La base de données sur cyprusgenome.org permet aux cliniciens et aux chercheurs de déterminer si un variant génétique est réellement rare et suspect localement, ou simplement une caractéristique bénigne de l’ascendance chypriote que les études mondiales ont négligée. Cette clarté peut prévenir des erreurs de diagnostic, orienter des stratégies nationales de dépistage plus intelligentes et poser les bases d’outils de prédiction du risque plus précis, adaptés à la population de l’île. À mesure que des séquençages supplémentaires et de nouvelles couches de données, comme des profils des gènes immunitaires et des mesures d’activité génique, seront ajoutés, cette ressource est destinée à devenir un pilier pour la médecine de précision et la planification de la santé publique à Chypre.
Citation: Antoniades, A., Chi, J., Brown, C. et al. Population genetic variation characterised through serial independent pool-seq: the Cyprus Genome Project. Sci Rep 16, 14215 (2026). https://doi.org/10.1038/s41598-026-44707-x
Mots-clés: génome de Chypre, génétique des populations, séquençage d’ADN en pool, variants rares, médecine de précision