Clear Sky Science · fr
Un atlas cutané multimodal identifie une communauté immuno-stromale multicellulaire associée à une cornification perturbée et à une expansion T cellulaire spécifique dans la dermatite atopique
Pourquoi cette maladie qui démange est importante
La dermatite atopique, souvent appelée eczéma, touche des millions d’enfants et d’adultes qui présentent une peau rouge, prurigineuse et facilement irritée. Les cliniciens savent que la barrière externe de la peau et le système immunitaire sont impliqués, mais le mélange exact de cellules et de signaux dans une zone de peau enflammée a été difficile à observer en détail. Cette étude utilise des techniques unicellulaires de pointe pour créer un « atlas » détaillé de la peau humaine, révélant quelles cellules dysfonctionnent dans la dermatite atopique et comment leurs interactions peuvent affaiblir la couche protectrice de la peau et alimenter l’inflammation chronique.
Cartographier chaque cellule dans la peau saine et malade
Pour construire cet atlas, les chercheurs ont prélevé de petites biopsies par punch dans la peau d’adultes atteints ou non de dermatite atopique. Ils ont analysé plus de 280 000 cellules individuelles issues de ces échantillons, puis les ont intégrées à plus de 400 000 cellules provenant d’études antérieures, obtenant ainsi une carte combinée de plus de 700 000 cellules cutanées. Grâce au séquençage ARN unicellulaire, ils ont mesuré les gènes activés dans chaque cellule, et dans un sous-ensemble de lymphocytes T ils ont également séquencé les récepteurs des cellules T pour suivre quelles cellules T s’étaient multipliées en réponse à des déclencheurs. Cette approche leur a permis de distinguer 16 classes cellulaires larges et 86 sous-types plus fins, y compris des populations rares habituellement manquées, comme les cellules cutanées complètement cornifiées et des fibroblastes spécialisés.
Comment les cellules qui construisent la peau dévient de leur trajectoire
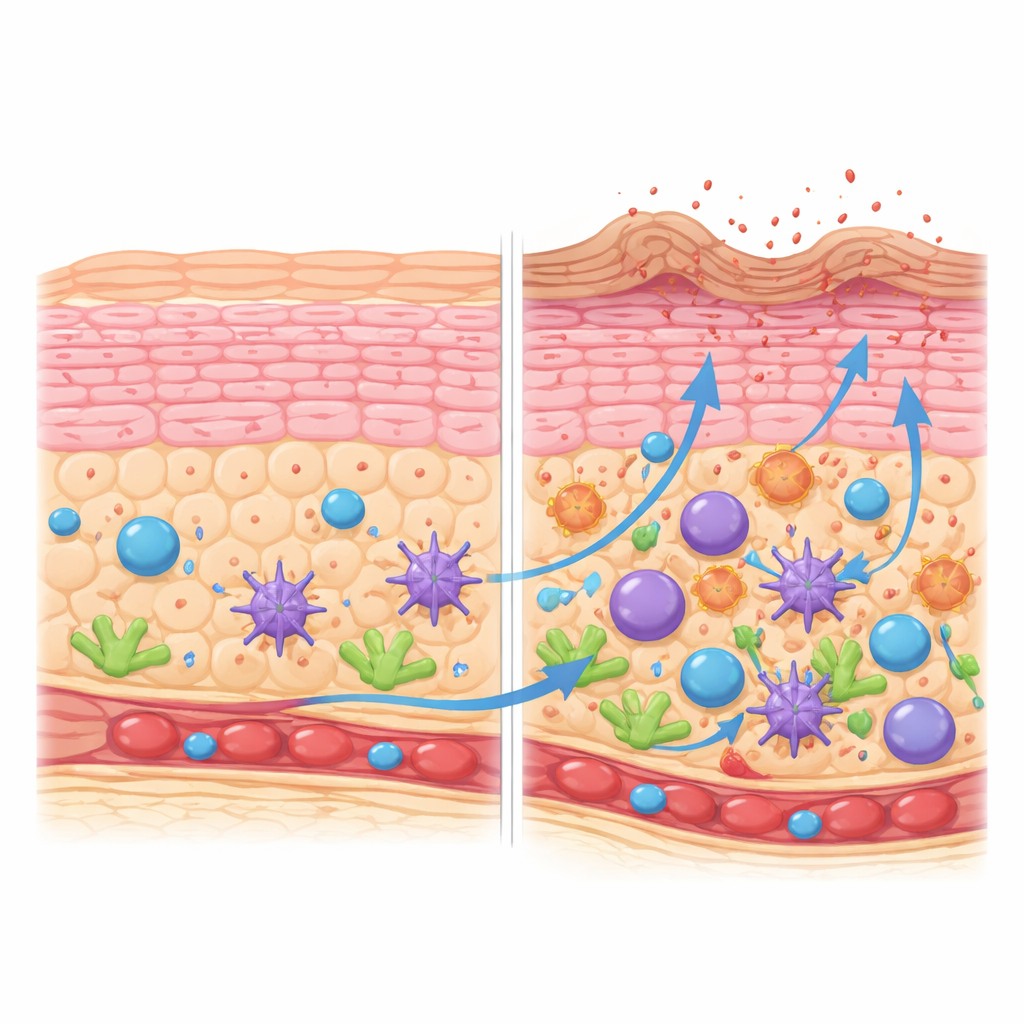
La barrière cutanée repose sur la maturation ordonnée des kératinocytes, qui migrent de la couche basale vers une surface cornifiée et résistante. En reconstruisant ce parcours, l’équipe a montré que dans la peau saine les kératinocytes progressent de manière fluide à travers des stades définis, activant au bon moment des gènes impliqués dans la structure, les lipides et la mort cellulaire contrôlée. Dans les lésions de dermatite atopique, cette progression est déformée. On observe davantage de kératinocytes en division et de cellules en stade intermédiaire, mais moins de cellules atteignant un état pleinement mature et cornifié. La couche supérieure est biaisée vers un sous-type moins avancé qui exprime moins des protéines nécessaires à la formation d’une barrière « briques-et-mortier » solide, et davantage de petites protéines liées au stress. Ces cellules cornifiées produisent aussi en excès des molécules inflammatoires de la famille de l’interleukine-1, orientant la surface vers l’irritation.
Un quartier densément peuplé de cellules immunitaires et de soutien
La peau atopique enflammée ne contenait pas seulement plus de cellules immunitaires ; elle montrait un changement organisé dans la composition cellulaire. Certains cellules dendritiques, qui captent et présentent les antigènes, s’accumulaient le long d’un parcours de maturation vers un état hautement activé et migratoire. Ces cellules produisaient des signaux qui attirent et façonnent les lymphocytes T et les cellules lymphoïdes innées. Parallèlement, un type particulier de fibroblaste, marqué par la chimiokine CCL19 et des enzymes liées à la régulation immunitaire, s’est développé dans le derme de soutien. Ces fibroblastes ont augmenté l’expression de gènes impliqués dans la présentation d’antigènes, l’orientation des cellules immunitaires et le remodelage tissulaire, suggérant que l’architecture de soutien de la peau participe activement au maintien de l’inflammation plutôt que de se contenter de la soutenir.
Des lymphocytes T uniques qui reviennent sans cesse
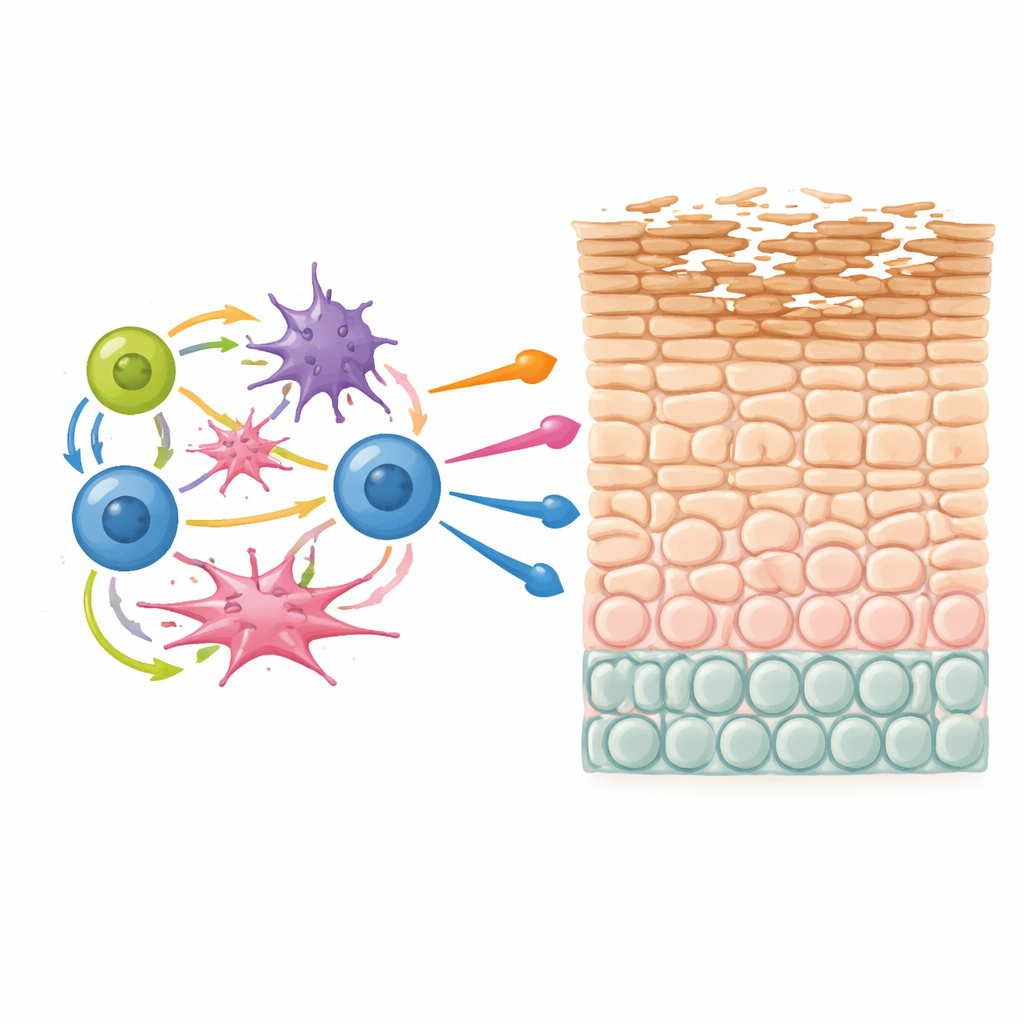
Une découverte marquante fut une population de lymphocytes T trouvée principalement dans les lésions de dermatite atopique qui produisaient simultanément trois molécules inflammatoires clés : IL-13, IL-22 et IL-26. Ces lymphocytes T existaient sous forme auxiliaire et cytotoxique et partageaient un programme génétique commun associé au prurit, à l’allergie de type 2 et au remodelage tissulaire. En reliant l’expression génique aux données des récepteurs des cellules T, les chercheurs ont montré que ces cellules productrices triples étaient souvent clonellement étendues — c’est-à-dire qu’un lymphocyte T initial avait rencontré à plusieurs reprises son antigène et s’était multiplié. Ce schéma suggère fortement une stimulation chronique, probablement par des antigènes environnementaux persistants ou endogènes dans la peau, et identifie ces cellules comme des acteurs potentiels majeurs de la maladie.
Une boucle inflammatoire auto-renforçante liée à la génétique
Lorsque l’équipe a examiné comment les types cellulaires fluctuent ensemble entre les patients, elle a identifié une communauté multicellulaire qui réapparaissait dans les lésions. Cette communauté incluait les lymphocytes T IL-13/IL-22/IL-26, des cellules dendritiques activées, des cellules lymphoïdes innées et naturelles en cycle, et des fibroblastes riches en CCL19. L’analyse computationnelle des paires ligand–récepteur indiquait que ces cellules échangent des signaux dans des boucles de rétroaction positives — les cellules dendritiques recrutent et activent les lymphocytes T, les lymphocytes T renforcent à leur tour les cellules dendritiques et les fibroblastes, et les cellules innées ajoutent d’autres signaux inflammatoires. Beaucoup des gènes mis en évidence dans ce réseau, y compris des gènes de risque bien connus comme IL13 et des composants de la barrière cutanée tels que la filaggrine, se chevauchent avec des régions identifiées par de larges études génétiques sur la dermatite atopique et les maladies allergiques associées. Cela suggère que des variants hérités peuvent prédisposer certaines personnes à former précisément cette communauté instable, qui perturbe ensuite la maturation des kératinocytes et affaiblit la barrière.
Ce que cela signifie pour les personnes vivant avec l’eczéma
Dans l’ensemble, ces résultats présentent la dermatite atopique comme un problème d’ensemble cellulaire plutôt que comme un seul coupable. Un groupe spécialisé de lymphocytes T, de cellules dendritiques, de fibroblastes et de cellules lymphoïdes innées semble s’auto-verrouiller dans un état inflammatoire qui interfère avec la capacité de la peau à cornifier correctement et à se sceller. Parce que de nombreux médicaments actuels et émergents ciblent justement les signaux partagés au sein de ce réseau, ce nouvel atlas aide à expliquer pourquoi certains traitements fonctionnent, pourquoi d’autres n’aident que des sous-groupes de patients, et où pourraient se trouver de nouvelles cibles médicamenteuses. Pour les personnes atteintes d’eczéma, ce travail ouvre la voie à des thérapies futures qui non seulement calment la suractivité immunitaire mais aussi restaurent la barrière cutanée en rompant les conversations cellulaires nocives qui entretiennent la maladie.
Citation: Fiskin, E., Eraslan, G., Alora-Palli, M.B. et al. Multi-modal skin atlas identifies a multicellular immune-stromal community associated with disrupted cornification and specific T cell expansion in atopic dermatitis. Nat Commun 17, 3194 (2026). https://doi.org/10.1038/s41467-026-69587-7
Mots-clés: dermatite atopique, barrière cutanée, atlas unicellulaire, cellules immunitaires, génétique de l’eczéma