Clear Sky Science · es
Validación y aplicación de un ensayo cuantitativo de PCR estandarizado para la evaluación de genes de resistencia antimicrobiana en aguas superficiales
Por qué importan los genes diminutos en aguas salvajes
Cuando recorres un parque nacional y ves arroyos claros y rápidos, parecen intocados por las personas. Pero incluso en lugares remotos, pueden aparecer trazas microscópicas de nuestros antibióticos en forma de genes que hacen que las bacterias sean más difíciles de eliminar. Este estudio planteó una pregunta simple pero importante: ¿podemos medir de manera fiable estos genes de resistencia a antibióticos en las aguas superficiales y utilizar esa información para entender hasta qué punto la actividad humana afecta incluso a los paisajes más protegidos?
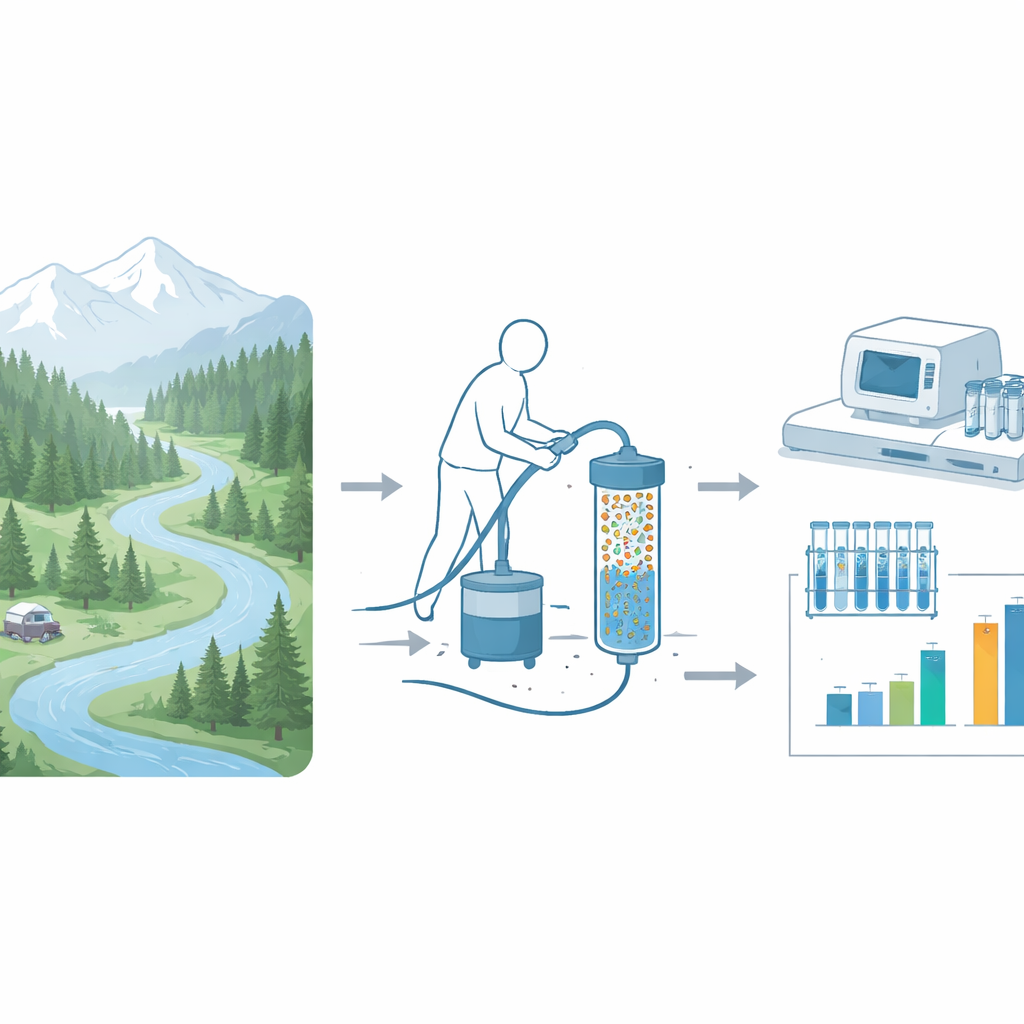
Buscando señales de alerta en el agua que fluye
Los antibióticos salvan vidas, pero su uso intensivo en medicina y agricultura ha ayudado a que las bacterias desarrollen defensas. Esas instrucciones defensivas están escritas en el ADN como genes de resistencia a antibióticos. Cuando las personas o los animales eliminan bacterias, o cuando las aguas residuales llegan a los ríos, estos genes pueden propagarse por el medio ambiente, a veces llegando a lugares que parecen prístinos. Científicos y gestores de tierras públicas necesitan formas de monitorear estas señales genéticas en lagos y arroyos para detectar cambios temprano y juzgar si son causados por el uso de visitantes, contaminación histórica o procesos naturales de fondo.
Construyendo una prueba genética estandarizada
El equipo de investigación desarrolló una placa de ensayo genética única basada en PCR cuantitativa, un método capaz de cuantificar secuencias de ADN específicas. Su panel apuntó a 47 marcadores génicos bacterianos distintos, incluidos muchos genes de resistencia conocidos y algunos destinados a ayudar a rastrear el origen de la contaminación, como humana, aviar o por animales de pastoreo. Diseñaron o adaptaron cuidadosamente los cebadores de ADN —secuencias cortas que le indican a la máquina de PCR qué copiar— y luego comprobaron que cada uno coincidiera realmente con el gen previsto comparándolos con las principales bases de datos de referencia. Para evaluar la fiabilidad de la prueba, la aplicaron a ADN de 41 aislados clínicos bacterianos y compararon los resultados con el secuenciamiento completo del genoma. La concordancia entre la prueba rápida y el secuenciamiento mucho más detallado fue extremadamente alta, con sensibilidad y especificidad cercanas al 98 por ciento.
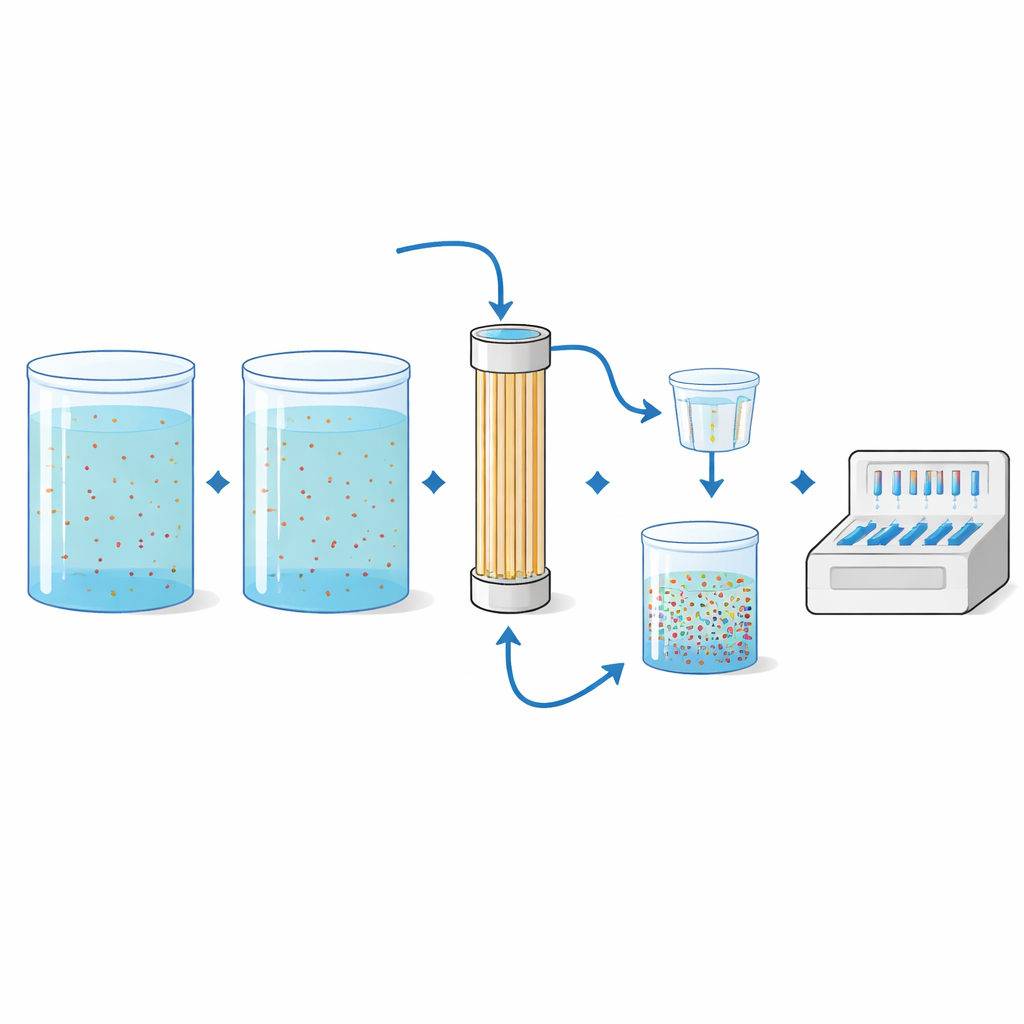
Concentrando señales raras a partir de grandes volúmenes
Los genes de resistencia en arroyos silvestres pueden ser extraordinariamente raros, por lo que el equipo necesitaba una forma de “ampliar” trazas diminutas en mucho volumen de agua. Utilizaron ultrafiltración de fibra hueca, una tecnología tomada de la diálisis y del tratamiento de agua potable. Se bombeaban grandes volúmenes —hasta 50 litros en este estudio— a través de un cartucho lleno de finas fibras huecas que atrapan microorganismos. El material atrapado se enjuagaba luego del filtro, se concentraba adicionalmente en membranas más pequeñas y finalmente se analizaba con el panel de PCR. En ensayos controlados de laboratorio, los científicos contaminaron agua estéril con bacterias conocidas que llevaban ocho genes de resistencia distintos a varias concentraciones y volúmenes. El método detectó de manera fiable muchos de los genes añadidos, especialmente cuando se filtraron volúmenes de agua mayores, y las proporciones medidas de genes de resistencia respecto al ADN bacteriano total coincidieron estrechamente con las expectativas.
Lo que los parques de Alaska pueden revelar
Con este enfoque, el equipo se orientó a tres parques nacionales de Alaska que difieren en la afluencia de visitantes: Denali, Kenai Fjords y Wrangell–St. Elias. En cada parque muestrearon dos arroyos, uno cercano a campamentos, carreteras o antiguas minas y otro en una ubicación más remota. De estos arroyos filtraron múltiples muestras de 20 y 50 litros, cultivaron algunas bacterias para probar cuáles podían crecer en presencia de antibióticos y emplearon el panel de PCR junto con el secuenciamiento de marcadores bacterianos generales para ver cómo se distribuían los genes de resistencia y las comunidades microbianas en general. En los seis sitios detectaron con alta confianza 19 genes de resistencia distintos. Algunos, como genes vinculados a antibióticos comunes como las sulfonamidas y las tetraciclinas, estuvieron bastante extendidos, mientras que otros asociados a fármacos hospitalarios potentes aparecieron en solo unas pocas muestras.
Huella humana en arroyos fríos y claros
El parque con mayor afluencia de visitantes, Denali, mostró la mayor variedad de genes de resistencia en conjunto. Sin embargo, el arroyo que destacó más por la abundancia de ADN resistente fue Exit Creek en Kenai Fjords National Park, que fluye debajo de un concurrido centro de visitantes y punto de inicio de senderos. Allí, la proporción de genes de resistencia respecto al ADN bacteriano total fue significativamente más alta que en cualquier otro sitio muestreado. En contraste, Wrangell–St. Elias, con muchos menos visitantes, mostró menos tipos de genes de resistencia, y algunos patrones apuntaron a otras influencias como la minería histórica del cobre. La mayoría de los grupos bacterianos identificados por el secuenciamiento amplio no eran patógenos humanos clásicos, y solo un aislado cultivado de todos los sitios mostró resistencia clara en pruebas de laboratorio tradicionales, lo que subraya que muchos genes de resistencia pueden residir en microbios ambientales más que en bacterias claramente causantes de enfermedad.
Qué significa esto para la protección de personas y parques
Este trabajo muestra que es posible usar una combinación estandarizada y apta para el campo de filtración de gran volumen y pruebas genéticas dirigidas para monitorear genes de resistencia a antibióticos en aguas superficiales, incluso donde la contaminación es baja. Al comparar tanto la frecuencia de aparición de genes de resistencia como su abundancia, los gestores pueden empezar a distinguir entre los niveles naturales de fondo y la influencia humana probable debida a visitantes, aguas residuales o contaminación heredada. Aunque la presencia de genes de resistencia por sí sola no demuestra una amenaza sanitaria inmediata, su seguimiento a lo largo del tiempo ofrece un sistema de alerta temprana y una forma de evaluar cuánto están protegiendo los parques tanto a los ecosistemas como a las comunidades aguas abajo en un mundo donde la resistencia a los antibióticos es una preocupación creciente.
Cita: Scott, L.C., Ahlstrom, C.A., Woksepp, H. et al. Validation and application of a standardized quantitative PCR assay for the assessment of antimicrobial resistance genes in surface water. Sci Rep 16, 11597 (2026). https://doi.org/10.1038/s41598-026-35635-x
Palabras clave: resistencia antimicrobiana, aguas superficiales, parques nacionales, monitoreo por qPCR, calidad del agua