Clear Sky Science · de
Validierung und Anwendung eines standardisierten quantitativen PCR-Tests zur Erfassung von Antibiotikaresistenzgenen in Oberflächengewässern
Warum winzige Gene in wilden Gewässern wichtig sind
Wenn Sie durch einen Nationalpark wandern und klare, rauschende Bäche sehen, wirken sie unberührt. Doch selbst in abgelegenen Gebieten können mikroskopische Spuren unserer Antibiotika als Gene auftauchen, die Bakterien schwerer zu töten machen. Diese Studie stellte eine einfache, aber wichtige Frage: Können wir diese Antibiotikaresistenzgene in Oberflächengewässern zuverlässig messen und die gewonnenen Daten nutzen, um zu verstehen, wie stark menschliche Aktivität sogar unsere am stärksten geschützten Landschaften beeinflusst?
Auf Warnzeichen im fließenden Wasser achten
Antibiotika retten Leben, aber ihr intensiver Einsatz in Medizin und Landwirtschaft hat Bakterien geholfen, Abwehrmechanismen zu entwickeln. Diese Anweisungen sind in der DNA als Antibiotikaresistenzgene kodiert. Wenn Menschen oder Tiere Bakterien ausscheiden oder Abwasser in Flüsse gelangt, können sich diese Gene in der Umwelt verbreiten und manchmal an scheinbar unberührten Orten landen. Wissenschaftler und Betreiber von Schutzgebieten brauchen Möglichkeiten, diese genetischen Warnsignale in Seen und Bächen zu überwachen, damit sie Veränderungen früh erkennen und beurteilen können, ob Besucherbetrieb, historische Verschmutzung oder natürliche Hintergrundprozesse die Ursache sind.
Entwicklung eines standardisierten Gentests
Das Forschungsteam entwickelte eine einzelne Testplatte auf Basis quantitativer PCR, einer Methode, die bestimmte DNA-Sequenzen zählen kann. Ihr Panel richtete sich gegen 47 verschiedene bakterielle Genmarker, darunter viele bekannte Resistenzgene und einige Marker, die helfen, die Herkunft von Kontaminationen nachzuverfolgen, etwa Mensch, Vogel oder Weidetiere. Sie entwarfen oder passten sorgfältig DNA-Primer an – kurze Sequenzen, die der PCR mitteilen, was kopiert werden soll – und überprüften anschließend, ob jeder Primer wirklich mit dem beabsichtigten Gen übereinstimmt, indem sie gegen große Referenzdatenbanken verglichen. Um die Zuverlässigkeit des Tests zu prüfen, führten sie ihn an DNA aus 41 klinischen bakteriellen Isolaten durch und verglichen die Ergebnisse mit vollständigen Genomsequenzen. Die Übereinstimmung zwischen dem Schnelltest und der deutlich detaillierteren Sequenzierung war sehr hoch, mit Sensitivität und Spezifität nahe 98 Prozent.
Seltene Signale aus großen Volumina konzentrieren
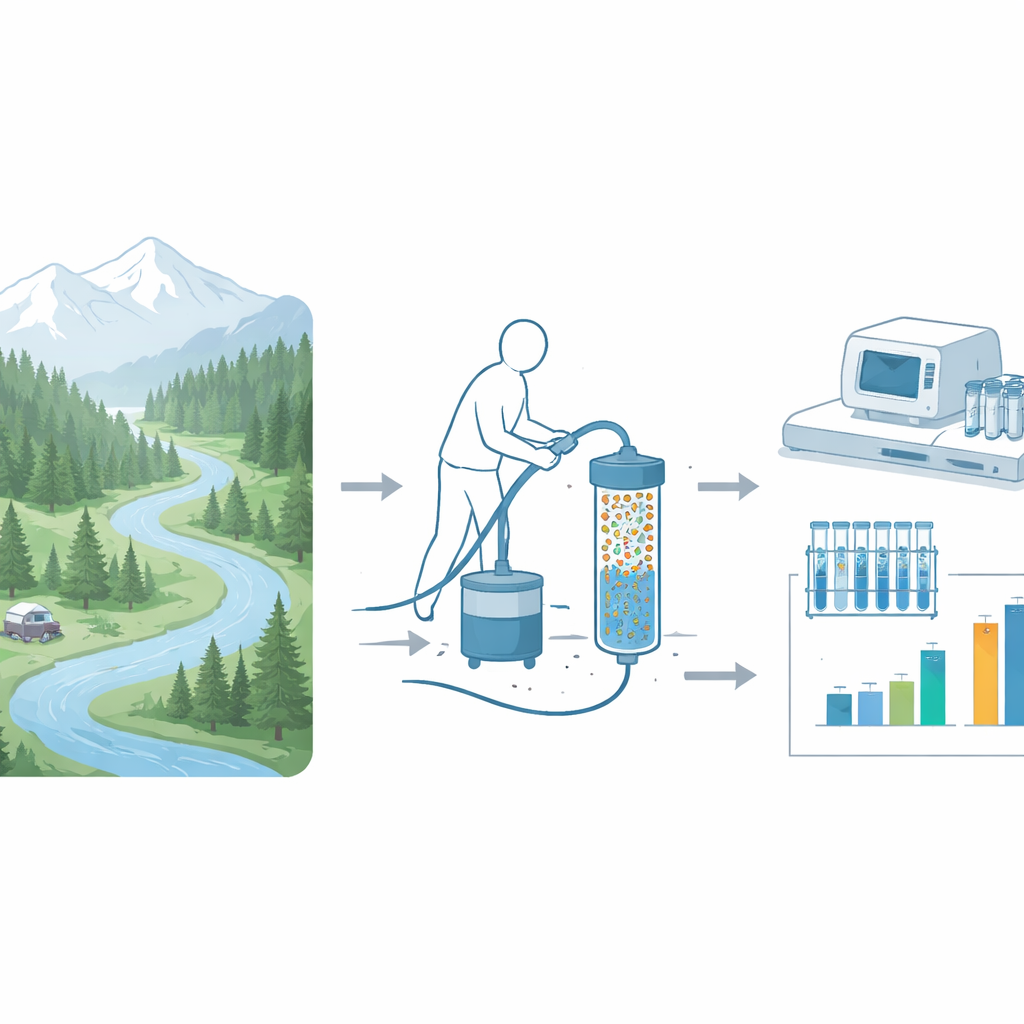
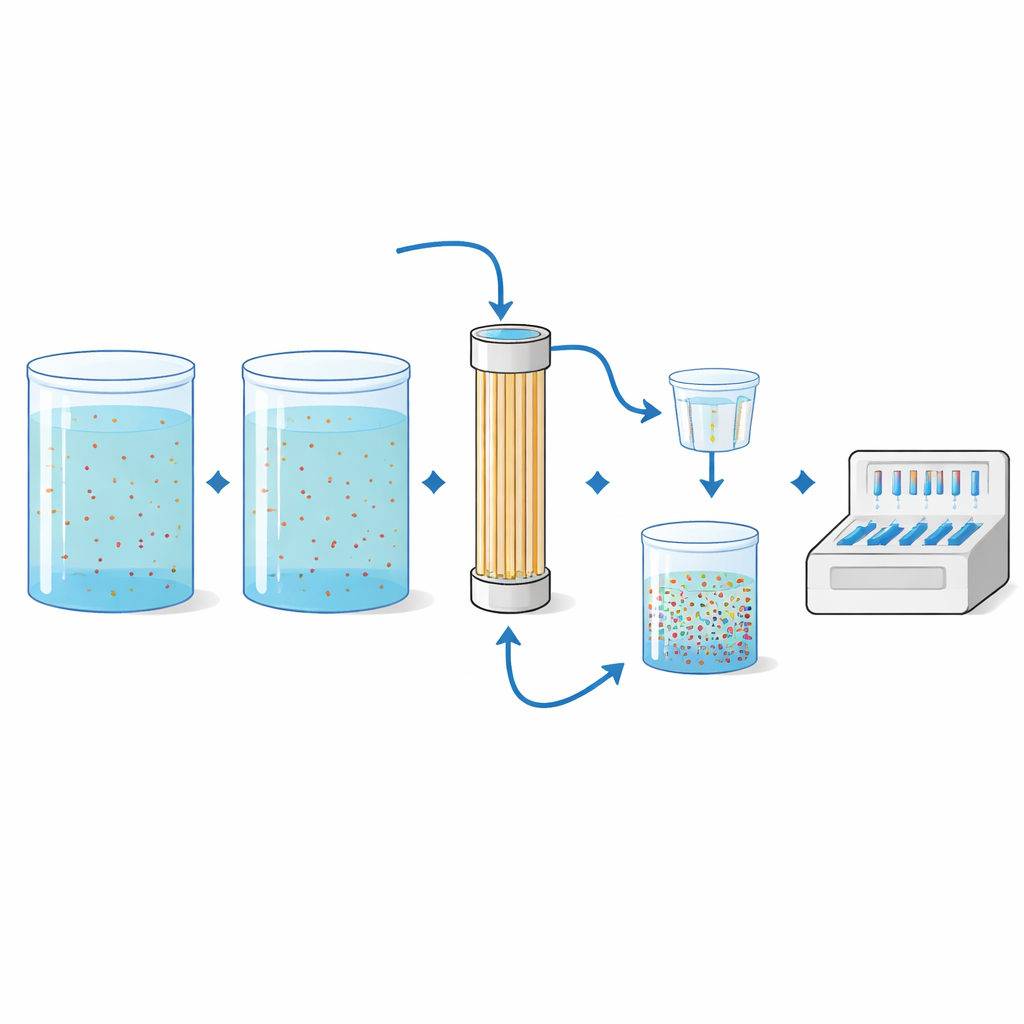
Resistenzgene in wilden Bächen können extrem selten sein, deshalb benötigte das Team eine Methode, um winzige Spuren in großen Wassermengen „heranzuholen“. Sie verwendeten Hohlfaser-Ultrafiltration, eine Technologie, die aus Dialyse und Trinkwasseraufbereitung entlehnt ist. Große Volumina – in dieser Studie bis zu 50 Liter – wurden durch eine Kartusche mit feinen Hohlfasern gepumpt, die Mikroben zurückhalten. Das zurückgehaltene Material wurde dann vom Filter abgespült, auf kleineren Membranen weiter konzentriert und schließlich mit dem PCR-Panel analysiert. In kontrollierten Labortests versetzten die Wissenschaftler steriles Wasser mit bekannten Bakterien, die acht verschiedene Resistenzgene trugen, in mehreren Konzentrationen und Volumina. Die Methode detektierte viele der zugesetzten Gene zuverlässig, besonders bei größeren filtrierten Wassermengen, und die gemessenen Verhältnisse von Resistenzgenen zu gesamter bakterieller DNA stimmen eng mit den Erwartungen überein.
Was Alaskas Parks verraten können
Mit diesem Ansatz wandte sich das Team drei Nationalparks in Alaska zu, die sich in der Besucherzahl unterscheiden: Denali, Kenai Fjords und Wrangell–St. Elias. In jedem Park entnahmen sie Proben aus zwei Bächen, einem nahe Campingplätzen, Straßen oder alten Bergbauflächen und einem in einer entlegeneren Lage. Aus diesen Bächen filtrierten sie mehrere 20- und 50-Liter-Proben, kultivierten einige Bakterien, um zu testen, welche im Beisein von Antibiotika wachsen konnten, und nutzten das PCR-Panel sowie die DNA-Sequenzierung allgemeiner bakterieller Marker, um zu sehen, wie Resistenzgene und die breitere mikrobielle Gemeinschaft verteilt sind. An allen sechs Standorten detektierten sie mit hoher Zuverlässigkeit 19 verschiedene Resistenzgene. Einige, wie Gene, die mit gängigen Antibiotika wie Sulfonamiden und Tetrazyklinen assoziiert sind, waren relativ weit verbreitet, während andere, die mit starken Krankenhausantibiotika verbunden sind, nur in wenigen Proben auftauchten.
Menschliche Spuren in kalten, klaren Bächen
Der Park mit der höchsten Besucherzahl, Denali, zeigte insgesamt die größte Vielfalt an Resistenzgenen. Doch der Bach mit der höchsten Menge an Resistenz-DNA war Exit Creek im Kenai Fjords National Park, der unterhalb eines belebten Besucherzentrums und Trailheads fließt. Dort war der Anteil von Resistenzgenen im Verhältnis zur gesamten bakteriellen DNA signifikant höher als an allen anderen untersuchten Stellen. Im Gegensatz dazu zeigte Wrangell–St. Elias, mit deutlich weniger Besuchern, weniger Resistenzgen-Typen, und einige Muster deuteten auf andere Einflüsse wie historischen Kupferbergbau hin. Die meisten bakteriellen Gruppen, die durch breite DNA-Sequenzierung identifiziert wurden, waren keine klassischen Humanpathogene, und nur ein einzelnes kultiviertes Isolat aus allen Standorten zeigte in traditionellen Labortests klare Resistenz – ein Hinweis darauf, dass viele Resistenzgene in Umweltmikroben vorkommen können und nicht unbedingt in offensichtlichen krankheitserregenden Bakterien.
Was das für den Schutz von Menschen und Parks bedeutet
Diese Arbeit zeigt, dass es möglich ist, eine standardisierte, feldtaugliche Kombination aus Großvolumenfiltration und zielgerichteter genetischer Analyse zu nutzen, um Antibiotikaresistenzgene in Oberflächengewässern zu überwachen, selbst dort, wo die Kontamination gering ist. Durch den Vergleich sowohl der Häufigkeit des Auftretens als auch der Abundanz von Resistenzgenen können Verantwortliche beginnen, zwischen natürlichem Hintergrundniveau und wahrscheinlichem menschlichem Einfluss durch Besucher, Abwasser oder Altlasten zu unterscheiden. Während das Vorhandensein von Resistenzgenen allein nicht zwangsläufig eine unmittelbare Gesundheitsgefahr beweist, bietet ihre langfristige Überwachung ein Frühwarnsystem und eine Möglichkeit, zu bewerten, wie gut Parks sowohl Ökosysteme als auch nachgelagerte Gemeinden schützen – in einer Welt, in der Antibiotikaresistenz ein wachsendes Problem darstellt.
Zitation: Scott, L.C., Ahlstrom, C.A., Woksepp, H. et al. Validation and application of a standardized quantitative PCR assay for the assessment of antimicrobial resistance genes in surface water. Sci Rep 16, 11597 (2026). https://doi.org/10.1038/s41598-026-35635-x
Schlüsselwörter: Antibiotikaresistenz, Oberflächengewässer, Nationalparks, qPCR-Überwachung, Wasserqualität