Clear Sky Science · es
La red del factor inducible por hipoxia refleja la progresión de la enfermedad renal en la diabetes y la inhibición de los cotransportadores sodio-glucosa
Por qué importa el bajo oxígeno en el riñón
Para millones de personas con diabetes tipo 2, el daño renal se desarrolla silenciosamente durante años antes de que aparezcan los síntomas. Este estudio plantea una pregunta aparentemente sencilla con grandes consecuencias: ¿qué ocurre dentro de las células renales cuando no reciben suficiente oxígeno, y pueden los fármacos modernos para la diabetes ayudar a que esas células vuelvan a un estado saludable? Siguiendo la actividad de cientos de genes controlados por la maquinaria sensora de oxígeno del organismo, los investigadores construyeron un mapa detallado de cómo progresa la enfermedad renal diabética y de cómo una clase de fármacos muy utilizada, los inhibidores de SGLT2, podría ayudar a proteger los riñones.
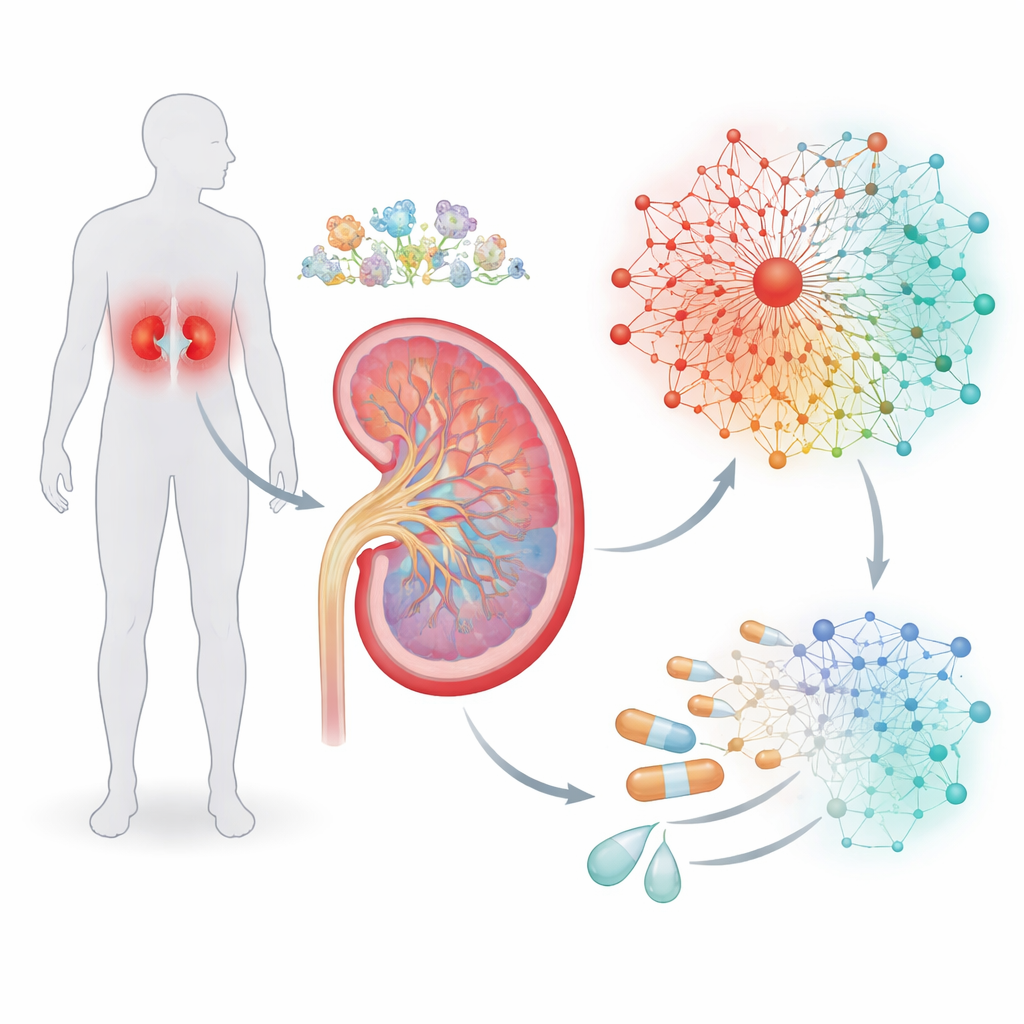
Rastreando el sistema de alarma del oxígeno en el riñón
El riñón es uno de los órganos más activos del cuerpo, filtrando sangre constantemente y ajustando los niveles de sal y agua. Ese trabajo consume mucho oxígeno y, en la diabetes, el equilibrio entre suministro y demanda de oxígeno puede inclinarse hacia un déficit crónico. Las células responden al bajo oxígeno mediante un interruptor maestro llamado factor inducible por hipoxia, o HIF, que activa o reprime muchos otros genes. En lugar de centrarse solo en HIF, los autores revisaron estudios previos para reunir una lista de genes conocidos por reaccionar ante la hipoxia. Usando secuenciación de ARN unicelular de alta resolución a partir de biopsias renales, examinaron en qué partes de la nefrona —los diferentes segmentos y tipos celulares de las unidades filtrantes del riñón— están más activos estos genes sensibles a la hipoxia.
Construyendo una red génica que refleja la enfermedad
Los interruptores génicos rara vez actúan solos, por lo que el equipo preguntó a continuación qué otros reguladores tienden a agruparse con HIF en el ADN. Al escanear las regiones promotoras —los tramos de ADN que controlan si un gen se utiliza— buscaron patrones recurrentes de sitios de unión, como frases gramaticales en una oración. Este análisis puso al descubierto “cassettes” donde los sitios de HIF coexisten con sitios para otras dos familias de factores de transcripción, denominadas KLF y ETS. A partir de estos patrones, los investigadores ensamblaron siete vías de señalización interconectadas que contienen 237 genes, formando una red reguladora impulsada por la hipoxia. De manera importante, datos de un gran proyecto de referencia renal mostraron que la mayoría de estos genes se encuentran en regiones de la cromatina abiertas y accesibles, lo que significa que las células renales están predispuestas a utilizar esta red cuando las condiciones lo requieren.
Señales de alerta tempranas en las células tubulares estresadas
Los investigadores preguntaron entonces si esta red centrada en HIF cambia a medida que avanza la enfermedad renal. Se centraron en las células del túbulo proximal, que afrontan gran parte del trabajo de transporte, con alto consumo energético, y que se ven muy afectadas en la diabetes. Un estado particular de estrés de estas células, denominado túbulo proximal adaptativo (aPT), se ha relacionado con peores resultados a largo plazo. Al comparar las células tubulares sanas con las células aPT, el estudio encontró que casi la mitad de los genes de la red cambiaron su actividad, a menudo acompañados de cambios en el grado de compactación del ADN local. Perturbaciones similares, y de mayor magnitud progresiva, aparecieron cuando examinaron tejido total de personas con enfermedad renal diabética en fases tempranas y tardías, y la transcriptómica espacial confirmó que muchos de estos genes alterados se concentran en regiones de los túbulos que muestran lesión visible.
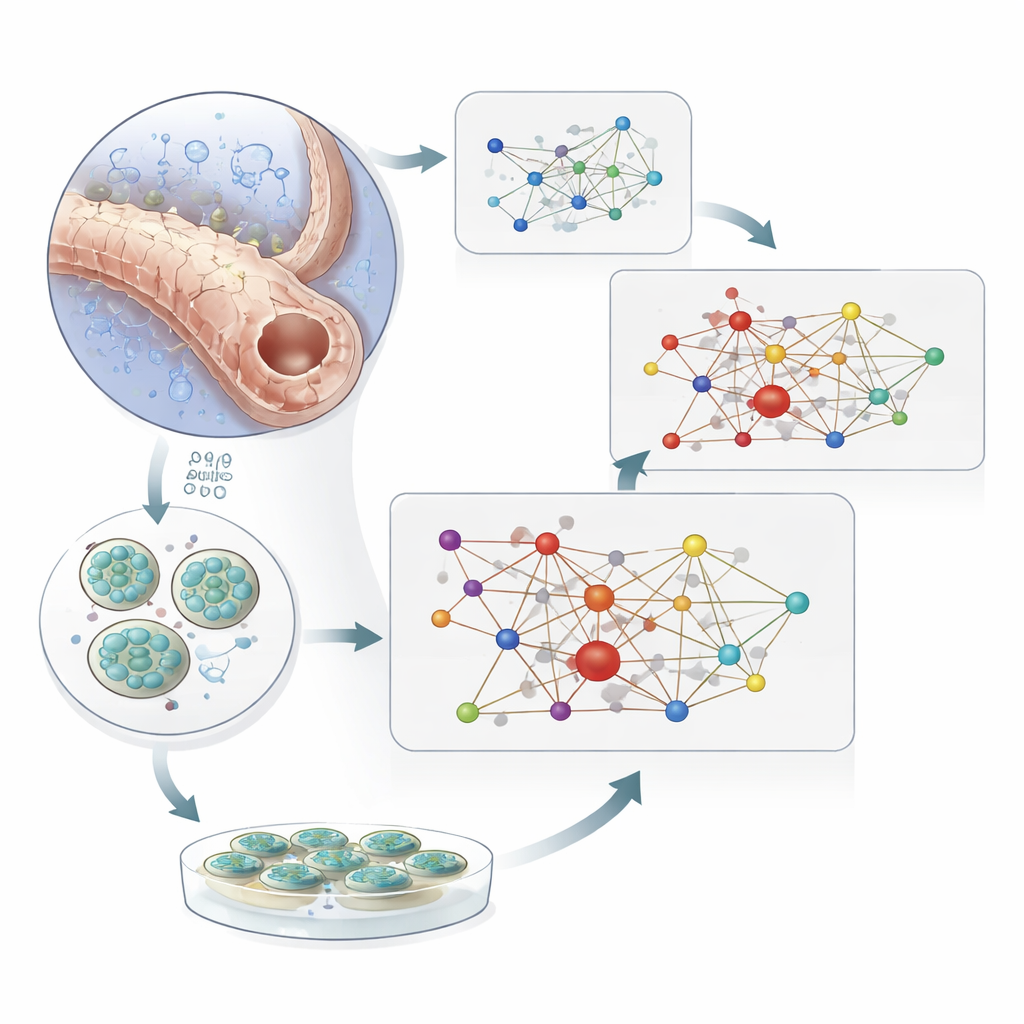
Probando la red en mini-riñones y con fármacos
Para separar causa de consecuencia, el equipo recurrió a organoides renales humanos —modelos renales miniatura cultivados en el laboratorio y derivados de células madre. Cuando estos organoides se expusieron a oxígeno muy bajo, docenas de genes de la red modificaron su expresión, reflejando los patrones observados en tejido humano enfermo. Experimentos en células renales cultivadas con HIF1A y HIF2A silenciados mostraron que muchos de estos cambios dependen directamente de la actividad de HIF. Finalmente, los investigadores analizaron a personas con diabetes tipo 2 que estaban o no tomando inhibidores de SGLT2, fármacos que reducen la carga de trabajo renal al cambiar cómo se manejan el azúcar y la sal en los túbulos. En las células del túbulo proximal de pacientes tratados, más de un tercio de los genes de la red que se habían alejado de niveles sanos volvieron a acercarse a un patrón normal. Cambios protectores similares aparecieron cuando organoides hipóxicos se expusieron a un inhibidor de SGLT2.
Qué significa esto para los pacientes y las terapias
En conjunto, estos hallazgos describen una “firma de estrés por oxígeno” multigénica que se activa tempranamente en los riñones diabéticos, mucho antes de que la cicatrización severa sea evidente al microscopio. En lugar de depender de un marcador único, la red centrada en HIF ofrece una lectura más rica sobre cuánto ha progresado la enfermedad renal y qué tan bien están funcionando las terapias. Los resultados apoyan la idea de que los inhibidores de SGLT2 ayudan a calmar esta red de estrés, lo que podría ralentizar el daño a los túbulos. Aunque el estudio no demuestra que la falta de oxígeno sea el único desencadenante —los cambios metabólicos en la diabetes probablemente también desempeñan un papel—, muestra que monitorizar esta red génica puede ser una forma poderosa de seguir la enfermedad y evaluar nuevos fármacos dirigidos a proteger los riñones del esfuerzo silencioso de la diabetes.
Cita: Nair, V., Minakawa, A., Smith, C. et al. Hypoxia inducible factor network reflects kidney disease progression in diabetes and sodium-glucose co-transporters inhibition. Sig Transduct Target Ther 11, 144 (2026). https://doi.org/10.1038/s41392-026-02653-0
Palabras clave: enfermedad renal diabética, hipoxia, red génica HIF, inhibidores de SGLT2, transcriptómica unicelular