Clear Sky Science · de
Eisenbasierte Ein‑Atom‑Katalysatoren für die selektive Ammoxidation von C(sp3)–H‑Bindungen und oxidative C–C‑Spaltungsreaktionen
Alltägliche Chemikalien in wertvolle Bausteine verwandeln
Chemiker haben sich lange auf toxische Reagenzien und energieintensive Anlagen verlassen, um Nitrile herzustellen – eine Familie kleiner, aber wirkungsvoller funktioneller Gruppen, die in vielen Arzneimitteln und Materialien vorkommen. Diese Studie stellt einen sichereren und effizienteren Weg vor, diese Verbindungen mithilfe eines Katalysators zu erzeugen, der aus einzelnen Eisenatomen besteht, die in einem porösen Kohlenstoffgerüst verankert sind. Durch die Verwendung von gewöhnlicher Luft und Ammoniak unter vergleichsweise milden Bedingungen kann das neue System einfache Kohlenwasserstoff‑Rohstoffe und sogar Plastikabfälle in hochwertige Nitrile umwandeln. Das weist in Richtung saubererer chemischer Produktion und nachhaltigerem Recycling. 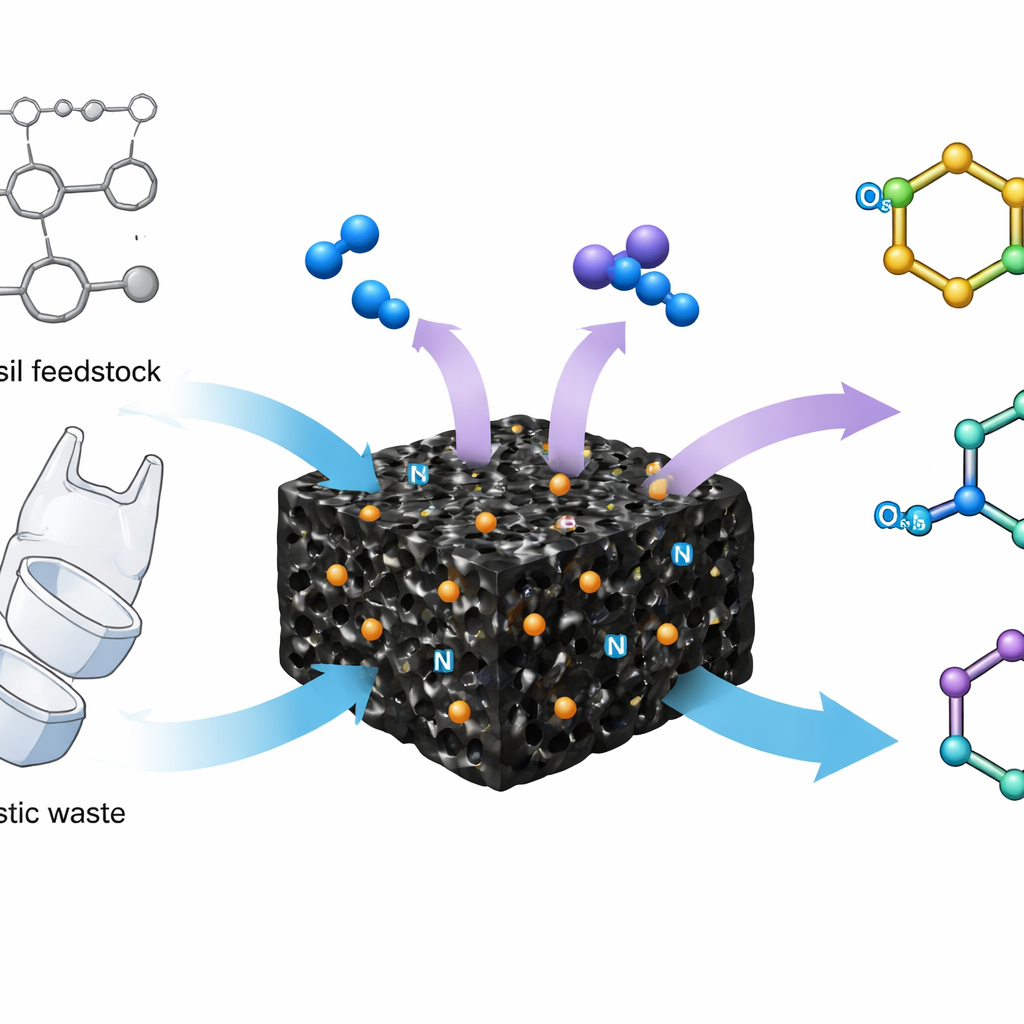
Warum Nitrile im Alltag wichtig sind
Nitrile sind stille Arbeitstiere des modernen Lebens. Die darin enthaltene Cyano‑Gruppe findet sich in mehr als 60 zugelassenen Arzneimitteln, etwa in Mitteln gegen Depressionen, Brustkrebs und Leukämie, sowie in vielen Agrarchemikalien und Spezialmaterialien. Traditionell stellt die Industrie Nitrile durch Reaktionen aromatischer Bausteine mit Cyanidsalzen oder Blausäuregas her. Diese Verfahren sind zwar effizient, aber gefährlich: Sie verwenden hochgiftige Reagenzien und erzeugen große Mengen an giftigen Abfällen. Ein attraktiverer Ansatz ist es, einfache Kohlenwasserstoffe aufzuwerten, indem ihre Kohlenstoff‑Wasserstoff‑Bindungen selektiv mit Sauerstoff oxidiert werden, sodass billige Methylarene und verwandte Moleküle direkt zu Nitrilen werden, ganz ohne Cyanid. Bislang verlangte diese Strategie jedoch seltene Metalle, harte Reaktionsbedingungen oder funktionierte nur für eine enge Palette von Ausgangsstoffen.
Einen Katalysator Atom für Atom entwerfen
Die Autorinnen und Autoren gingen dieses Problem an, indem sie einen heterogenen Katalysator entwarfen, in dem einzelne Eisenatome in einem schwammartigen Kohlenstoffnetzwerk eingebettet sind, das auch Stickstoff und Bor enthält. Anstatt größere Eisenpartikel zu bilden, die weniger selektiv und schwerer zu kontrollieren sein können, verteilt die Herstellungsweise das Eisen als isolierte Zentren, die von Stickstoffatomen umgeben sind; benachbartes Bor stimmt das lokale Umfeld fein ab. Moderne Mikroskopie und Spektroskopie zeigen, dass diese Eisenzentren in einer mikro‑ und mesoporösen Kohlenstoffmatrix sitzen, was eine sehr große Oberfläche und Kanäle bietet, durch die Sauerstoff, Ammoniak und organische Moleküle diffundieren und reagieren können. Messungen zur Sauerstoffspeicherung und ‑aktivierung der Katalysatoren sowie zur Säurestärke ihrer Oberflächen legen nahe, dass die Bor‑Stickstoff‑Ko‑Dotierung die Eisenstellen besonders gut dazu befähigt, die ersten, schwierigen Bindungsbrechungsschritte auszulösen.
Von einfachen Aromaten zu Arzneimitteln und mehr
Getestet an einem Modellsubstrat, 4‑Methylanisol, übertraf der Eisen‑Ein‑Atom‑Katalysator eine breite Palette kommerzieller Edelmetallkatalysatoren und industrieller Materialien und lieferte das entsprechende Nitril in hoher Ausbeute und Selektivität unter Verwendung von wässrigem Ammoniak, Sauerstoff und Wasser als Lösungsmittel. Das Team untersuchte daraufhin die Reaktionsbreite und fand, dass sich mehr als 60 verschiedene Ausgangsstoffe – darunter Toluene, mehrfach substituierte Aromaten und stickstoffhaltige Ringsysteme – in ihre Nitrile umwandeln ließen. Diese Produkte sind wertvolle Zwischenprodukte für Pharma‑ und Pflanzenschutzmittel. Der Katalysator fördert außerdem eine anspruchsvollere Umwandlung: die oxidative Spaltung von Kohlenstoff‑Kohlenstoff‑Bindungen in Alkylarenen. In diesen Fällen werden Seitenketten abgespalten, sodass einfache Benzonitrile entstehen, selbst aus komplexen Ausgangsstoffen wie Lignin‑Modellverbindungen aus Biomasse. 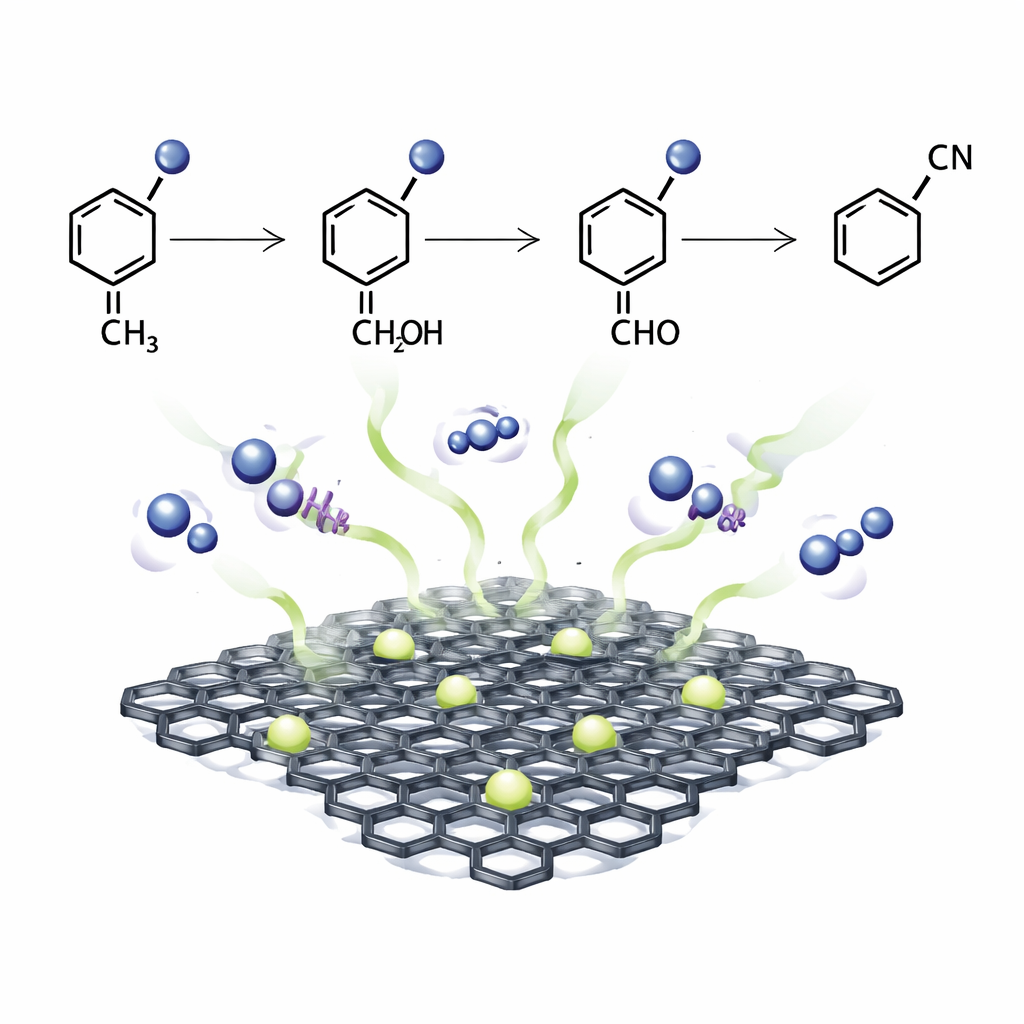
Plastikabfälle in nützliche Moleküle aufwerten
Über Feinchemikalien hinaus kann dieselbe Chemie auch Plastikabfälle aufwerten. Polystyrol und verwandte Copolymere, die häufig in Verpackungen und Schaumstoffen vorkommen, bestehen aus Ketten aromatischer Ringe, die durch C–C‑Bindungen verknüpft sind. Unter den neuen katalytischen Bedingungen brechen diese Polymere zu Benzonitril und Benzamid in brauchbaren Ausbeuten ab, und Größen‑Ausschluss‑Messungen bestätigen, dass die Polymerketten tatsächlich in kleinere Fragmente geschnitten werden. Bemerkenswert ist, dass der Katalysator echten Plastikabfall mit Additiven und Füllstoffen toleriert und in kontinuierlichen Flussreaktoren viele Stunden arbeiten kann, bevor eine Regeneration nötig ist. Eine einfache Behandlung mit verdünnter Wasserstoffperoxidlösung stellt die Ein‑Atom‑Eisenstellen wieder her und belebt die Aktivität, sodass mehrere Wiederverwendungszyklen möglich sind.
Wie der Katalysator seine Arbeit verrichtet
Kontrollversuche und Echtzeit‑spektroskopische Untersuchungen sprechen für einen schrittweisen Mechanismus. Zunächst wird Sauerstoff an den Eisenstellen aktiviert und bildet reaktive Superoxid‑Spezies. Diese Spezies abstrahieren Wasserstoffatome von den benzylichen Positionen des organischen Substrats und erzeugen Radikale, die anschließend zu Aldehyden oder Ketonen weiterverarbeitet werden. In Anwesenheit von Ammoniak bilden diese Zwischenprodukte Imine, die weiter zur Bildung von Nitrilen oxidiert werden. Bei Alkylarenen und Polymeren führt eine ähnliche Abfolge zur Spaltung von C–C‑Bindungen und zur Freisetzung aromatischer Nitrile. Der Schlüssel zu diesem Verhalten ist die einzigartige Anordnung von Eisen, Stickstoff und Bor im porösen Kohlenstoff, die Eisen als hochaktiven Ein‑Atom‑Standort stabilisiert und gleichzeitig inaktive Nanopartikel vermeidet.
Auf dem Weg zu grünerer Chemie und zirkulären Materialien
Im Kern zeigt diese Arbeit, dass sorgfältig entwickelte Ein‑Atom‑Eisenkatalysatoren teureren und gefährlicheren Systemen bei der Herstellung von Nitrilen – einer grundlegenden Funktionsgruppe der chemischen Industrie – ebenbürtig sein oder sie übertreffen können. Durch die Verwendung von reichlich vorhandenem Eisen, Luft und Ammoniak und den Betrieb in Flüssigphasen deutet das Verfahren auf eine sicherere und nachhaltigere Produktion von pharmazeutischen Wirkstoffen und Spezialchemikalien hin. Gleichzeitig zeigt ihre Fähigkeit, ligninähnliche Fragmente und Polystyrolabfälle in wertvolle Nitrile zu verwandeln, wie fortschrittliche Katalyse dazu beitragen könnte, Materialkreisläufe zu schließen und weggeworfenen Kohlenstoff in nützliche Rohstoffe statt in Umweltverschmutzung zu verwandeln.
Zitation: Ma, Z., Rockstroh, N., Chen, Z. et al. Iron-based single-atom catalysts for selective ammoxidation of C(sp3)–H bonds and oxidative C–C cleavage reactions. Nat Catal 9, 389–403 (2026). https://doi.org/10.1038/s41929-026-01513-y
Schlüsselwörter: Ein‑Atom‑Katalyse, grüne Nitril‑Synthese, Aufwertung von Plastik, C–H‑Bindungsaktivierung, Eisenkatalysatoren