Clear Sky Science · de
Das hydrodynamische Drehmoment-Dipol aus rotierenden bakteriellen Flagellen treibt symmetrische Scheiben an
Kleine Schwimmer, die winzige Zahnräder drehen können
Auf den ersten Blick ähnelt eine Wolke schwimmender Bakterien chaotischem Ziellossein. Die Studie zeigt jedoch, dass diese Mikroben unter den richtigen Bedingungen etwas überraschend Geordnetes vollbringen können: Sie bringen vollkommen runde, symmetrische Scheiben dazu, sich in eine vorgegebene Richtung zu drehen, ohne jemals direkt an ihren Rändern zu drücken. Die Arbeit zeigt, wie die Verdrehbewegung bakterieller Schwänze als neuartige mikroskopische Energiequelle genutzt werden kann und welche möglichen Folgen das für intelligente Materialien, winzige Maschinen und das Fortbewegen von Bakterien in engen Räumen in der Natur haben könnte.
Wie Bakterien sich fortbewegen und ihre Umgebung durchmischen
Bewegliche Bakterien wie Escherichia coli treiben sich mit rotierenden Motoren an, die lange, flexible Schwänze – Flagellen – in Rotation versetzen. Auf der Größenskala von wenigen Mikrometern verhält sich Wasser wie zäher Sirup: Nichts gleitet einfach weiter, und um sich fortzubewegen, muss eine Zelle ständig auf die Flüssigkeit drücken. Jahrelang beschrieben Physiker schwimmende Mikroben hauptsächlich danach, wie sie Fluid entlang ihrer Bewegungsrichtung ziehen oder schieben; dieses Bild erklärt Effekte wie die erhöhte Diffusion von benachbarten Teilchen und sogar „superfluid“-ähnliches Verhalten dichter mikrobieller Suspensionen. Diese Standardauffassung vernachlässigt jedoch weitgehend ein anderes Merkmal der Bewegung: Weil das Flagellenbündel in eine Richtung rotiert und der Zellkörper in die entgegengesetzte, um das Gesamtdrehmoment auszugleichen, wirkt jede Bakterienzelle auch wie ein winziges Paar gegenrotierender Rührer.
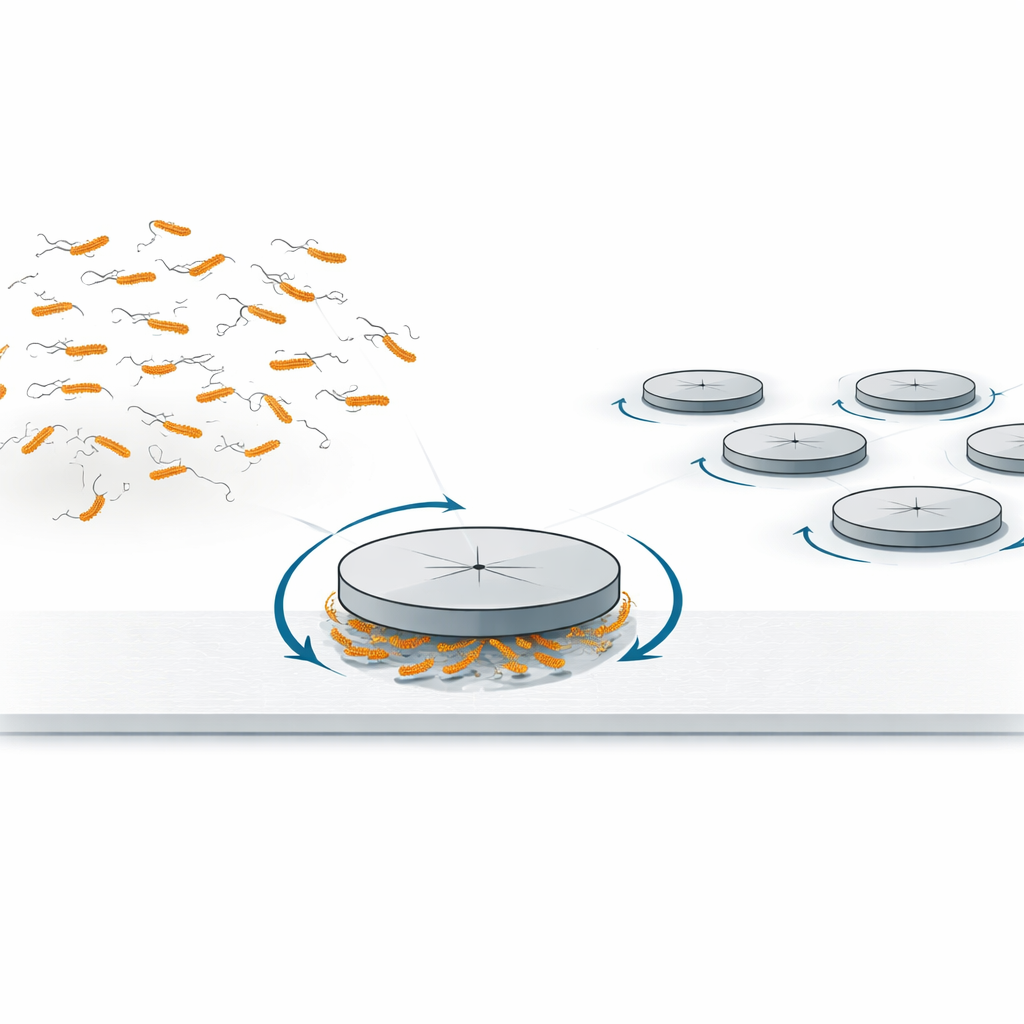
Von zufälligen Zusammenstößen zu kontrolliertem Drehmoment
Die Autorinnen und Autoren untersuchten zunächst einen bekannteren Effekt: Wenn glatte Scheiben, oder „Pucks“, auf der Bodenwand einer schmalen Glaszelle platziert wurden, die mit einer dichten Suspension schwimmender Bakterien gefüllt war, führten Zusammenstöße der Bakterien mit den Scheibenrändern zu einer langsamen Drehung der Pucks im Uhrzeigersinn. Dieses Verhalten war bereits bei unregelmäßig geformten Aggregaten beobachtet worden und lässt sich damit erklären, dass E. coli in der Nähe einer festen Oberfläche natürlicherweise auf gekrümmten, im Uhrzeigersinn verlaufenden Bahnen schwimmen. Diese gekrümmten Trajektorien führen zu geringfügig mehr Stößen in einer Drehrichtung als in der anderen und erzeugen so ein schwaches Nettodrehmoment am Umfang der Scheibe. Das Team maß, wie die Drehgeschwindigkeit von der Scheibengröße abhängt, und zeigte, dass sie sich im erwarteten Maßstab für diesen Rand-Kollisionsmechanismus verändert, womit bestätigt wird, dass einfache Stöße schwimmender Bakterien symmetrische Objekte in Rotation versetzen können.
Einzelne Bakterien unter einer Scheibe einsperren
Um eine subtilere Bewegungsquelle zu untersuchen, nutzten die Forschenden hochauflösendes 3D-Drucken, um Scheiben mit schmalen Untergrundkanälen zu formen, die nur wenige Mikrometer hoch und breit waren. In einem Design endeten vier kurze radiale Kammern knapp vor der Scheibenmitte; in einem anderen führte ein gerader Kanal quer durch die Scheibe und war an beiden Enden offen. Diese Strukturen waren nach unten ausgerichtet, sodass Bakterien, die entlang der Bodenfläche schwammen, gelegentlich eintreten und unter einem Puck eng eingeschlossen werden konnten. Weil die Kanäle so schmal waren, konnten sich Bakterien nicht leicht umdrehen oder an den Wänden vorbeigleiten, um einfach an einem Sackgassenende zu drücken. Sobald jedoch eine einzelne Zelle eine radiale Kammer betrat, stieg die Drehfrequenz der Scheibe um eine Größenordnung an — stets in derselben (Uhrzeigersinn-)Richtung — und nahm weiter zu, wenn mehr Kammern gefüllt wurden. Selbst wenn die Kanäle an beiden Enden offen waren — es gab also keine Wand, gegen die gedrückt werden konnte — erzeugte das Durchqueren einer einzelnen Bakterienzelle quer durch die Scheibe eine charakteristische „runter–hoch“-Änderung im Winkel der Scheibe: Zuerst drehte sie sich in die eine Richtung und dann in die andere, als die Zelle austrat. Entscheidend ist, dass dieses Muster nicht davon abhängt, ob das Bakterium von links nach rechts oder von rechts nach links schwamm, womit einfaches Schieben als Ursache ausgeschlossen ist.
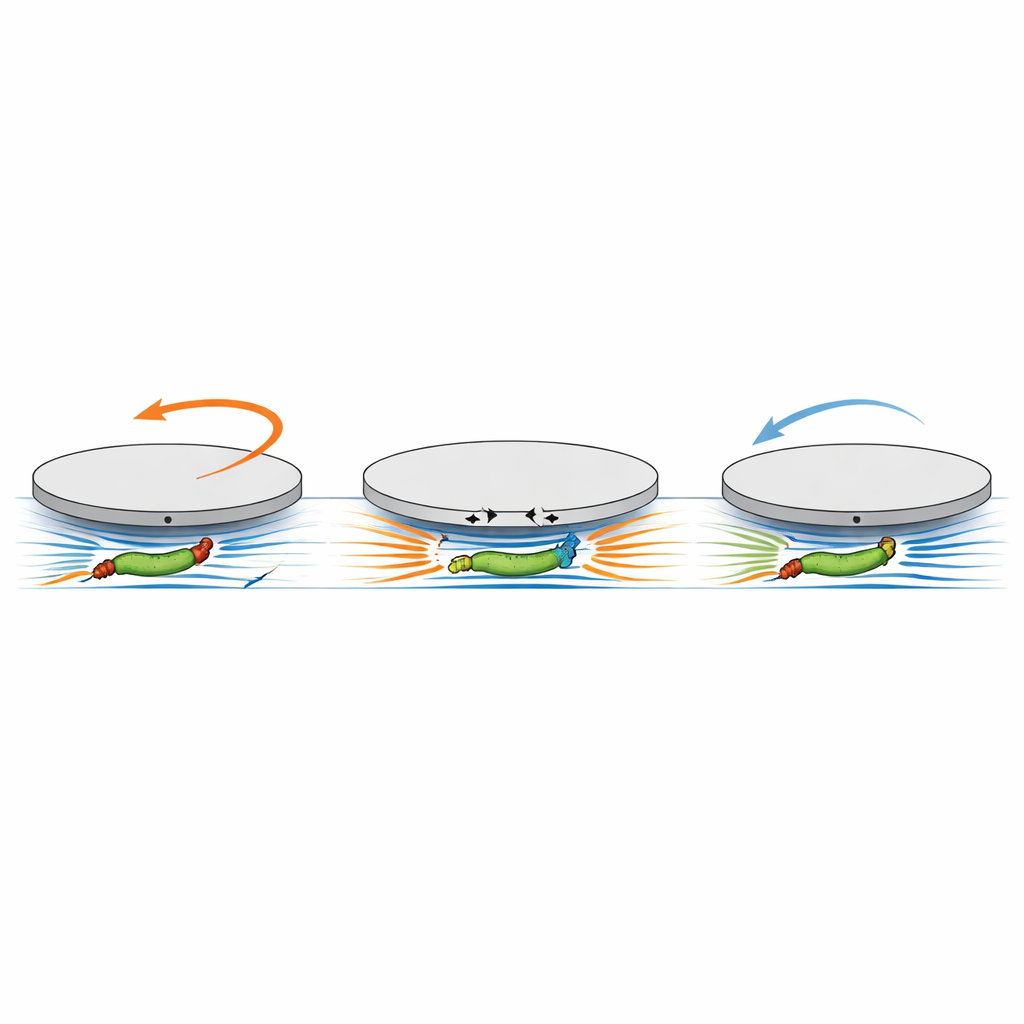
Ein verborgener Drehmoment, der die Scheibe greift
Um diese rätselhaften Beobachtungen zu erklären, entwickelten die Forschenden ein hydrodynamisches Modell, das sich auf die Verdrehungs- statt auf die geradlinige Wirkung des bakteriellen Motors konzentriert. Im Modell werden der rotierende Zellkörper und das gegenrotierende Flagellenbündel als zwei winzige Quellen rotationsbehafteter Bewegung im Fluid behandelt, die durch einen Abstand getrennt sind, der mit der Zelllänge vergleichbar ist. Wenn dieses Paar in einem schmalen Kanal direkt unter der Scheibe liegt, erzeugen die rotierenden Strömungen an der oberen Wand des Kanals — der Unterseite der Scheibe — Scherkräfte in entgegengesetzte Richtungen an leicht versetzten Positionen. Weil diese beiden Zugmuster entlang des Kanals versetzt sind, löschen sie sich nicht vollständig aus. Stattdessen addieren sie sich zu einem Nettodrehmoment, das dazu neigt, die gesamte Scheibe in Drehung zu versetzen. Die Rechnungen zeigen, dass dieses Drehmoment unabhängig von der Schwimmrichtung der Zelle ist und mit dem effektiven Abstand zwischen Körper und Flagellen skaliert, der wiederum mit der Zelllänge zunimmt. Das Modell reproduziert sowohl die anfängliche Drehung im Uhrzeigersinn, wenn Körper und Flagellen gemeinsam unter der Scheibe liegen, als auch die spätere Umkehr, wenn beim Verlassen der Zelle nur noch einer von beiden im Kanal verbleibt.
Auf dem Weg zu chiralen Flüssigkeiten und mikrobiellen Maschinen
Durch den Vergleich von Messungen mit ihrem Modell kommen die Autorinnen und Autoren zu dem Schluss, dass die rotierenden Motoren von E. coli als „Drehmoment-Dipole“ wirken, die Verdrehungsbewegung durch ein Fluid auf nahe Objekte übertragen können, ohne direkten Kontakt oder Formasymmetrie. Die Begrenzung — hier die schmalen Kanäle unter den Scheiben — wandelt diese lokale Verdrehung in einen persistenten, gerichteten Drehimpuls um. Wenn viele solche Pucks in einem bakteriellen Bad platziert werden, können sie eine Ansammlung identischer Rotoren bilden, die alle in dieselbe Richtung drehen — ein Schritt in Richtung „chiral“er Flüssigkeiten, deren makroskopisches Verhalten von einem globalen Drehsinn abhängt. Über die neue Möglichkeit hinaus, mikroskopische Maschinen zu entwerfen, die von lebenden Zellen angetrieben werden, könnte dieser Mechanismus überall dort eine Rolle spielen, wo Bakterien mit rotierenden Flagellen sich durch dichte oder poröse Umgebungen bewegen — etwa Böden, Biofilme oder technische Filter — und so ihre eigene Navigation subtil mit der Bewegung ihrer Umgebung koppeln.
Zitation: Grober, D., Dhar, T., Saintillan, D. et al. The hydrodynamic torque dipole from rotary bacterial flagella powers symmetric discs. Nat. Phys. 22, 620–627 (2026). https://doi.org/10.1038/s41567-026-03189-4
Schlüsselwörter: bakterielle Beweglichkeit, Microfluidik, aktive Materie, Mikroschwimmer, Mikroroboter