Clear Sky Science · zh
神经元APOE4诱导的海马早期网络过度兴奋性在阿尔茨海默病发病机制中的作用
为何焦躁的脑回路不可忽视
许多人携带一种常见的基因变体APOE4,这会大幅提升他们在未来数十年内发展为阿尔茨海默病的风险,往往在症状出现前就已经存在。然而,在那些相对“安静”的年岁里,大脑内部到底发生了什么,一直不清楚。本研究在小鼠中使用精密的电生理记录和基因工具,表明APOE4使大脑中特定的记忆回路在生命早期变得过度活跃且不稳定,远早于记忆问题出现。理解这一早期阶段可能为预防提供窗口,而不必等到损伤广泛扩散后再介入。
记忆枢纽中的早期电风暴
研究者聚焦于海马体——一个对形成记忆和空间映射至关重要的海马形结构。在携带人类APOE4的小鼠中,他们在动物自由移动时记录了大脑的电活动,寻找短暂的大幅度爆发称为发作间期棘波(interictal spikes),这是过度兴奋网络的标志,常见于癫痫及阿尔茨海默病患者。年轻的APOE4小鼠在两个海马区域——CA3和齿状回——中显示出比携带低风险APOE3形式的对照小鼠更多此类事件。邻近的CA1区域则相对安静。值得注意的是,CA3和齿状回早期棘波的数量能预测同一批小鼠数月后在空间学习任务中的表现更差,将早期网络过度活跃性与未来记忆衰退联系了起来。
易激越且更小的脆弱神经元
为查明驱动这种过度兴奋的原因,团队将海马切片,并测量单个神经元对注入电流的反应。在年轻的APOE4小鼠中,CA3锥体细胞及一部分齿状颗粒细胞比APOE3小鼠对应细胞更容易且更频繁放电。这些神经元需要更少的电流即可触发放电,反应更快,放电增益更陡峭,均为内在过度兴奋性的标志。同时,它们在形态上更小:电容测量与直接显微镜观察均显示细胞表面积和体积减少。体积较小的神经元通常具有更高的输入电阻,因此输入信号对膜电位的推动更显著,更容易被触发。在年龄较大的APOE3小鼠中,神经元逐渐“追上”——它们也变得更小和更易激发——这提示APOE4加速了一种类似于衰老的过程,而非创造了全新的病理机制。
当兴奋与抑制的平衡失衡
神经回路依赖兴奋信号(推动活动)与抑制信号(抑制活动)之间的微妙平衡。研究者通过记录进入CA3和齿状回神经元的微小自发电流来检查这种平衡。在年轻APOE4小鼠中,CA3细胞接收到额外的兴奋性输入,而抑制保持稳定,使兴奋—抑制比上倾,进一步放大了它们的过度兴奋。在齿状回中,随年龄增长情况发生了变化:兴奋驱动保持相似,但APOE4小鼠的抑制性输入减少,这与先前显示的某些抑制性中间神经元逐渐丧失的研究一致。这种制动力量的逐步下降使齿状回在较老的APOE4动物中持续过度兴奋,恰好在它们记忆表现恶化时长期存在。
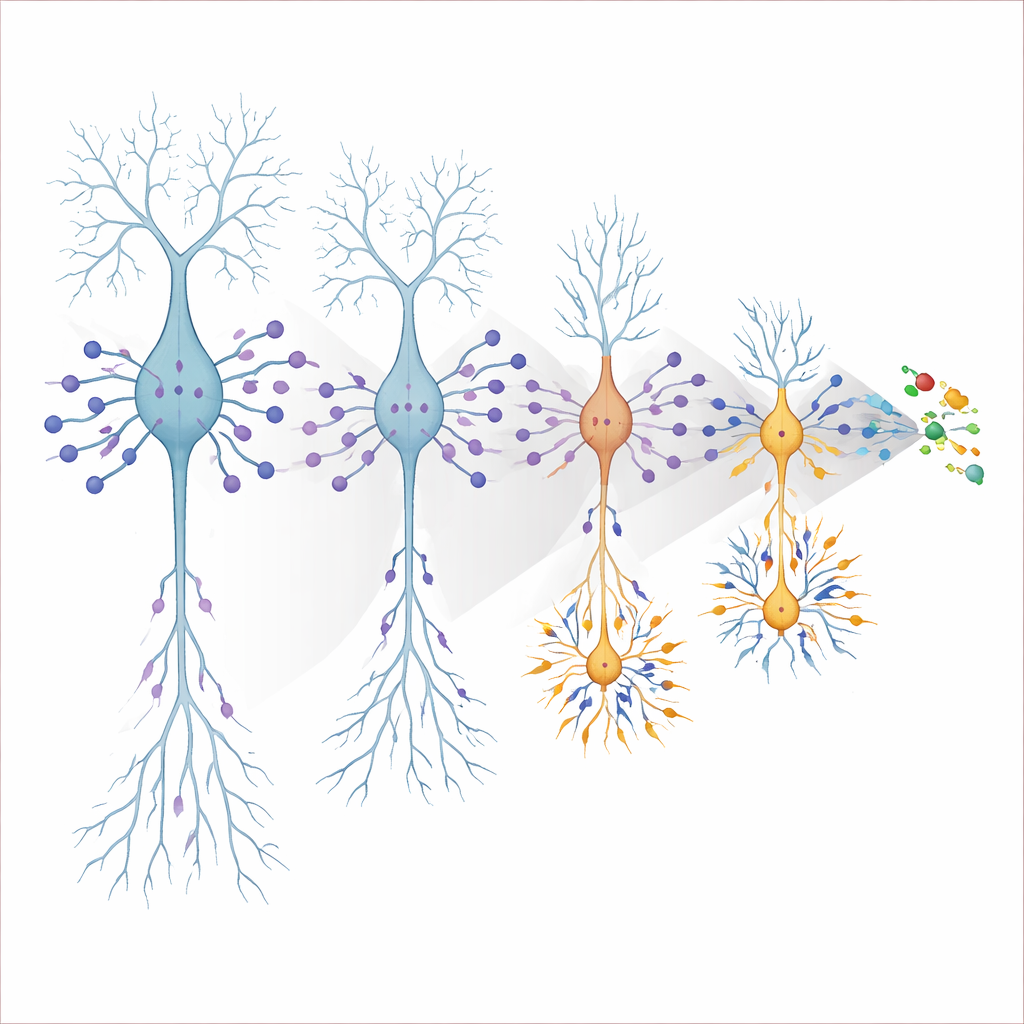
神经元自身产生的APOE4的有害作用与新的分子嫌疑人
APOE常被认为是由星形胶质细胞产生的支持性蛋白,但处于应激状态的神经元也能生成APOE。通过选择性地仅在神经元中删除APOE4,作者证明了这一来源至关重要:从神经元中去除APOE4完全使它们的体积和放电行为正常化,而从胶质细胞中去除则对兴奋性影响甚微。为锁定下游的分子效应子,他们对不同年龄和细胞类型进行了单核RNA测序,然后筛选出表达与早期过度兴奋状态相对应的基因。其中一个突出者是Nell2,这是一种先前与神经元生长和突触相关的蛋白,在人类阿尔茨海默病的大脑和脑脊液中水平升高。采用CRISPR干扰方法下调APOE4神经元中的Nell2,团队能够使这些细胞体积增大并将其放电回落至接近正常,而不改变邻近细胞——这是强有力的证据,表明过量的Nell2有助于将APOE4的存在转化为结构性缩小和电生理过度活跃。
对未来阿尔茨海默病预防的意义
综合来看,结果描绘出一条事件链:神经元内的APOE4在特定海马细胞中提升Nell2及其他基因的表达;这些神经元缩小并变得过度兴奋;CA3和齿状回的局部回路进入长期过度活跃状态;随着时间推移,抑制性细胞减少,网络的制动系统失效,最终导致记忆问题。对于携带APOE4的人来说,这表明有害变化可能在症状出现前多年就已开始,此时若针对网络过度兴奋性或像Nell2这样的分子进行干预,仍可能保护脆弱回路。与其将阿尔茨海默病仅视为晚年斑块与缠结的累积,这项工作更强调它是一种早期、微妙的回路不稳定性疾病——若足够早干预,或许可以将其稳定下来。
引用: Tabuena, D.R., Jang, SS., Grone, B. et al. Neuronal APOE4-induced early hippocampal network hyperexcitability in Alzheimer’s disease pathogenesis. Nat Aging 6, 886–904 (2026). https://doi.org/10.1038/s43587-026-01096-0
关键词: APOE4, 海马过度兴奋性, 阿尔茨海默病, 齿状回, Nell2