Clear Sky Science · ar
الفرط المبكر في نشاط الشبكة الحُصَينِيَّة الناتج عن APOE4 في مَرَض ألزهايمر
لماذا تهم الدوائر الدماغية المضطربة
يحمل العديد من الأشخاص متغيراً جينياً شائعاً يُدعى APOE4 يزيد بشكل كبير من خطر إصابتهم بمرض ألزهايمر، وغالباً قبل عقود من ظهور الأعراض. ومع ذلك، بقي ما يحدث داخل الدماغ خلال تلك السنوات الهادئة غامضاً. تستخدم هذه الدراسة تسجيلات وأدوات جينية متقدمة في الفئران لتُظهر أن APOE4 يجعل دوائر الذاكرة المحددة في الدماغ تصبح مفرطة النشاط وغير مستقرة في وقت مبكر من الحياة، قبل بروز مشاكل الذاكرة بوقت طويل. وفهم هذه المرحلة المبكرة قد يفتح نافذة للوقاية بدلاً من الانتظار حتى يكون الضرر واسع النطاق.
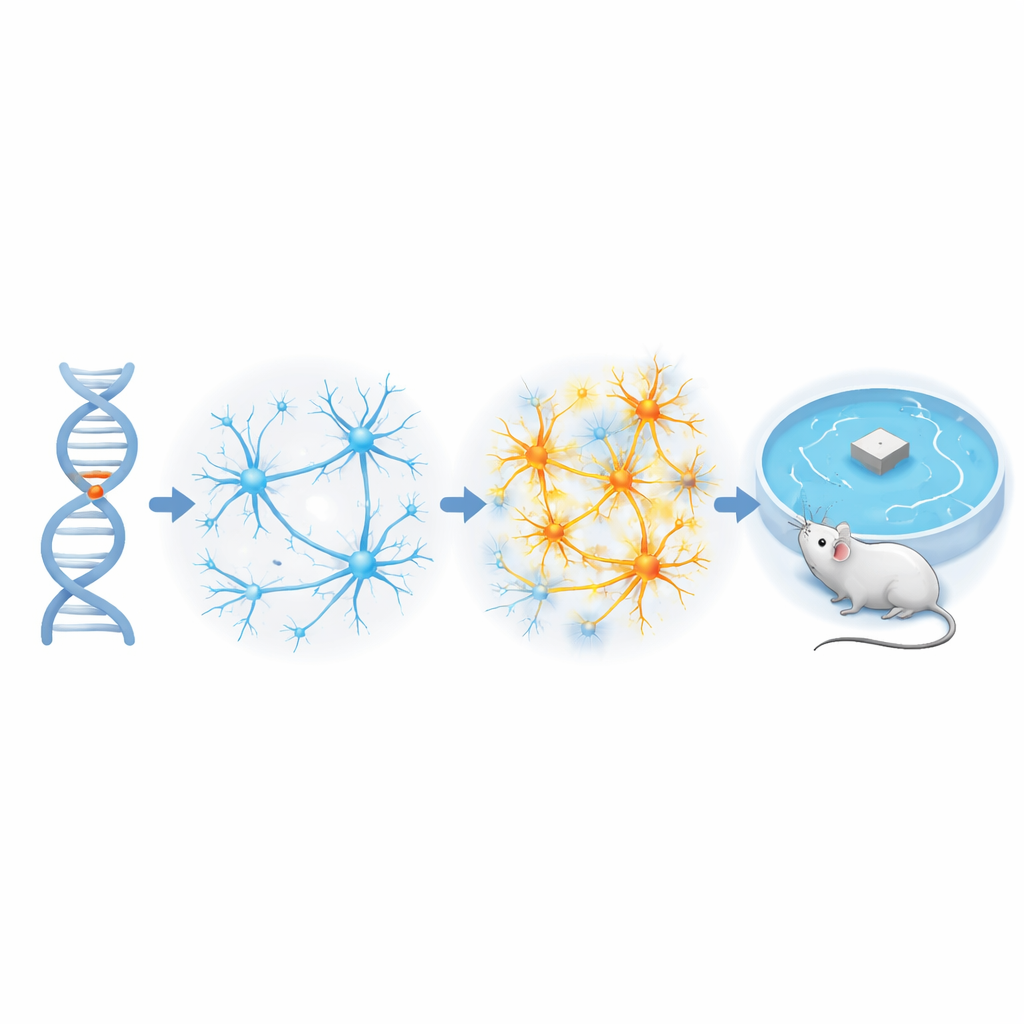
عواصف كهربائية مبكرة في مراكز الذاكرة
ركز الباحثون على الحُصين، البُنية المُشَبَّهة بالفرس البحري والمهمة لتكوين الذكريات ورسم الخرائط المكانية. في فئران مُهندَسة لتحمل APOE4 البشري، سجّلوا النشاط الكهربائي للدماغ بينما كانت الحيوانات تتحرك بحرية. بحثوا عن اندفاعات قصيرة ذات سعة عالية تُعرف بالذبذبات بين النوبات (interictal spikes)، وهي علامة على شبكات مفرطة الإثارة تُرى غالباً في الصرع وفي أشخاص مصابين بألزهايمر. أظهرت فئران APOE4 الشابة عدداً أكبر بكثير من هذه الأحداث في منطقتين من الحصين، تُدَعيان CA3 واللولب السني (dentate gyrus)، مقارنة بفئران الضبط الحاملة للشكل الأقل خطراً APOE3. أما المنطقة المجاورة CA1 فبقيت هادئة نسبياً. ومن اللافت أن عدد الذبذبات المبكرة في CA3 واللولب السني تنبأ بمدى تدهور أداء نفس الفئران في مهمة تعلم مكانية بعد عدة أشهر، رابطاً بين فرط نشاط الشبكة المبكر وتراجع الذاكرة المستقبلي.
خلايا عصبية أصغر وأكثر قابلية للنشاط في الدوائر الضعيفة
لكشف ما يقود هذا الفرط في النشاط، قَسَم الفريق الحصين وقيَس كيف تستجيب الخلايا العصبية المفردة لتيارات محقونة. في فئران APOE4 الشابة، كانت خلايا الحرشفية في CA3 وجزء من خلايا الحبيبة في اللولب السني تُطلق نبضات أسهل وبوتيرة أعلى مقارنةً بتلك في فئران APOE3. هذه الخلايا احتاجت تياراً أقل لتوليد نبضة، استجابت أسرع، وأظهرت منحنى إطلاق أعلى حدةً—كلها علامات على فرط إثارة جوهري. في الوقت نفسه، كانت أصغر جسدياً: أظهرت قياسات السعة الكهربائية والمجهر تقلصاً في مساحة السطح والحجم الخلوي. الخلايا الأصغر تميل إلى مقاومة دخلٍ أعلى، لذلك تؤثر الإشارات الواردة على التغير في الجهد بقوة أكبر، مما يجعلها أسهل في التنشيط. في فئران APOE3 الأكبر سناً، «لحقت» الخلايا تدريجياً—فأصبحت هي أيضاً أصغر وأكثر إثارة—مما يوحي بأن APOE4 يسرّع عملية تشبه الشيخوخة بدلاً من خلق عملية جديدة بالكامل.
عندما يفشل التوازن بين إشارات التشغيل والإيقاف
تعتمد الدوائر العصبية على توازن دقيق بين الإشارات المنشطة التي تحفز النشاط والإشارات المثبطة التي تكبحه. فحص الباحثون هذا التوازن بتسجيل تيارات عفوية صغيرة واردة إلى خلايا CA3 والحبيبة. في فئران APOE4 الشابة، تلقت خلايا CA3 مدخلاً إضافياً إثارياً بينما ظل التثبيط مستقراً، مما أمال نسبة الإثارة إلى التثبيط صعوداً وزاد من تضخيم فرط نشاطها. في اللولب السني، تغيرت الصورة مع التقدم في العمر: بقي الدفع الإثاري مشابهاً، لكن الدخل المثبط انخفض في فئران APOE4، وهو ما يتوافق مع أعمال سابقة أظهرت خسارة تدريجية لأنواع معينة من الخلايا الوصلية المثبطة هناك. أدى هذا الانخفاض التدريجي في قوة الكبح إلى إبقاء اللولب السني في حالة فرط إثارة مستمرة لدى الحيوانات الأكبر سناً الحاملة لـAPOE4، تماماً حينما تدهورت قدرتها على الذاكرة.
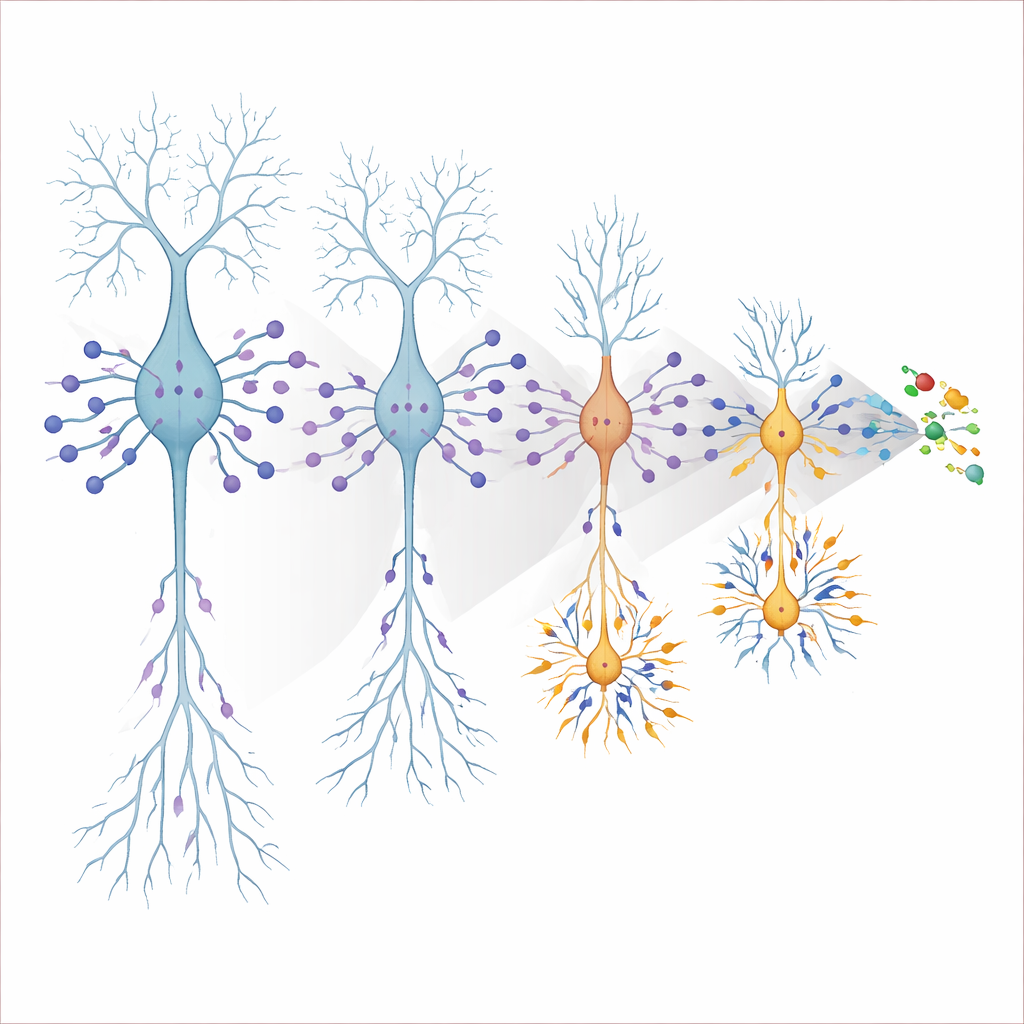
دور ضار لـAPOE4 المنتج داخل الخلايا العصبية ومشتبه جزيئي جديد
غالباً ما يُنظر إلى APOE كبروتين داعم تصنعه الخلايا الدبقية النجمية، لكن الخلايا العصبية المتوترة يمكن أن تصنعه أيضاً. بحذف APOE4 اختيارياً في الخلايا العصبية فقط، أظهر المؤلفون أن هذا المصدر العصبي كان حاسماً: إزالة APOE4 من الخلايا العصبية أعادت حجمها وسلوك إطلاقها إلى الوضع الطبيعي تماماً، بينما كان لإزالته من الخلايا الدبقية تأثير ضئيل على القابلية للإثارة. لتحديد لاعبين جزيئيين تابعين، أجروا تسلسل الحمض النووي الريبي للنووية المفردة عبر الأعمار والأنواع الخلوية، ثم صفّوا الجينات التي تغاير تعابيرها مع الحالة المبكرة المفرطة الإثارة. برز من بين النتائج جين Nell2، وهو بروتين رُبط سابقاً بنمو الخلايا العصبية والمشابك وُجدت مستوياته مرتفعة في دماغ وحَوَل السائل الشوكي لدى البشر المصابين بألزهايمر. باستخدام نهج مقاطعة CRISPR لتقليل Nell2 في خلايا APOE4 العصبية، استطاع الفريق تكبير هذه الخلايا وتهدئة إطلاقها باتجاه الوضع الطبيعي، دون تغيير الخلايا المجاورة—دليل قوي على أن فرط Nell2 يساهم في تحويل وجود APOE4 إلى انكماش بنيوي وفرط نشاط كهربائي.
ماذا يعني هذا لوقاية ألزهايمر في المستقبل
إجمالاً، ترسم النتائج سلسلة من الأحداث: يعزز APOE4 العصبي Nell2 وتغييرات جينية أخرى في خلايا حصينية محددة؛ تنكمش تلك الخلايا وتصبح مفرطة الإثارة؛ تدخل الدوائر المحلية في CA3 واللولب السني حالة نشاط مفرط طويلة الأمد؛ مع مرور الوقت تُفقد الخلايا المثبطة ويعجز نظام الفرملة في الشبكة، ما يؤدي في نهاية المطاف إلى مشاكل الذاكرة. بالنسبة للحاملين لـAPOE4، يشير ذلك إلى أن التغيرات الضارة قد تبدأ سنوات قبل الأعراض، عندما قد يحمي استهداف فرط النشاط الشبكي أو جزيئات مثل Nell2 الدوائر الضعيفة. بدلاً من النظر إلى ألزهايمر كمجرد تراكم متأخر لللوحات والتشابكات، يبرز هذا العمل أنه اضطراب من عدم استقرار دائري مبكر ودقيق—يمكن أن يُستتَسَنَخ إذا تدخلنا في وقت مبكر بما فيه الكفاية.
الاستشهاد: Tabuena, D.R., Jang, SS., Grone, B. et al. Neuronal APOE4-induced early hippocampal network hyperexcitability in Alzheimer’s disease pathogenesis. Nat Aging 6, 886–904 (2026). https://doi.org/10.1038/s43587-026-01096-0
الكلمات المفتاحية: APOE4, فرط الإثارة في الحصين, مرض ألزهايمر, اللولب السني (dentate gyrus), Nell2