Clear Sky Science · it
L’iperattività precoce indotta da APOE4 nei neuroni nell’ippocampo nella patogenesi della malattia di Alzheimer
Perché i circuiti cerebrali irrequieti sono importanti
Molte persone portano una variante genica comune chiamata APOE4 che aumenta notevolmente il rischio di sviluppare la malattia di Alzheimer, spesso decenni prima della comparsa dei sintomi. Tuttavia, ciò che avviene realmente nel cervello durante quegli anni silenziosi è rimasto per lo più oscuro. Questo studio utilizza registrazioni sofisticate e strumenti genetici nei topi per mostrare che APOE4 rende specifici circuiti della memoria nel cervello iperattivi e instabili precocemente nella vita, molto prima che emergano problemi di memoria. Capire questa fase iniziale potrebbe aprire una finestra per la prevenzione, invece di aspettare che il danno sia ormai diffuso.
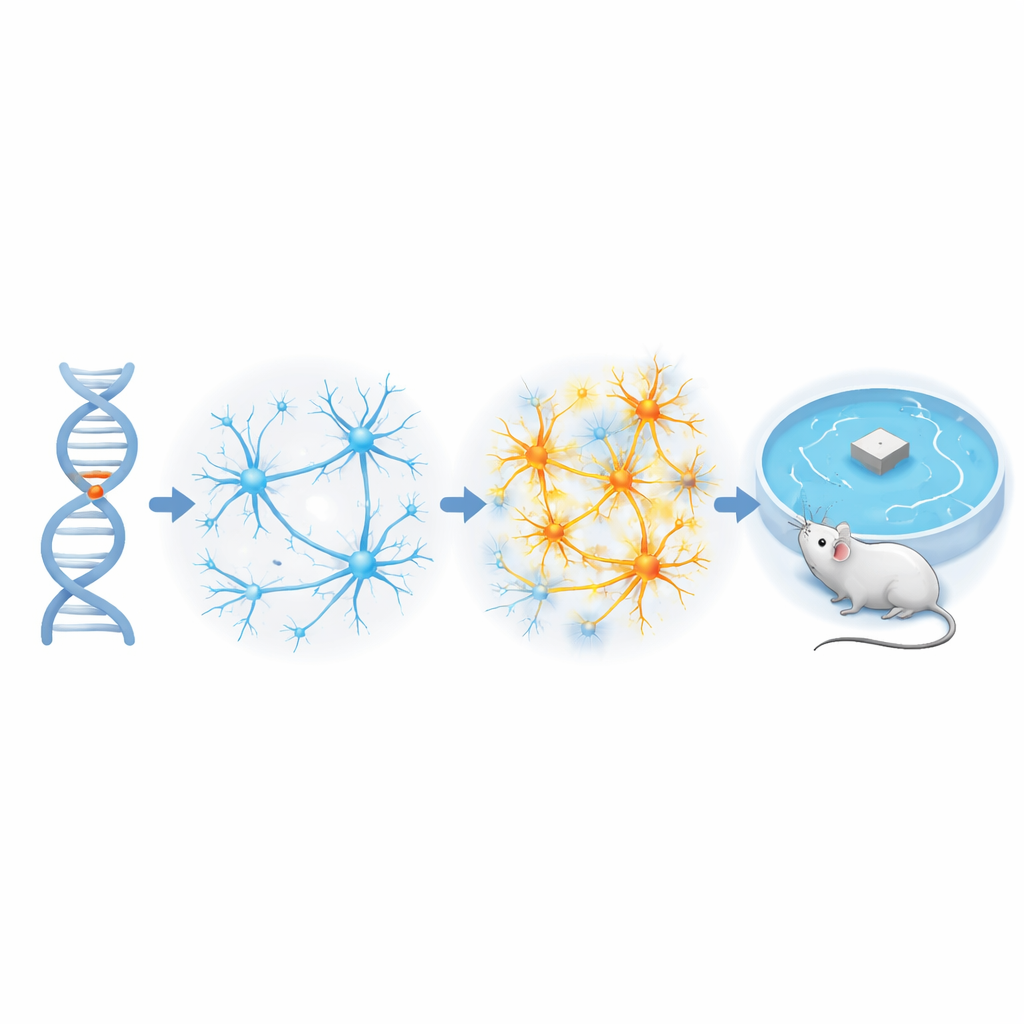
Tempeste elettriche precoci negli snodi della memoria
I ricercatori si sono concentrati sull’ippocampo, una struttura a forma di cavalluccio marino cruciale per formare ricordi e mappare lo spazio. In topi ingegnerizzati per portare l’APOE4 umano, hanno registrato l’attività elettrica del cervello mentre gli animali si muovevano liberamente. Hanno cercato brevi raffiche ad alta ampiezza note come spike interictali, un segnale tipico di reti iper‑eccitabili spesso osservato nell’epilessia e nelle persone con Alzheimer. I giovani topi APOE4 mostravano molti più di questi eventi in due regioni ippocampali, chiamate CA3 e giro dentato, rispetto ai topi di controllo portatori della forma a rischio inferiore APOE3. Una regione vicina, CA1, è rimasta relativamente tranquilla. In modo sorprendente, il numero di spike precoci in CA3 e nel giro dentato prevedeva quanto male gli stessi topi si sarebbero comportati in un compito di apprendimento spaziale molti mesi dopo, collegando l’iperattività di rete precoce al successivo declino della memoria.
Neuroni più piccoli e più reattivi nei circuiti vulnerabili
Per capire cosa guida questa iperattività, il gruppo ha sezionato l’ippocampo e misurato come singoli neuroni rispondessero a correnti iniettate. Nei giovani topi APOE4, le cellule piramidali di CA3 e un sottoinsieme dei granuli del giro dentato si attivavano con maggiore facilità e più frequentemente rispetto a quelle dei topi APOE3. Questi neuroni richiedevano meno corrente per generare spike, rispondevano più rapidamente e avevano una curva di scarica più ripida, tutti segnali di ipereccitabilità intrinseca. Allo stesso tempo, erano fisicamente più piccoli: misure di capacità elettrica e osservazioni microscopiche dirette mostravano una riduzione della superficie e del volume cellulare. I neuroni più piccoli tendono ad avere una resistenza d’ingresso maggiore, perciò i segnali in arrivo fanno variare il loro potenziale in modo più marcato, rendendoli più facili da attivare. Nei topi APOE3 più anziani, i neuroni gradualmente «recuperavano»—anche loro diventavano più piccoli e più eccitabili—suggerendo che APOE4 accelera un processo simile all’invecchiamento piuttosto che crearne uno del tutto nuovo.
Quando l’equilibrio tra segnali di via libera e di stop fallisce
I circuiti neurali si basano su un delicato equilibrio tra segnali eccitatori che promuovono l’attività e segnali inibitori che la frenano. I ricercatori hanno esaminato questo bilanciamento registrando piccole correnti spontanee in ingresso ai neuroni di CA3 e del giro dentato. Nei giovani topi APOE4, le cellule di CA3 ricevevano un input eccitatorio aumentato mentre l’inibizione restava stabile, inclinando verso l’alto il rapporto eccitazione–inibizione e amplificando ulteriormente la loro iperattività. Nel giro dentato, il quadro cambiava con l’età: la spinta eccitatoria restava simile, ma l’input inibitorio diminuiva nei topi APOE4, coerentemente con lavori precedenti che mostrano una perdita graduale di specifici interneuroni inibitori in quella zona. Questo calo progressivo dei freni lasciava il giro dentato persistentemente iperattivo nei topi APOE4 più anziani, proprio quando peggiorava la loro performance mnemonica.
Un ruolo dannoso per l’APOE4 prodotto dai neuroni e un nuovo sospetto molecolare
APOE è spesso considerato una proteina di supporto prodotta dalle cellule gliali a forma stellata, ma anche i neuroni stressati possono sintetizzarla. Eliminando selettivamente APOE4 soltanto nei neuroni, gli autori hanno dimostrato che questa fonte neuronale era cruciale: rimuovere APOE4 dai neuroni normalizzava completamente le loro dimensioni e il loro comportamento di scarica, mentre eliminarlo dalle cellule gliali aveva scarso effetto sull’eccitabilità. Per individuare attori molecolari a valle, hanno eseguito sequenziamento dell’RNA a livello di singolo nucleo attraverso età e tipi cellulari, quindi hanno filtrato i geni la cui espressione seguiva lo stato iper‑eccitabile precoce. Uno spicca: Nell2, una proteina precedentemente collegata alla crescita neuronale e alle sinapsi e trovata a livelli elevati nel cervello e nel liquido spinale di persone con Alzheimer. Usando un approccio CRISPR di interferenza per ridurre Nell2 nei neuroni APOE4, il gruppo è riuscito ad aumentare le dimensioni di queste cellule e a ridurre la loro attività verso valori più normali, senza alterare le cellule vicine—forte evidenza che un eccesso di Nell2 aiuta a convertire la presenza di APOE4 in restringimento strutturale e iperattività elettrica.
Cosa significa per la prevenzione futura dell’Alzheimer
Nel complesso, i risultati delineano una catena di eventi: l’APOE4 neuronale aumenta Nell2 e altri cambiamenti genici in specifiche cellule ippocampali; quei neuroni si rimpiccioliscono e diventano iperattivi; i circuiti locali in CA3 e nel giro dentato entrano in uno stato di sovra‑attivazione duraturo; nel tempo, le cellule inibitorie vengono perse e il sistema di frenata della rete fallisce, culminando in problemi di memoria. Per le persone portatrici di APOE4, ciò suggerisce che cambiamenti dannosi possono iniziare anni prima dei sintomi, quando intervenire sull’iperattività di rete o su molecole come Nell2 potrebbe ancora proteggere i circuiti vulnerabili. Piuttosto che considerare l’Alzheimer esclusivamente come un accumulo tardivo di placche e grovigli, questo lavoro lo mette in luce come un disturbo di instabilità circuitale precoce e sottile—uno stato che potrebbe essere stabilizzato se si interviene abbastanza presto.
Citazione: Tabuena, D.R., Jang, SS., Grone, B. et al. Neuronal APOE4-induced early hippocampal network hyperexcitability in Alzheimer’s disease pathogenesis. Nat Aging 6, 886–904 (2026). https://doi.org/10.1038/s43587-026-01096-0
Parole chiave: APOE4, iperattività ippocampale, malattia di Alzheimer, giro dentato, Nell2