Clear Sky Science · zh
通过克隆和同型选择设计的抗体药物偶联物限制表达CSPG4的三阴性乳腺癌生长
这项研究为何重要
三阴性乳腺癌是乳腺癌中最具侵袭性的一种亚型,缺乏许多用于其他亚型的靶向治疗选择。本研究探索了一种更精确攻击这些肿瘤的新途径,通过构建一种“智能炸弹”式药物,能够定位肿瘤细胞表面的特定标志,同时尽量保护大部分健康组织。对于那些疾病复发或对化疗耐药的患者,这类聚焦治疗可能提供迫切需要的新选项。
在顽固肿瘤细胞上的新标志
研究者将注意力集中在一种名为CSPG4的表面分子上,该分子位于部分癌细胞的外侧。通过分析大量乳腺肿瘤数据库并检查患者组织样本,他们证明CSPG4在三阴性乳腺癌中比在其他乳腺癌类型中更为常见。重要的是,在标准化疗后残留的肿瘤组织中,CSPG4水平保持不变甚至升高,这表明携带该标志的细胞尤其顽强,可能是复发的罪魁祸首。肿瘤中CSPG4水平高的患者预后往往更差,使其成为一个有吸引力的精准药物靶点。
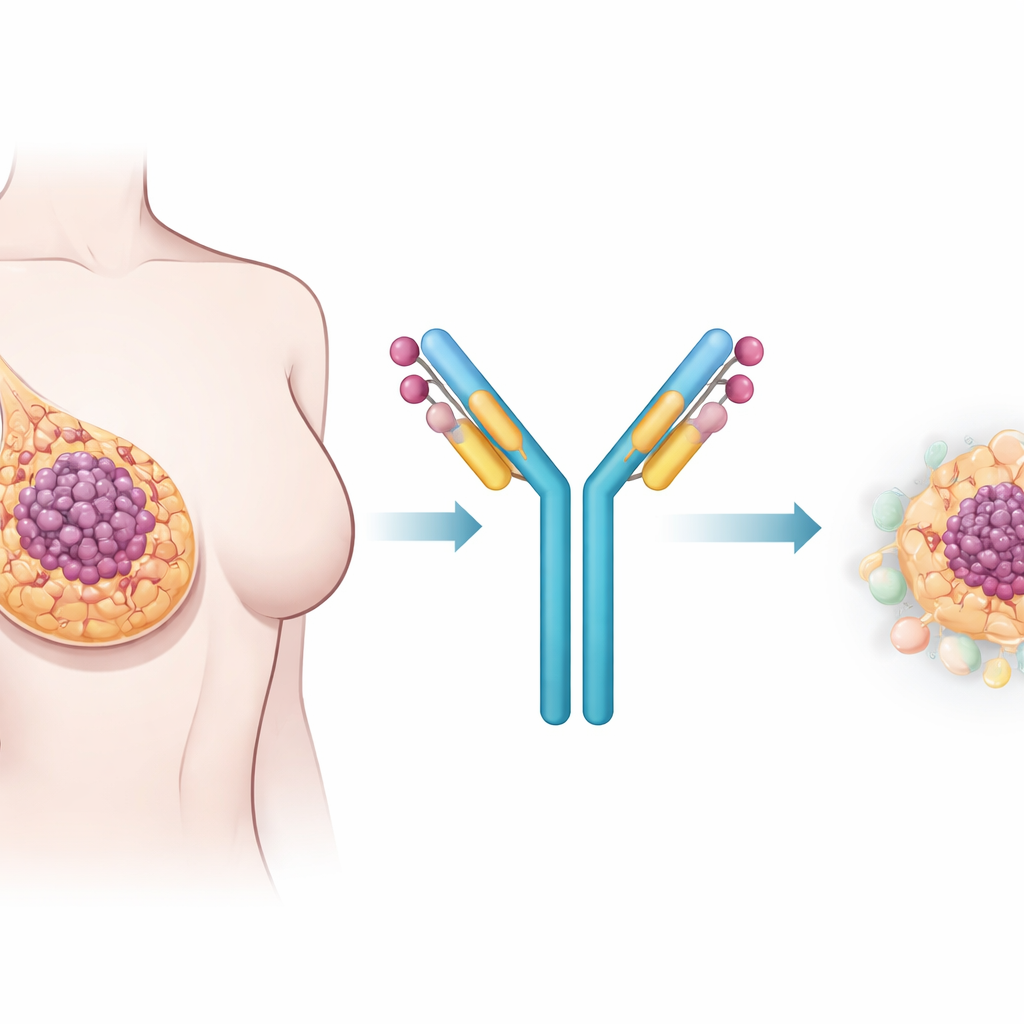
构建制导导弹式药物
为了利用这一标志,团队设计了抗体–药物偶联物(ADC)。这类药物由两部分组成:识别癌细胞上选定靶点的抗体,以及像有效载荷一样连接到抗体上的强效细胞杀伤药物。研究小组比较了三种都能识别CSPG4但结合分子不同位点的抗体,并测试了两种常见的抗体“骨架”——IgG1和IgG4,它们在体内的行为有差异。在细胞培养实验中,一种抗体版本——以IgG1格式的225.28S——表现突出。它对CSPG4的结合力强,能被癌细胞高效摄取,并且在与一种类似化疗的标准有效载荷连接后,比其他候选者更有效地杀死CSPG4阳性的细胞。
升级有效载荷以增强作用
在确定了最佳抗体骨架后,科学家将225.28S IgG1与一种名为DXd的下一代有效载荷配对,DXd是一种已在其他乳腺癌获批疗法中使用的高效药物。他们将偶联物设计为平均每个抗体上连接约八个DXd分子,同时保持结构完整性和纯度。在体外测试中,该ADC能有效进入富含CSPG4的三阴性乳腺癌和黑色素瘤细胞,并显著降低其存活率,而对低CSPG4表达的细胞影响较小。这种特性表明药物的杀伤力主要限制在携带目标的细胞上,这是成功精准药物的关键要求。
在活体疾病模型中的测试
随后团队转向患者来源的异种移植模型,在这种模型中,人类三阴性乳腺肿瘤组织片段被种植在免疫缺陷小鼠的乳腺脂肪垫中。在两种表达CSPG4的独立模型中,使用225.28S IgG1–DXd ADC的治疗在与其他开发中ADC相似的剂量下显著减慢或停止了肿瘤生长,并在未见明显体重下降或毒性迹象的情况下延长了动物的存活。有意思的是,即便仅使用抗体本身而没有药物有效载荷,在小鼠体内存在人类免疫细胞时也能减缓肿瘤生长。这表明抗体不仅可以传递毒性货物,还可能招募免疫系统攻击CSPG4阳性细胞。
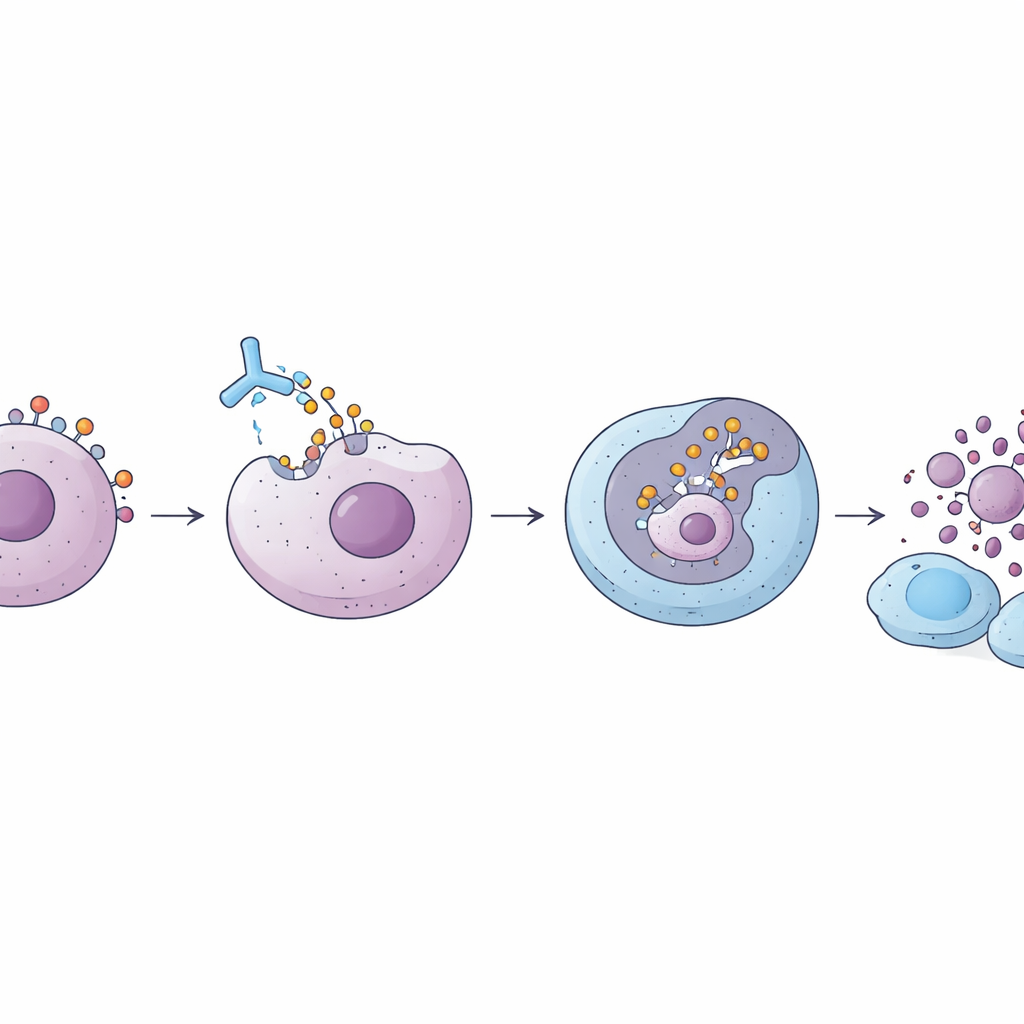
这对未来患者可能意味着什么
总体而言,研究表明CSPG4是化疗耐药三阴性乳腺癌中的有前景标志,并且仔细选择抗体克隆及其结构类型可以显著影响ADC的疗效。优化构建的225.28S IgG1–DXd在现实的临床前模型中缩小了CSPG4阳性肿瘤体积,并在动物中表现出良好的安全性。尽管在将该方法用于人体之前还需大量工作——包括安全性研究、剂量探索和临床试验——这些结果指向一种潜在的新型靶向治疗,可能为当前选择非常有限的一类患者带来希望。
引用: Esapa, B., Liu, Y., Chenoweth, A.M. et al. An antibody-drug conjugate designed through clone and isotype selection restricts the growth of CSPG4-expressing triple-negative breast cancer. npj Precis. Onc. 10, 161 (2026). https://doi.org/10.1038/s41698-026-01341-0
关键词: 三阴性乳腺癌, 抗体药物偶联物, CSPG4, 靶向治疗, 精准肿瘤学