Clear Sky Science · ru
Конъюгат антитело‑лекарство, разработанный путем выбора клона и изотипа, ограничивает рост тройного‑негативного рака молочной железы, экспрессирующего CSPG4
Почему это исследование важно
Тройно‑негативный рак молочной железы — одна из самых агрессивных форм рака молочной железы, и для него отсутствует большинство таргетных методов лечения, доступных при других подтипах. В этом исследовании изучается новый способ более точечной атаки на такие опухоли: создание «умной бомбы», которая нацеливается на специфический маркер на раковых клетках, щадя при этом большую часть здоровой ткани. Для пациентов с рецидивирующим или резистентным к химиотерапии заболеванием такие сфокусированные методы лечения могут предоставить крайне необходимые варианты.
Новый флаг на упорных опухолевых клетках
Исследователи сосредоточились на молекуле на поверхности клеток под названием CSPG4, расположенной на внешней стороне некоторых раковых клеток. Анализ больших наборов данных опухолей молочной железы и исследование образцов тканей пациентов показали, что CSPG4 встречается значительно чаще при тройно‑негативном раке, чем при других типах рака молочной железы. Важно, что уровни CSPG4 оставались неизменными или даже повышались в тканях опухолей, сохранившихся после стандартной химиотерапии, что свидетельствует о том, что клетки с этим маркером особенно устойчивы и могут быть ответственны за рецидив. У пациентов с опухолями с высоким уровнем CSPG4 наблюдались худшие исходы, что делает этот маркер привлекательной мишенью для точечных препаратов.
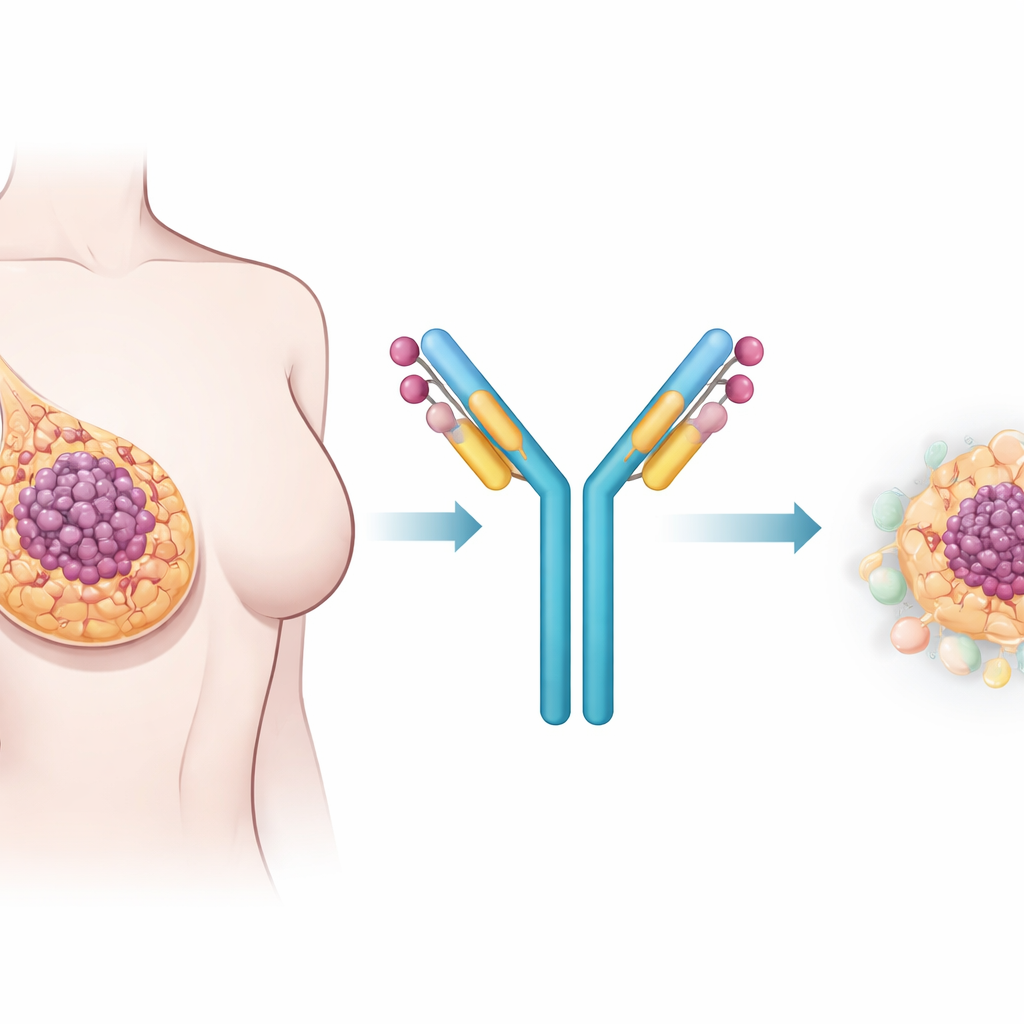
Создание направленного «ракетообразного» лекарства
Чтобы использовать этот маркер, команда разработала конъюгаты антитело‑лекарство (ADC). Это сочетание двух компонентов: антитела, распознающего выбранную цель на раковых клетках, и мощного цитотоксического вещества, связанного с антителом в виде полезной нагрузки. Группа сравнила три различных антитела, распознающих CSPG4, но связывающихся с немного разными участками молекулы. Они также протестировали два распространенных «каркаса» антител — IgG1 и IgG4, которые отличаются поведением в организме. В культурах клеток выделялся один вариант антитела, обозначенный как 225.28S в формате IgG1. Он прочно связывался с CSPG4, эффективно захватывался в раковые клетки и, при соединении со стандартной химиотерапевтической нагрузкой, убивал CSPG4‑положительные клетки значительно эффективнее других кандидатов.
Усиление нагрузки для более сильного эффекта
После определения лучшего антительного каркаса ученые соединили 225.28S IgG1 с новым поколением нагрузки, известной как DXd — высокоактивным веществом, уже применяемым в одобренных препаратах для других подтипов рака молочной железы. Они спроектировали конъюгат так, чтобы в среднем к каждому антителу было прикреплено восемь молекул DXd, сохранив при этом структурную целостность и чистоту. В лабораторных тестах этот ADC эффективно проникал в клетки тройно‑негативного рака молочной железы и меланомы с высоким уровнем CSPG4 и резко снижал их выживаемость, тогда как клетки с низким уровнем CSPG4 подвергались намного меньшему воздействию. Такое поведение указывает на то, что действие препарата в основном ограничено клетками с целевым маркером, что является ключевым требованием для успеха точной медицины.
Испытания в живых моделях сложного заболевания
Затем команда перешла к моделям с ксенотрансплантатами, полученными от пациентов, в которых кусочки человеческих тройно‑негативных опухолей выращивали в молочных жировых подушках иммунодефицитных мышей. В двух независимых моделях с экспрессией CSPG4 лечение ADC 225.28S IgG1–DXd существенно замедляло или останавливалo рост опухоли при дозах, сопоставимых с теми, что используются для других разрабатываемых ADC, и увеличивало выживаемость животных без явной потери веса или признаков токсичности. Интересно, что само антитело без лекарственной нагрузки также могло замедлять рост опухоли при наличии человеческих иммунных клеток у мышей. Это позволяет предположить, что антитело не только доставляет токсическую нагрузку, но и может привлекать иммунную систему для атаки на CSPG4‑положительные клетки.
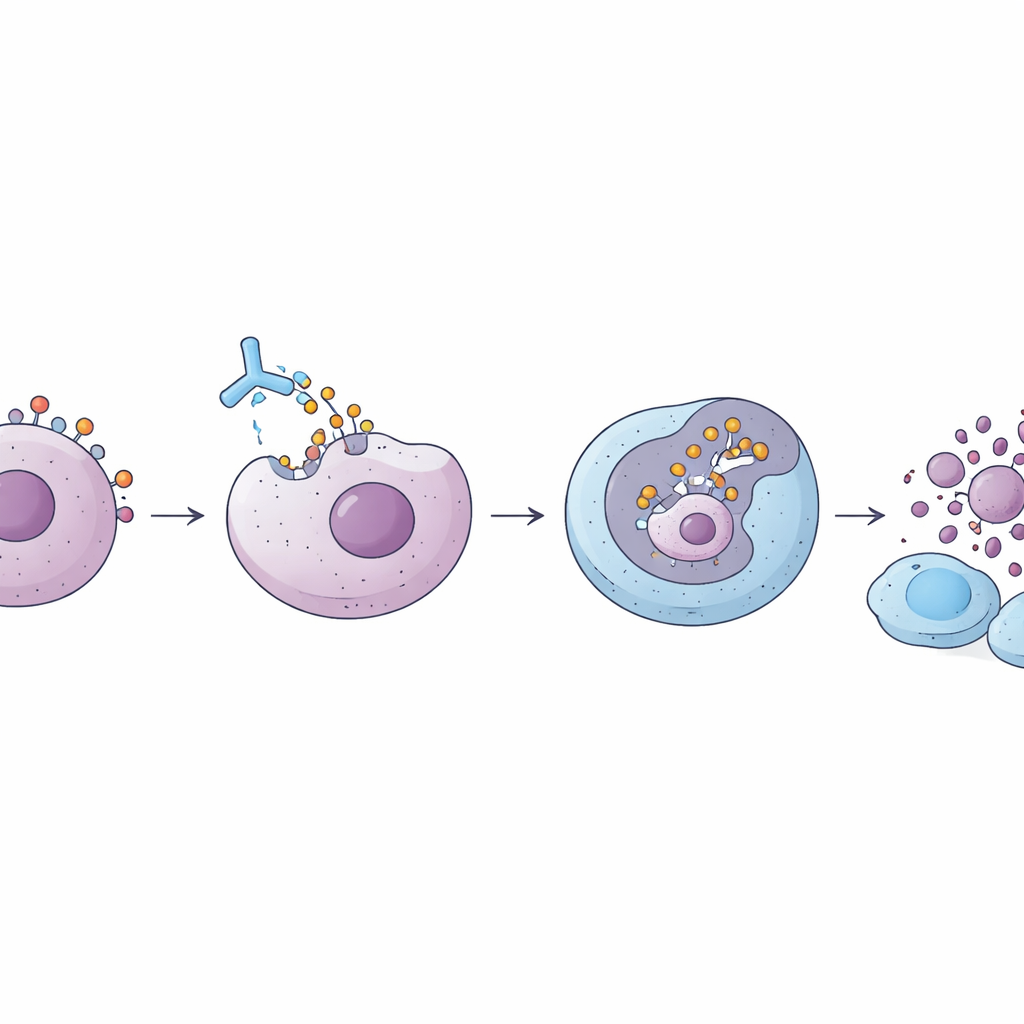
Что это может означать для будущих пациентов
В целом исследование показывает, что CSPG4 является перспективным маркером при тройно‑негативных опухолях, устойчивых к химиотерапии, и что внимательный выбор как клона антитела, так и его структурного типа может резко повлиять на эффективность ADC. Оптимизированная конструкция 225.28S IgG1–DXd уменьшала CSPG4‑положительные опухоли в реалистичных доклинических моделях, при этом в экспериментах на животных выглядела безопасной. Хотя до испытаний на людях предстоит выполнить еще много работы — включая исследования безопасности, подбор доз и клинические испытания — результаты указывают на возможную новую таргетную терапию для группы пациентов, у которых сейчас очень ограниченные варианты лечения.
Цитирование: Esapa, B., Liu, Y., Chenoweth, A.M. et al. An antibody-drug conjugate designed through clone and isotype selection restricts the growth of CSPG4-expressing triple-negative breast cancer. npj Precis. Onc. 10, 161 (2026). https://doi.org/10.1038/s41698-026-01341-0
Ключевые слова: тройно‑негативный рак молочной железы, конъюгат антитело‑лекарство, CSPG4, таргетная терапия, точная онкология