Clear Sky Science · es
Un conjugado anticuerpo-fármaco diseñado mediante selección de clon e isotipo restringe el crecimiento del cáncer de mama triple negativo que expresa CSPG4
Por qué importa esta investigación
El cáncer de mama triple negativo es una de las formas más agresivas de cáncer de mama y carece de muchas de las terapias dirigidas disponibles para otros subtipos. Este estudio explora una nueva forma de atacar estos tumores con mayor precisión, construyendo una “bomba inteligente” que se dirige a un marcador específico en las células cancerosas mientras preserva la mayor parte del tejido sano. Para los pacientes cuya enfermedad reaparece o resiste a la quimioterapia, tratamientos tan focalizados podrían ofrecer opciones urgentemente necesarias.
Una nueva bandera en células tumorales resistentes
Los investigadores se centraron en una molécula de superficie llamada CSPG4, que se encuentra en el exterior de algunas células cancerosas. Al analizar grandes conjuntos de datos de tumores de mama y examinar muestras de tejido de pacientes, mostraron que CSPG4 aparece con mucha más frecuencia en cánceres de mama triple negativos que en otros tipos de cáncer de mama. Es importante que los niveles de CSPG4 se mantuvieran igual o incluso aumentaran en el tejido tumoral que persistía después de la quimioterapia estándar, lo que sugiere que las células que llevan este marcador son especialmente resistentes y podrían ser responsables de la recaída. Los pacientes cuyos tumores tenían altos niveles de CSPG4 tendían a tener peores resultados, lo que lo convierte en una bandera atractiva para dirigir fármacos de precisión.
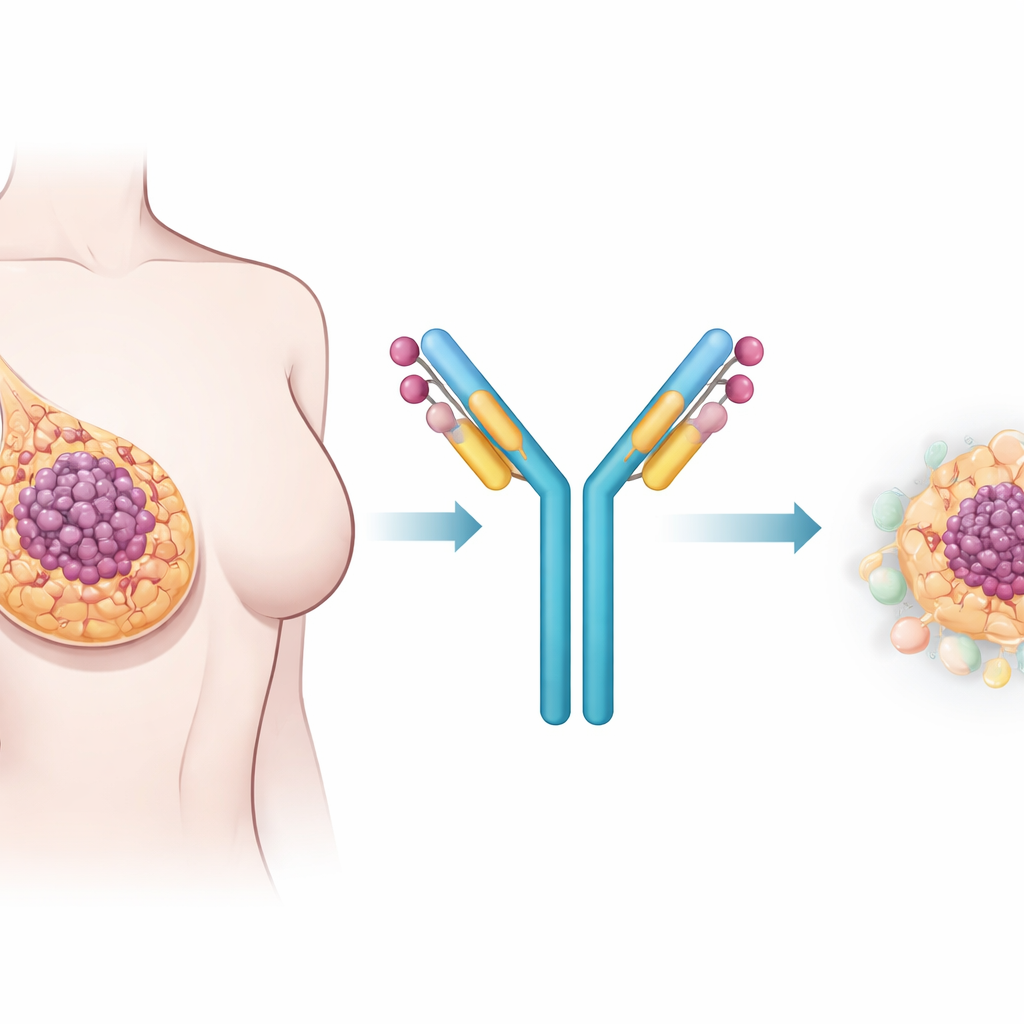
Construyendo un fármaco guiado
Para aprovechar este marcador, el equipo diseñó conjugados anticuerpo-fármaco, o ADCs. Estos son combinaciones de dos partes: un anticuerpo que reconoce un objetivo elegido en las células cancerosas y un potente fármaco citotóxico unido al anticuerpo como carga. El grupo comparó tres anticuerpos diferentes que reconocen CSPG4 pero se unen a partes ligeramente distintas de la molécula. También probaron dos “cimientos” de anticuerpo comunes, llamados IgG1 e IgG4, que difieren en su comportamiento en el organismo. En experimentos en cultivo celular, una versión del anticuerpo, denominada 225.28S en formato IgG1, destacó. Se unía fuertemente a CSPG4, era captada eficientemente por las células cancerosas y, cuando se enlazaba a una carga similar a la quimioterapia estándar, mataba las células positivas para CSPG4 con mucha más eficacia que las otras candidatas.
Mejorando la carga para un impacto mayor
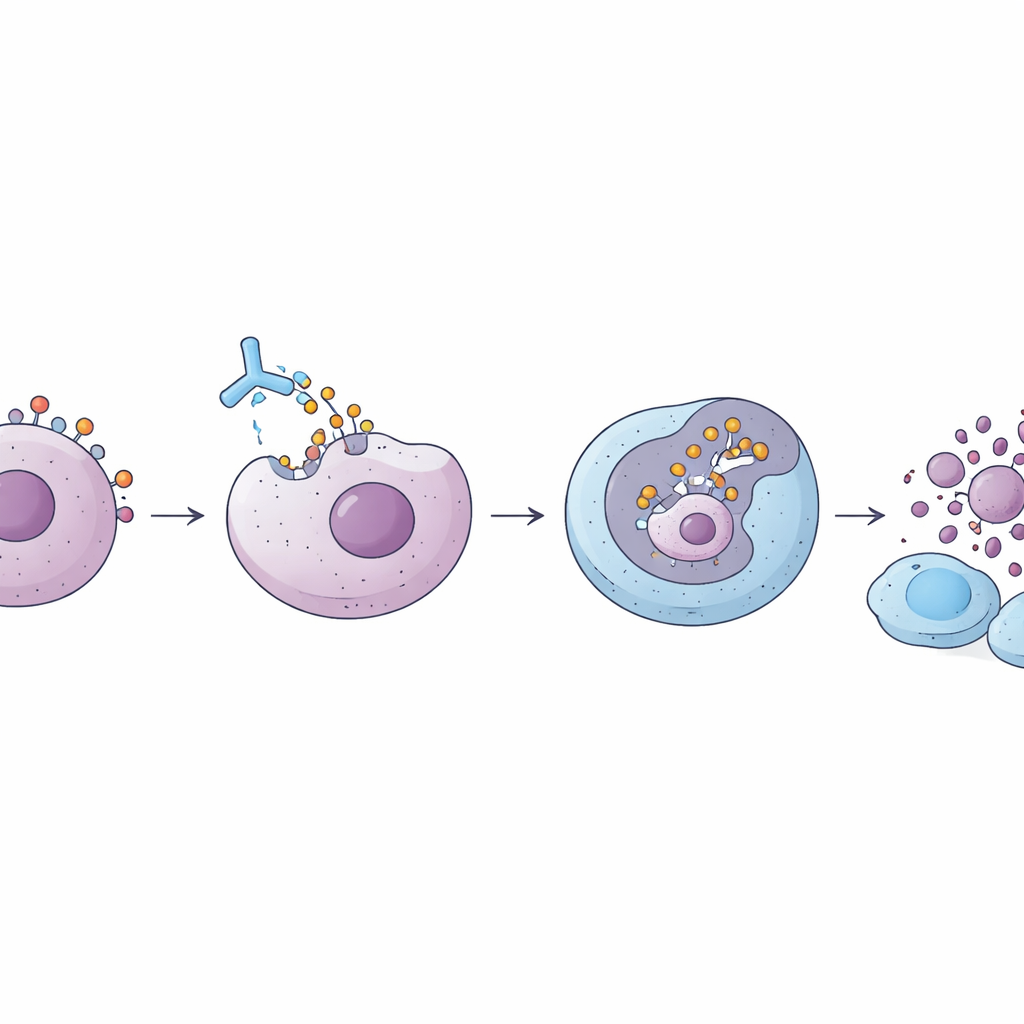
Tras identificar el mejor andamiaje de anticuerpo, los científicos emparejaron 225.28S IgG1 con una carga de nueva generación conocida como DXd, un fármaco de alta potencia ya utilizado en terapias aprobadas para otros subtipos de cáncer de mama. Diseñaron el conjugado de modo que, en promedio, ocho moléculas de DXd estuvieran unidas a cada anticuerpo, manteniendo la integridad estructural y la pureza. En pruebas de laboratorio, este ADC entró de forma eficiente en células de cáncer de mama triple negativo y melanoma ricas en CSPG4 y redujo drásticamente su supervivencia, mientras que tuvo mucho menos efecto sobre células con poco CSPG4. Este comportamiento indica que el efecto del fármaco se concentra en gran medida en las células que portan el objetivo previsto, un requisito clave para una medicina de precisión exitosa.
Pruebas en modelos vivos de una enfermedad difícil
El equipo pasó luego a modelos de xenoinjertos derivados de pacientes, en los que fragmentos de tumores humanos de cáncer de mama triple negativo se implantan en las mamas de ratones inmunodeficientes. En dos modelos independientes que expresaban CSPG4, el tratamiento con el ADC 225.28S IgG1–DXd ralentizó o detuvo sustancialmente el crecimiento tumoral a dosis similares a las usadas para otros ADCs en desarrollo, y prolongó la supervivencia de los animales sin pérdida de peso evidente ni signos de toxicidad. Curiosamente, incluso el anticuerpo solo, sin una carga de fármaco, pudo ralentizar el crecimiento tumoral cuando había células inmunitarias humanas presentes en los ratones. Esto sugiere que el anticuerpo puede no solo entregar una carga tóxica, sino también reclutar al sistema inmune para atacar las células positivas para CSPG4.
Qué podría significar esto para futuros pacientes
En conjunto, el estudio demuestra que CSPG4 es un marcador prometedor en cánceres de mama triple negativo resistentes a la quimioterapia y que la elección cuidadosa tanto del clon de anticuerpo como de su tipo estructural puede influir de forma drástica en la eficacia de un ADC. El constructo optimizado, 225.28S IgG1–DXd, redujo tumores positivos para CSPG4 en modelos preclínicos realistas y mostró un aparente perfil de seguridad en animales. Aunque queda mucho trabajo antes de que este enfoque pueda probarse en personas —incluyendo estudios de seguridad, determinación de dosis y ensayos clínicos—, los resultados apuntan hacia una posible nueva terapia dirigida para un grupo de pacientes que actualmente tienen opciones muy limitadas.
Cita: Esapa, B., Liu, Y., Chenoweth, A.M. et al. An antibody-drug conjugate designed through clone and isotype selection restricts the growth of CSPG4-expressing triple-negative breast cancer. npj Precis. Onc. 10, 161 (2026). https://doi.org/10.1038/s41698-026-01341-0
Palabras clave: cáncer de mama triple negativo, conjugado anticuerpo-fármaco, CSPG4, terapia dirigida, oncología de precisión