Clear Sky Science · zh
合成设计的环状RNA可用于靶向与心血管相关的microRNA以改善细胞功能
这对心脏健康为何重要
随着年龄增长,我们的血管会变得僵硬,血管壁中行为异常的细胞助长心肌梗死、中风及其他心血管疾病的发生。这项研究探讨了一种新的基于RNA的分子——在实验室中构建成小环状——能在血管细胞内吸附有害的调控RNA。通过驯服这些体积小却功能强大的分子,研究人员希望能温和地将衰老的血管引导回更健康的状态。
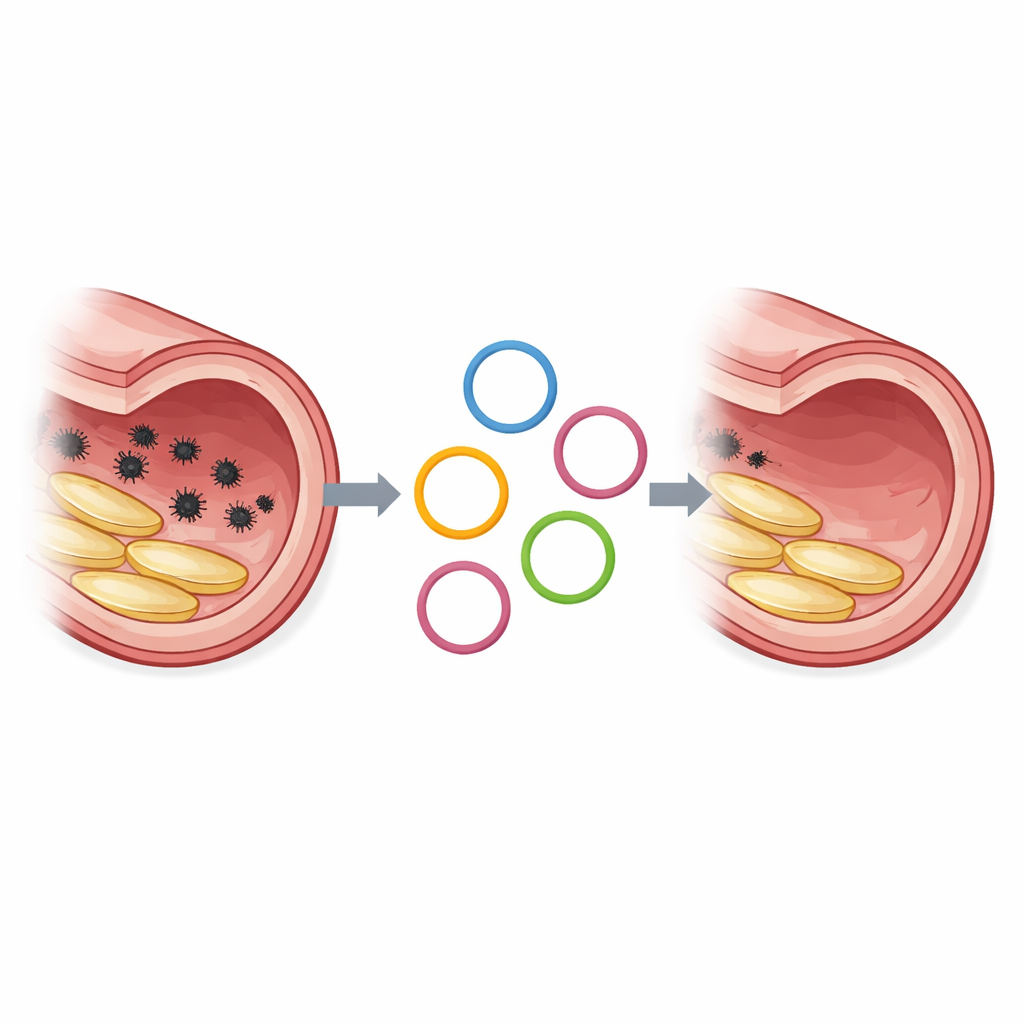
随年龄出错的小型遗传开关
在我们细胞内,称为microRNA的短RNA片段充当基因活动的微调旋钮。其中两种,miR-21-5p和miR-146a-5p,在血管老化过程中变得过度活跃,并与炎症、瘢痕形成以及血管平滑肌细胞过度增生有关。血管平滑肌细胞是帮助血管维持形态的收缩细胞。当这些microRNA过多时,它们会沉默本应抑制细胞增殖并减轻炎症的保护性基因,从而促进心血管疾病中逐渐出现的损伤。
将天然RNA环转化为治疗工具
自然界已经使用环状RNA作为海绵,结合microRNA并阻止它们干扰其他RNA。受此启发,团队设计并合成了合成环状RNA(circRNA),每种携带多个为miR-21-5p或miR-146a-5p精心调校的结合位点。由于这些构建体是封闭的环状,它们能抵抗快速降解常规线性RNA药物的细胞酶。研究人员在体外制备这些circRNA,纯化以去除残留的线性片段,并用凝胶和Northern blot等方法确认其环状形态和稳定性。
在衰老血管细胞中测试这些环
为了检验这些circRNA是否真的能改善细胞行为,科学家在体外培养的人类血管平滑肌细胞和内皮细胞上进行实验,并将其推入早期衰老样状态。在这些衰老细胞中,miR-21-5p和miR-146a-5p的水平确实比年轻细胞高。当研究人员引入低剂量的环状构建体时,观察到circRNA水平约在一天内达到峰值,随后在数天内逐渐下降。在此时间窗口内,靶向的microRNA水平下降,表明这些环成功结合并消耗了过量的microRNA分子。
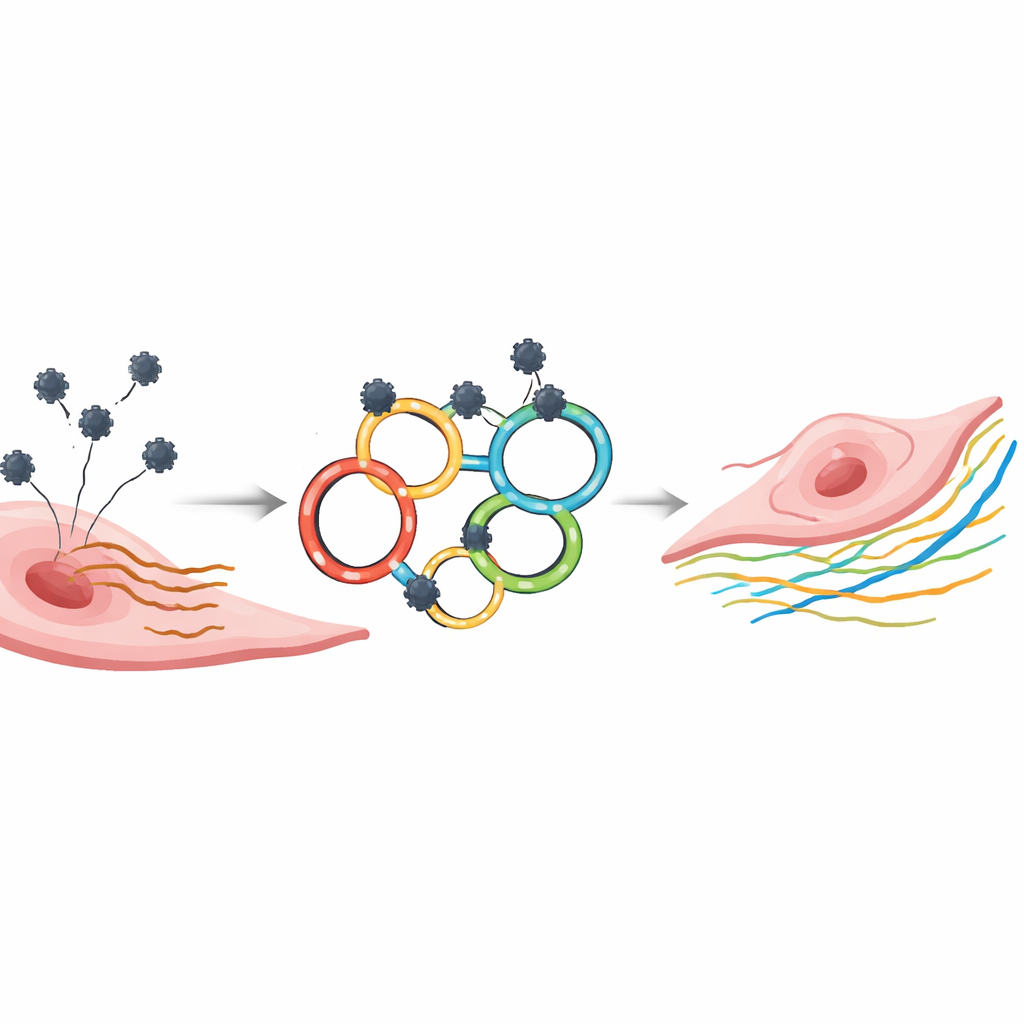
比标准抗miR药物更强的基因效应
团队将其环状设计与标准的反义“抗-miR”寡核苷酸进行了比较,后者是直接中和microRNA的线性RNA片段但稳定性较差。重要的是,使用远低于抗-miR的浓度,circRNA就能实现类似的miR-21-5p和miR-146a-5p下降。在衰老的平滑肌细胞中,针对miR-21-5p的circRNA比抗-miR方法更明显地提高了其已知的保护性靶基因(如PTEN和PDCD4)的表达。针对miR-146a-5p的circRNA同样上调了多种参与调控炎症和细胞生长的基因。在功能测试中,靶向miR-21的circRNA适度减少了平滑肌细胞的迁移——这种过度迁移会促成血管壁增厚。内皮细胞的基因变化更为细微,但在迁移和增殖方面表现出改善,表明修复能力有所提升。
RNA环用于治疗的前景与挑战
尽管这项工作完全在体外完成,但它突出了环状RNA相比传统microRNA抑制剂的若干优势:更稳定、有效剂量更低,并能提供持续但有时间限制的基因活动重塑。作者也指出了仍需克服的难题,例如确保高纯度以避免不必要的免疫反应,以及找到安全、高效的载体,将这些环输送到全身的血管细胞中。尽管如此,他们的结果表明,定制设计的RNA环有一天可能成为定向抑制有害microRNA、帮助维持血管健康的个性化治疗基础。
引用: Böttcher, S., Kalies, K., Knöpp, K. et al. Synthetically designed circRNA can be used to target cardiovascular relevant microRNAs to improve cellular function. Sci Rep 16, 12023 (2026). https://doi.org/10.1038/s41598-026-46870-7
关键词: 环状RNA疗法, 血管老化, microRNA抑制, 心血管疾病, 血管平滑肌细胞