Clear Sky Science · zh
通过细胞外乙酰-HMGB1下调半乳凝素-9转录水平,铁死亡抑制胶质瘤细胞的生物学行为
这项脑癌研究为何重要
胶质瘤是最致命的脑肿瘤之一,即便经过手术、放疗和化疗,许多患者的肿瘤仍会复发。本研究探讨了一种新近被认可的细胞死亡形式——铁死亡,以及如何利用它来减缓胶质瘤生长。通过揭示铁死亡如何改变肿瘤细胞的行为及其与免疫系统的相互作用,这项工作指向了可能使脑肿瘤侵袭性降低并更易治疗的新药靶点。
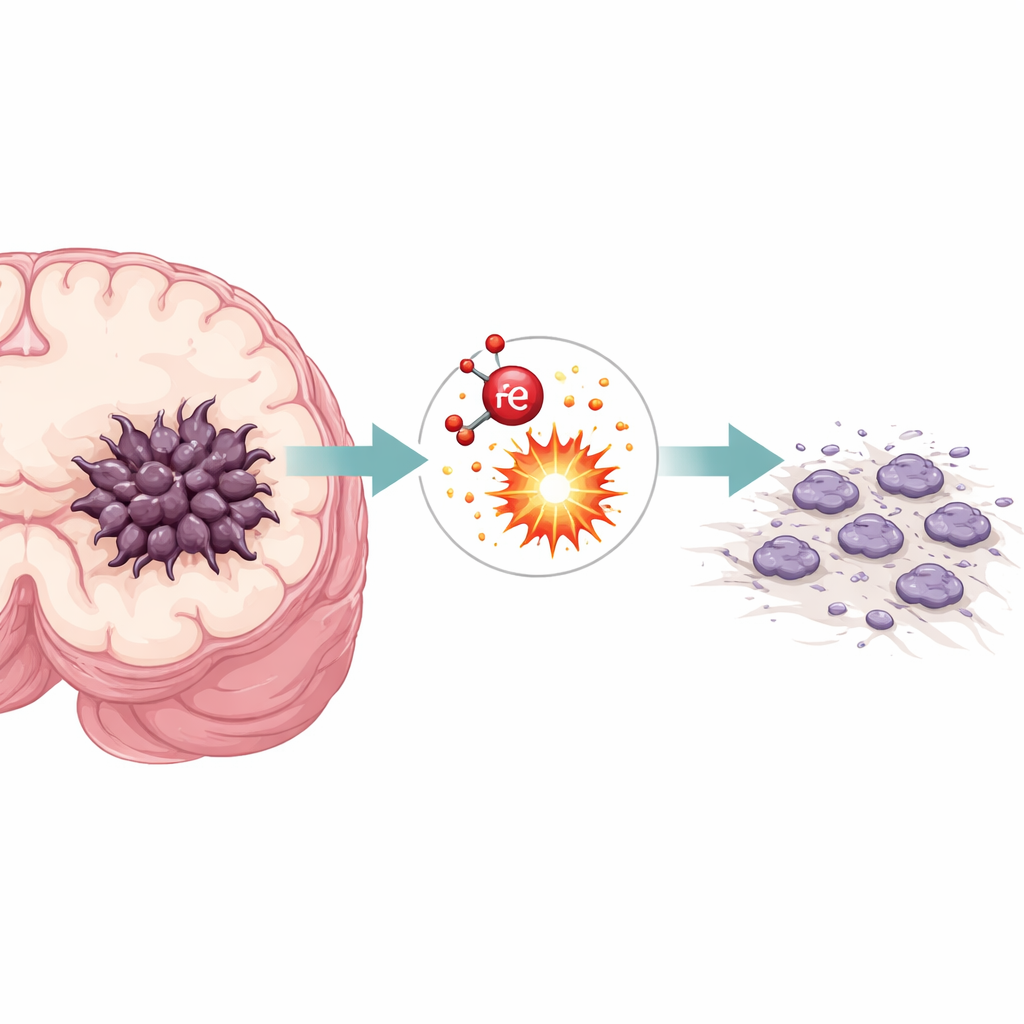
肿瘤细胞死亡的另一种途径
大多数人都听说过癌细胞逃避“程序性细胞死亡”,例如凋亡。铁死亡是一种较新发现的、依赖铁的细胞死亡方式,由细胞膜的失控损伤驱动。胶质瘤细胞对铁的需求很高,这使得它们在适当条件下特别容易发生铁死亡。研究人员使用一种名为erastin的化合物在体外培养的人胶质瘤细胞系中诱导铁死亡。他们通过检测反应性氧物种的激增来确认这一点——这些化学活跃分子标志着细胞内部的强烈氧化应激。
应激信号如何从肿瘤细胞逸出
研究团队聚焦于一种名为HMGB1的分子,该分子通常位于细胞核内,但在细胞受压或即将死亡时可以移出细胞。其一种化学修饰形式——乙酰-HMGB1——可在肿瘤微环境中充当危险信号。科学家发现,在诱导铁死亡时,胶质瘤细胞向培养液中释放了更多的乙酰-HMGB1。他们还表明,细胞内一种基本的回收过程——自噬,既促进铁死亡也促进乙酰-HMGB1的释放:增强自噬会增加释放,抑制自噬则会减少释放。
使肿瘤细胞侵袭性下降且更脆弱
接下来,研究人员考察了这些变化对胶质瘤细胞侵袭行为的影响。在模拟肿瘤细胞穿越组织屏障的侵袭实验中,发生铁死亡的细胞穿膜能力显著下降,表明其侵袭潜能降低。细胞增殖速度下降,更多细胞进入凋亡这一另一种程序性死亡。当研究团队用一种源自甘草的化合物(甘草酸)阻断细胞外的乙酰-HMGB1时,这些益处部分消失:侵袭和增殖有所恢复,凋亡减少。这表明铁死亡期间释放的乙酰-HMGB1并非单纯副产物,而是积极参与抑制肿瘤细胞侵袭性的过程,自噬则有助于维持该效应。
将细胞死亡与免疫“刹车”联系起来
研究随后转向免疫检查点——这些分子可作为免疫攻击的开关。胶质瘤细胞常利用这些检查点逃避免疫监视。研究人员在诱导铁死亡后测量了四个此类基因的表达活性。其中两个,CD155和半乳凝素-9,明显下调,而CD80和HMGB1本身在基因水平上变化不大。当他们同时诱导铁死亡并阻断乙酰-HMGB1时,只有半乳凝素-9从降低状态转为升高表达,而CD155仍保持低水平。抑制自噬也削弱了半乳凝素-9的下降。综合这些结果,提示了一个特定的事件链:铁死亡 → 自噬 → 乙酰-HMGB1的释放 → 半乳凝素-9基因活性下降。
对未来脑肿瘤治疗可能的意义
已知半乳凝素-9有助于营造免疫抑制性微环境,从而保护肿瘤免受免疫攻击。通过表明铁死亡可通过释放乙酰-HMGB1来降低半乳凝素-9水平,这项工作勾勒出一种既削弱胶质瘤细胞又降低其免疫逃逸能力的潜在路径。尽管该研究仅在一条细胞系中进行,且信号通路的重要细节仍需厘清,但它将铁死亡以及乙酰-HMGB1/半乳凝素-9轴列为有前景的靶点。长远来看,能够安全触发该通路或模拟其效应的药物,可能作为现有疗法的补充,从而有助于在与脑肿瘤的斗争中扭转局势。
引用: Xu, Y., Tan, G. & Zhu, R. Ferroptosis inhibits biological behaviors of glioma cells by downregulating Galectin-9 transcriptional level via extracellular Acetyl-HMGB1. Sci Rep 16, 10681 (2026). https://doi.org/10.1038/s41598-026-45969-1
关键词: 胶质瘤, 铁死亡, 免疫检查点, HMGB1, 半乳凝素-9