Clear Sky Science · ru
Ферроптоз подавляет биологическое поведение клеток глиомы путем понижения транскрипционного уровня галектин-9 через внеклеточный ацетилированный HMGB1
Почему это исследование рака мозга важно
Глиомы относятся к одним из самых смертых опухолей мозга, и даже при хирургии, лучевой терапии и химиотерапии у многих пациентов опухоль возвращается. В этом исследовании изучается недавно признанная форма гибели клеток — ферроптоз — и то, как ее можно использовать для замедления роста глиомы. Раскрывая, как ферроптоз меняет поведение опухолевых клеток и их взаимодействие с иммунной системой, работа указывает на новые мишени для препаратов, которые могут сделать опухоли мозга менее инвазивными и более поддающимися лечению.
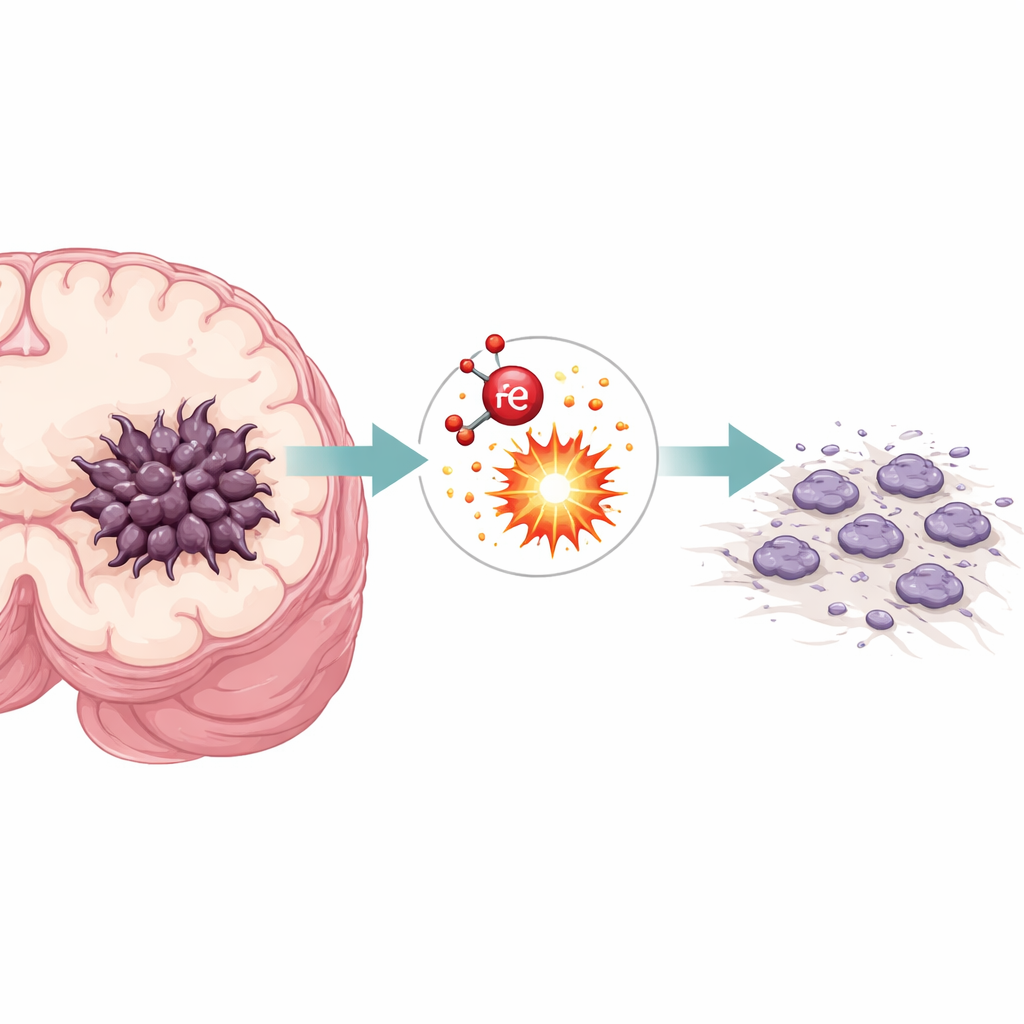
Другой путь гибели опухолевых клеток
Большинство людей слышали о том, что раковые клетки избегают «запрограммированной гибели», такой как апоптоз. Ферроптоз — более новая, зависящая от железа форма гибели клеток, вызванная неконтролируемым повреждением клеточных мембран. Клетки глиомы имеют высокий спрос на железо, что делает их особенно уязвимыми к ферроптозу при соответствующем воздействии. Исследователи использовали соединение, называемое эрастин, чтобы вызвать ферроптоз в культуре человеческой линии клеток глиомы. Они подтвердили это измерением всплеска реактивных форм кислорода — химически агрессивных молекул, свидетельствующих о сильном окислительном стрессе в клетках.
Как сигналы стресса покидают опухолевую клетку
Команда сосредоточилась на молекуле HMGB1, которая обычно находится в ядре клетки, но может покидать клетку при стрессе или гибели. Химически модифицированная форма — ацетилированный HMGB1 — может выступать как сигнал опасности в окружении опухоли. Ученые обнаружили, что при индукции ферроптоза клетки глиомы выделяют значительно больше ацетилированного HMGB1 в среду культивирования. Они также показали, что базовый процесс утилизации внутри клетки, называемый аутопагией, способствует как ферроптозу, так и выделению ацетилированного HMGB1: усиление аутопагии увеличивало выделение, а блокирование — снижало его.
Делая опухолевые клетки менее инвазивными и более хрупкими
Далее исследователи изучили, что означают эти изменения для агрессивности поведения клеток глиомы. В тестах на инвазию, имитирующих перемещение опухолевых клеток через тканевые барьеры, клетки, подвергшиеся ферроптозу, значительно хуже проходили через мембрану, что указывает на снижение инвазивного потенциала. Их скорость роста упала, и больше клеток подвергалось апоптозу, другой форме программируемой смерти. Когда команда блокировала внеклеточный ацетилированный HMGB1 с помощью соединения, полученного из солодки (глицирризиновая кислота), эти преимущества частично исчезали: инвазия и рост снова увеличивались, а апоптоз снижался. Это указывает на то, что ацетилированный HMGB1, выделяемый во время ферроптоза, является не просто побочным продуктом, а активно способствует сдерживанию агрессивности опухолевых клеток, при этом аутопагия помогает поддерживать этот эффект.
Связывание гибели клеток с иммунными «тормозами»
Затем исследование обратилось к иммунным контрольным точкам — молекулам, которые могут действовать как выключатели для иммунной атаки. Клетки глиомы часто используют эти контрольные точки, чтобы скрыться от иммунной системы. Исследователи измеряли активность четырех таких генов в клетках глиомы после индукции ферроптоза. Два из них, CD155 и галектин-9, были явно понижены, тогда как CD80 и сам HMGB1 на уровне гена существенно не изменились. Когда они одновременно вызывали ферроптоз и блокировали ацетилированный HMGB1, только экспрессия галектин-9 сменила понижение на повышение, тогда как CD155 оставался низким. Ингибирование аутопагии также ослабляло падение уровня галектин-9. В совокупности эти результаты указывают на специфическую цепочку событий: ферроптоз → аутопагия → выделение ацетилированного HMGB1 → снижение активности гена галектин-9.
Что это может значить для будущих методов лечения опухолей мозга
Известно, что галектин-9 помогает создавать иммуносупрессивную среду, которая защищает опухоли от атак. Показав, что ферроптоз может снижать уровни галектин-9 через выделение ацетилированного HMGB1, эта работа очерчивает потенциальный способ одновременно ослабить клетки глиомы и затруднить им уклонение от иммунной защиты. Хотя исследование проведено на одной клеточной линии и важные детали сигнального пути еще предстоит уточнить, оно выделяет ферроптоз и ось ацетилированный HMGB1/галектин-9 как перспективные мишени. В перспективе препараты, которые безопасно запускают этот путь или имитируют его эффекты, могли бы дополнить существующие терапии и помочь изменить баланс в пользу борьбы с опухолями мозга.
Цитирование: Xu, Y., Tan, G. & Zhu, R. Ferroptosis inhibits biological behaviors of glioma cells by downregulating Galectin-9 transcriptional level via extracellular Acetyl-HMGB1. Sci Rep 16, 10681 (2026). https://doi.org/10.1038/s41598-026-45969-1
Ключевые слова: глиома, ферроптоз, иммунные контрольные точки, HMGB1, галектин-9