Clear Sky Science · zh
异源 saRNA 首针——多价蛋白增强策略诱导对 SARS-CoV-2 和 MERS-CoV 的广谱且持久免疫
为何面向未来的疫苗很重要
在过去二十年里,世界已经历三次危险的冠状病毒暴发:SARS、MERS 和 COVID‑19。每一次,疫苗都是在对单一新威胁的紧急应对中匆忙开发出来的。本研究提出了一个更大的问题:我们能否设计一种接种策略,让免疫系统同时为整个冠状病毒家族做好准备,包括尚未出现、无法命名的未来变体?通过在动物中结合最前沿的 RNA 技术与传统蛋白疫苗,研究者勾画出一条通往更普适保护的可行路径。
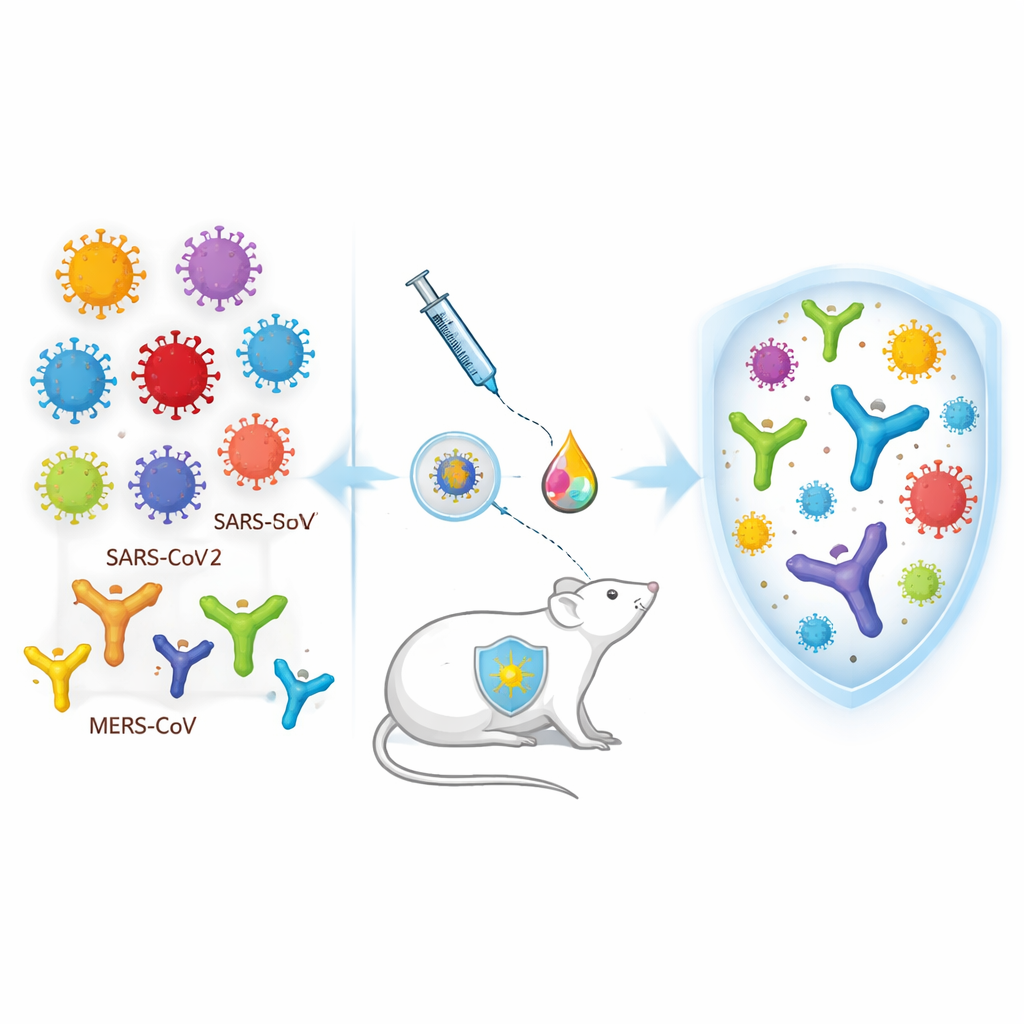
两种不同疫苗的协同作用
研究团队聚焦于“异源”首针‑增强策略,即首针和加强针使用不同类型的疫苗。首针为封装在聚合物树枝状纳米颗粒中的自增殖 RNA(saRNA)。注射后,这段 RNA 指示细胞短暂产生冠状病毒刺突蛋白,强烈激活免疫系统。增强针为蛋白类疫苗,包含刺突蛋白的三种受体结合域(RBD):来自原始武汉株的 RBD、Beta 变体的 RBD 以及 MERS‑CoV 的 RBD,均与长期使用的明胶‑铝佐剂(alum)混合。设计理念是让 RNA 首针迅速建立强劲的免疫记忆,然后用多价蛋白增强剂扩展并稳定这种记忆,覆盖多种病毒亲缘株。
小鼠中更强且更广的抗体反应
在小鼠中,单用 RNA 首针可以对其编码的刺突或 RBD 产生可靠的抗体反应,而仅用蛋白疫苗也能达到类似效果,但通常需要更高的剂量。当研究者将这两种平台结合使用——先 RNA、后蛋白——效果显著。即使蛋白增强剂剂量很低、单独使用几乎不引起反应,在 RNA 首针奠定基础后也能触发抗体水平的大幅跃升。重要的是,包含 MERS‑CoV 成分的增强针在扩展识别病毒谱方面起到了作用,同时并未削弱对 SARS‑CoV‑2 变体的反应。相比第二次 RNA 注射,含铝的蛋白增强后抗体下降更慢,提示保护可能更持久。
在仓鼠中显示持久免疫与灵活性
为验证该策略随时间的持久性及在另一物种中的表现,研究团队在叙利亚金仓鼠中进行了更长期的实验。动物接种的方案为同种平台两针(RNA/RNA 或 蛋白/蛋白)或混合的 RNA 首针/蛋白增强。首次增强后,各组均产生抗体,但只有异源组在长达 78 天的停顿期内维持甚至增加了抗体水平,而同平台组的反应逐渐减弱。当所有动物随后接种包含 Beta 与 Omicron 蛋白的单次更新增强针时,混合平台的动物显示出最大的抗体跃升,包括对 Omicron 的反应,尽管该变体已知具有免疫逃逸能力。整个过程中,动物对重复接种的耐受性良好。
平衡效力与副作用
现代 RNA 疫苗以高效著称,但在激活固有免疫信号时,可能引发短暂的类流感副反应。研究者比较了 RNA 与蛋白疫苗诱导的早期炎症标志物。常规脂质递送的 RNA 配方产生更强且持续时间更长的细胞因子激增,而基于树枝状聚合物的 RNA 颗粒则将这种反应调低。含铝佐剂的蛋白增强剂只引发短暂的峰值反应,通常在一天内消退。这一模式支持这样的接种安排:首针用 RNA 提供所需的强烈激活以训练免疫系统,而随后用蛋白增强以较低的系统性炎症安全地刷新并扩展保护范围。
这对未来大流行意味着什么
对非专业读者而言,结论是经过深思熟虑的不同疫苗类型组合能使免疫既更强又更具适应性。在这项研究中,动物中先 RNA 首针、后多价蛋白增强的方案带来了高水平抗体、覆盖多种冠状病毒株(包括 MERS‑CoV 和类似 Omicron 的变体)的广谱性,以及数月后仍能被“唤醒”的记忆反应。由于 RNA 与铝佐剂蛋白疫苗均可规模化生产并随新变体更新,这种异源策略为构建面向未来的冠状病毒疫苗提供了现实的框架,使其不仅防护上一次大流行,也有望应对下一次。
引用: Renn, D., McPartlan, J.S., Banala, S. et al. Heterologous saRNA prime – multivalent protein boost strategy induces broad and durable immunity against SARS-CoV-2 and MERS-CoV. Sci Rep 16, 14565 (2026). https://doi.org/10.1038/s41598-026-44645-8
关键词: 泛冠状病毒疫苗, 异源首针-增强, 自增殖 RNA, 多价蛋白增强剂, SARS-CoV-2 与 MERS-CoV 免疫