Clear Sky Science · nl
Heterologe saRNA prime – multivalente eiwitbooststrategie induceert brede en duurzame immuniteit tegen SARS-CoV-2 en MERS-CoV
Waarom toekomstbestendige vaccins ertoe doen
In twee decennia hebben we al drie gevaarlijke coronavirusuitbraken gezien: SARS, MERS en COVID‑19. Elke keer moesten vaccins snel worden ontwikkeld tegen één nieuw dreigend virus. Deze studie stelt een bredere vraag: kunnen we een vaccinatiestrategie ontwerpen die het immuunsysteem tegelijk voorbereidt op een hele familie coronavirussen, inclusief toekomstige varianten die we nu nog niet kunnen benoemen? Met een combinatie van geavanceerde RNA‑technologie en klassieke eiwitvaccins in dieren schetsen de onderzoekers een praktische route naar meer universele bescherming.
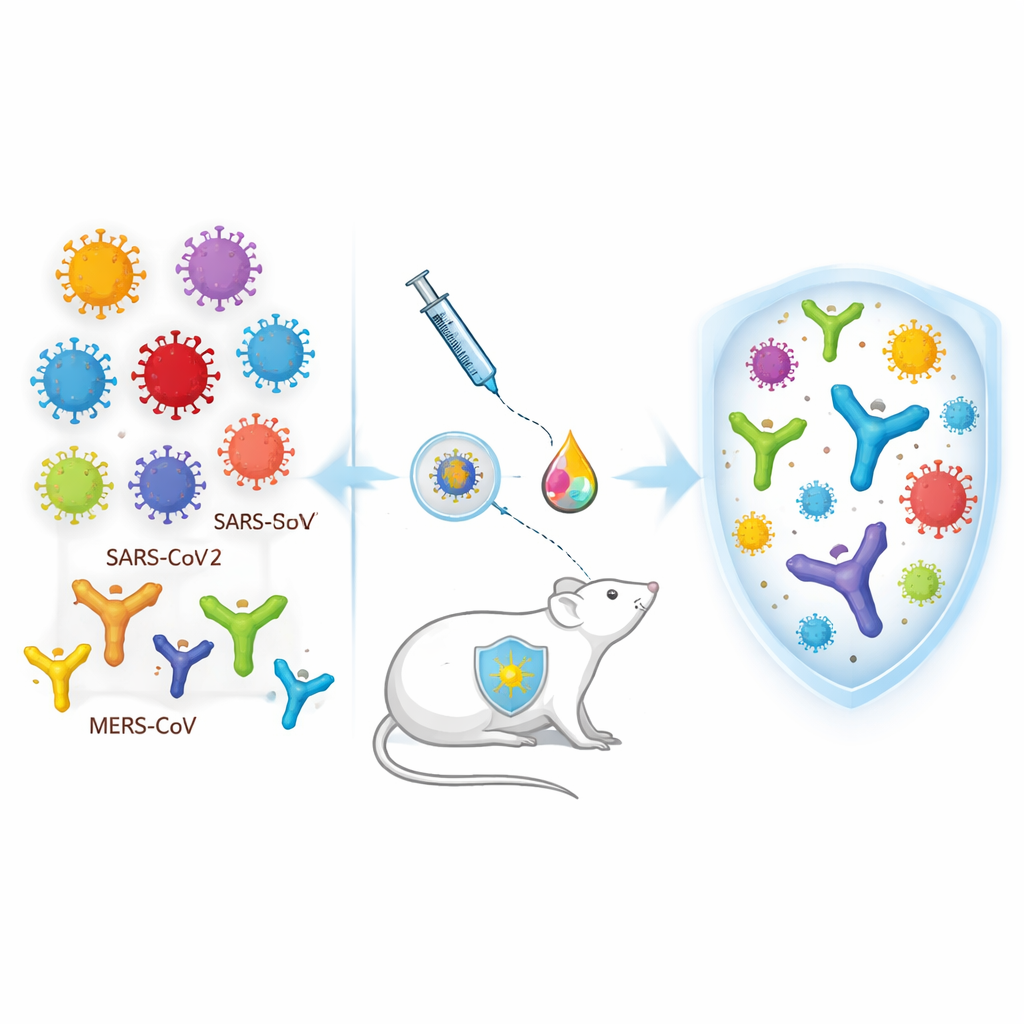
Twee verschillende prikken die samenwerken
Het team richtte zich op een “heterologe” prime‑boostbenadering, wat betekent dat de eerste en tweede prik verschillende vaccinetypen gebruiken. De prime is een zelfversterkend RNA (saRNA) verpakt in dendrimer‑nanodeeltjes. Eenmaal geïnjecteerd, geeft dit RNA cellen de opdracht tijdelijk coronavirus‑spike-eiwitten te maken, wat het immuunsysteem krachtig alarmeert. De boost is een eiwitprik met drie versies van de receptorbindende domein (RBD) van de spike: één van de oorspronkelijke Wuhan SARS‑CoV‑2‑stam, één van de Beta‑variant en één van MERS‑CoV, allemaal gemengd met het al lang gebruikte alum‑adjuvans. Het idee is dat de RNA‑prik snel sterk immuungeheugen opbouwt, waarna de multivalente eiwitprik dat geheugen verbreedt en stabiliseert over meerdere virale verwanten.
Sterkere en bredere antilichamen bij muizen
Bij muizen leverde de RNA‑prime alleen al robuuste antilichaamreacties op tegen de spike‑ of RBD‑variant die het codeerde, terwijl alleen‑eiwitprikken vergelijkbare reacties gaven maar hogere doseringen vereisten. Wanneer de onderzoekers de platforms combineerden—eerst RNA, later eiwit—was het effect dramatisch. Zelfs zeer lage doses van de eiwitbooster, die op zichzelf nauwelijks een respons opwekten, veroorzaakten enorme stijgingen in antilichaamniveaus zodra een RNA‑prime de basis had gelegd. Belangrijk is dat boosters met MERS‑CoV‑componenten het spectrum van herkende virussen vergrootten zonder de respons op SARS‑CoV‑2‑varianten te verzwakken. Ook daalden de antilichamen langzamer na de alum‑gebaseerde eiwitboost dan na een tweede RNA‑prik, wat duidt op mogelijk duurzamere bescherming.
Langdurige immuniteit en flexibiliteit bij hamsters
Om te onderzoeken of deze strategie over tijd en in een andere soort standhoudt, voerde het team langere studies uit bij Syrische goudhamsters. Dieren kregen ofwel twee keer hetzelfde type prik (RNA/RNA of eiwit/eiwit) of het gemengde RNA‑prime/eiwit‑boostschema. Na de eerste booster ontwikkelde iedere groep antilichamen, maar alleen de heterologe groep handhaafde of verhoogde zelfs haar niveaus tijdens een lange pauze van 78 dagen, terwijl de responsen bij dezelfde‑platformgroepen vervaagden. Toen later alle dieren een enkele geüpdatete booster met Beta‑ en Omicron‑eiwitten ontvingen, lieten de dieren met het gemengde platform de grootste stijging van antilichamen zien, ook tegen Omicron, ondanks diens bekende vermogen om immuniteit te ontwijken. Gedurende het hele experiment verdroegen de dieren de herhaalde vaccinaties goed.
Balanceren van kracht en bijwerkingen
Moderne RNA‑vaccins staan bekend om hun krachtige werking maar kunnen tijdelijke griepachtige bijwerkingen veroorzaken doordat ze aangeboren immuunsignalen activeren. De onderzoekers vergeleken deze vroege ontstekingsmarkers tussen RNA‑ en eiwitprikken. Conventionele lipidegebaseerde RNA‑formuleringen veroorzaakten sterkere, langer aanhoudende cytokinesurges, terwijl de dendrimer‑gebaseerde RNA‑deeltjes dit temperden. De alum‑geadjuveerde eiwitboosters veroorzaakten slechts kortdurende pieken die binnen een dag verdwenen. Dit patroon suggereert een schema waarbij de initiële RNA‑prik de krachtige stimulans levert die nodig is om het immuunsysteem te trainen, terwijl latere eiwitboosters veilig opfrissen en de bescherming verbreden met minder systemische ontsteking.
Wat dit kan betekenen voor toekomstige pandemieën
Voor niet‑specialisten is de conclusie dat het doelbewust combineren van vaccinetypen immuniteit zowel sterker als aanpasbaarder kan maken. In deze studie leverde een RNA‑prime gevolgd door een multivalente eiwitboost in dieren hoge antilichaamniveaus, brede dekking van meerdere coronavirusstammen (inclusief MERS‑CoV en Omicron‑achtige varianten) en responsen die maanden later nog “wakker gemaakt” konden worden. Omdat zowel RNA‑ als alum‑gebaseerde eiwitvaccins op schaal geproduceerd en aangepast kunnen worden naarmate nieuwe varianten opkomen, biedt deze heterologe aanpak een realistisch kader voor het bouwen van toekomstbestendige coronavirusvaccins die beschermen niet alleen tegen de vorige pandemie, maar ook tegen de volgende.
Bronvermelding: Renn, D., McPartlan, J.S., Banala, S. et al. Heterologous saRNA prime – multivalent protein boost strategy induces broad and durable immunity against SARS-CoV-2 and MERS-CoV. Sci Rep 16, 14565 (2026). https://doi.org/10.1038/s41598-026-44645-8
Trefwoorden: pan-coronavirusvaccins, heterologe prime-boost, zelfversterkend RNA, multivalente eiwitbooster, SARS-CoV-2 en MERS-CoV immuniteit