Clear Sky Science · de
Heterologisches saRNA-Prime – multivalenter Protein-Boost-Ansatz induziert breite und anhaltende Immunität gegen SARS-CoV-2 und MERS-CoV
Warum zukunftssichere Impfstoffe wichtig sind
In nur zwei Jahrzehnten hat die Welt bereits drei gefährliche Coronavirus-Ausbrüche erlebt: SARS, MERS und COVID‑19. Jedes Mal mussten Impfstoffe schnell gegen eine einzelne neue Bedrohung entwickelt werden. Diese Studie stellt eine größere Frage: Können wir eine Impfstrategie entwerfen, die das Immunsystem gleichzeitig auf eine ganze Familie von Coronaviren vorbereitet, einschließlich künftiger Varianten, die wir noch nicht benennen können? Mithilfe einer Kombination aus moderner RNA-Technologie und klassischen Proteinimpfstoffen in Tierversuchen zeichnen die Forschenden einen praktischen Weg zu umfassenderem Schutz nach.
Zwei verschiedene Spritzen, die zusammenwirken
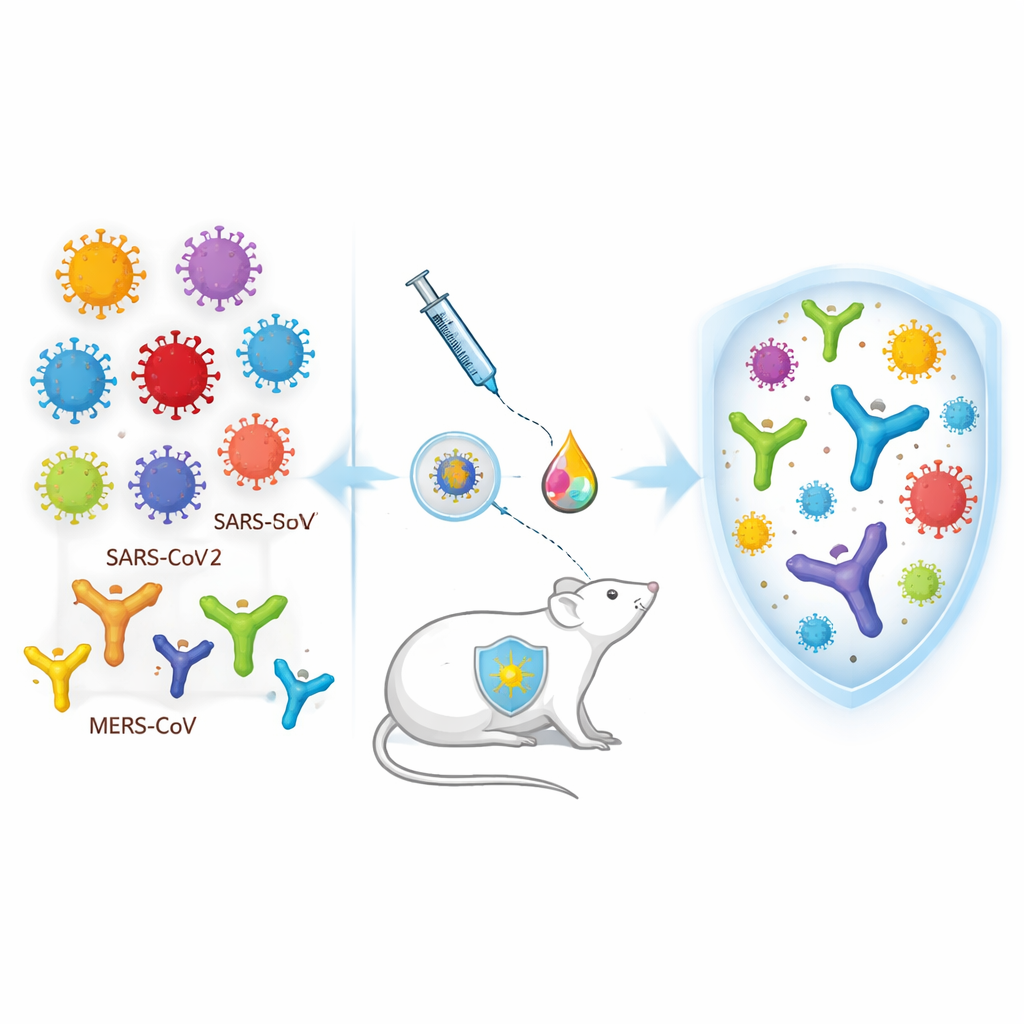
Das Team konzentrierte sich auf einen „heterologen“ Prime‑Boost-Ansatz, das heißt, die erste und zweite Dosis nutzen unterschiedliche Impfstofftypen. Der Prime ist eine selbstverstärkende RNA (saRNA), verpackt in Dendrimer-Nanopartikel. Nach der Injektion veranlasst diese RNA Zellen dazu, vorübergehend Coronavirus-Spike-Proteine herzustellen und so das Immunsystem kräftig zu alarmieren. Der Boost ist eine Proteinimpfung, die drei Varianten der rezeptorbindenden Domäne (RBD) des Spike enthält: eine aus dem ursprünglichen Wuhan-SARS‑CoV‑2-Stamm, eine aus der Beta-Variante und eine aus MERS‑CoV, alle gemischt mit dem seit langem verwendeten Alum-Adjuvans. Die Idee ist, mit der RNA-Impfung schnell ein starkes immunologisches Gedächtnis aufzubauen und dann mit der multivalenten Proteinimpfung dieses Gedächtnis über mehrere virale Verwandte hinweg zu verbreitern und zu stabilisieren.
Stärkere und breitere Antikörper bei Mäusen
Bei Mäusen erzeugte der RNA-Prime allein solide Antikörperantworten gegen die jeweils kodierte Spike‑ oder RBD‑Version, während reine Proteinimpfungen Ähnliches bewirkten, aber höhere Dosen erforderten. Als die Forschenden die Plattformen kombinierten – zuerst RNA, später Protein – war der Effekt dramatisch. Selbst sehr niedrige Dosen des Protein-Boosters, die allein kaum eine Reaktion hervorgerufen hätten, lösten nach einem RNA-Prime enorme Anstiege der Antikörperspiegel aus. Wichtig ist, dass Booster mit MERS‑CoV-Komponenten das Spektrum der erkannten Viren erweiterten, ohne die Reaktion auf SARS‑CoV‑2-Varianten abzuschwächen. Zudem fielen die Antikörperspiegel nach dem alum-basierten Protein-Boost langsamer ab als nach einer zweiten RNA-Dosis, was auf einen langlebigeren Schutz hindeutet.
Anhaltende Immunität und Flexibilität bei Hamstern
Um zu prüfen, ob diese Strategie über längere Zeit und in einer anderen Spezies trägt, führten die Forschenden längere Studien an Goldhamstern (Mesocricetus auratus) durch. Die Tiere erhielten entweder zweimal dieselbe Art von Impfung (RNA/RNA oder Protein/Protein) oder den gemischten RNA‑Prime/Protein‑Boost-Zeitplan. Nach dem ersten Booster entwickelten alle Gruppen Antikörper, doch nur die heterologe Gruppe hielt ihre Werte während einer langen Pause von 78 Tagen aufrecht oder steigerte sie sogar, während die Reaktionen in den gleichplattformigen Gruppen verblassten. Als alle Tiere später einen einzelnen aktualisierten Booster mit Beta- und Omicron-Proteinen erhielten, zeigten die Tiere mit gemischter Plattform den größten Anstieg an Antikörpern, auch gegen Omicron, trotz seiner bekannten Fähigkeit, Immunität zu umgehen. Insgesamt vertrugen die Tiere die wiederholten Impfungen gut.
Abwägung von Wirksamkeit und Nebenwirkungen
Moderne RNA-Impfstoffe sind bekannt für ihre starke Wirkung, können aber vorübergehende grippeähnliche Nebenwirkungen hervorrufen, weil sie angeborene Immunreaktionen anstoßen. Die Forschenden verglichen diese frühen Entzündungsmarker zwischen RNA- und Proteinimpfungen. Konventionelle lipidbasierte RNA-Formulierungen lösten stärkere, länger anhaltende Zytokinanstiege aus, während die dendrimerbasierten RNA-Partikel dies abschwächten. Die alum-adjuvantierten Proteinbooster verursachten nur kurzlebige Spitzen, die sich innerhalb eines Tages zurückbildeten. Dieses Muster legt einen Zeitplan nahe, bei dem die initiale RNA-Impfung den kräftigen Impuls zum Trainieren des Immunsystems liefert, während spätere Proteinbooster den Schutz sicher und mit weniger systemischer Entzündung auffrischen und verbreitern.
Was das für künftige Pandemien bedeuten könnte
Für Nichtfachleute lautet die Schlussfolgerung, dass das durchdachte Mischen von Impfstofftypen die Immunität sowohl stärker als auch anpassungsfähiger machen kann. In dieser Studie erzielte ein RNA-Prime gefolgt von einem multivalenten Protein-Boost in Tierversuchen hohe Antikörperspiegel, eine breite Abdeckung mehrerer Coronavirus-Stämme (einschließlich MERS‑CoV und Omicron-ähnlicher Varianten) und Reaktionen, die Monate später bereitstanden, wieder „aufgeweckt“ zu werden. Da sowohl RNA- als auch alum-basierte Proteinimpfstoffe in großem Maßstab hergestellt und an neue Varianten angepasst werden können, bietet dieser heterologe Ansatz ein realistisches Rahmenkonzept für zukunftssichere Coronavirus-Impfstoffe, die nicht nur gegen die letzte Pandemie, sondern auch gegen die nächste schützen.
Zitation: Renn, D., McPartlan, J.S., Banala, S. et al. Heterologous saRNA prime – multivalent protein boost strategy induces broad and durable immunity against SARS-CoV-2 and MERS-CoV. Sci Rep 16, 14565 (2026). https://doi.org/10.1038/s41598-026-44645-8
Schlüsselwörter: Pan-Coronavirus-Impfstoffe, heterologes Prime-Boost, selbstverstärkende RNA, multivalenter Protein-Booster, Immunität gegen SARS-CoV-2 und MERS-CoV