Clear Sky Science · zh
疫苗诱导的T细胞反应不足以产生对SARS-CoV-2的保护性免疫
这项研究为何重要
随着COVID-19疫苗的推广,关注点很大一部分集中在抗体——那些能阻止病毒感染细胞的蛋白质上。但免疫系统的另一面——T细胞,常被认为有助于防止患者入院并提供更持久的保护。本研究提出了一个简单但关键的问题:如果疫苗主要引发强烈的T细胞反应而几乎不产生中和抗体,这是否足以防止重症COVID-19?
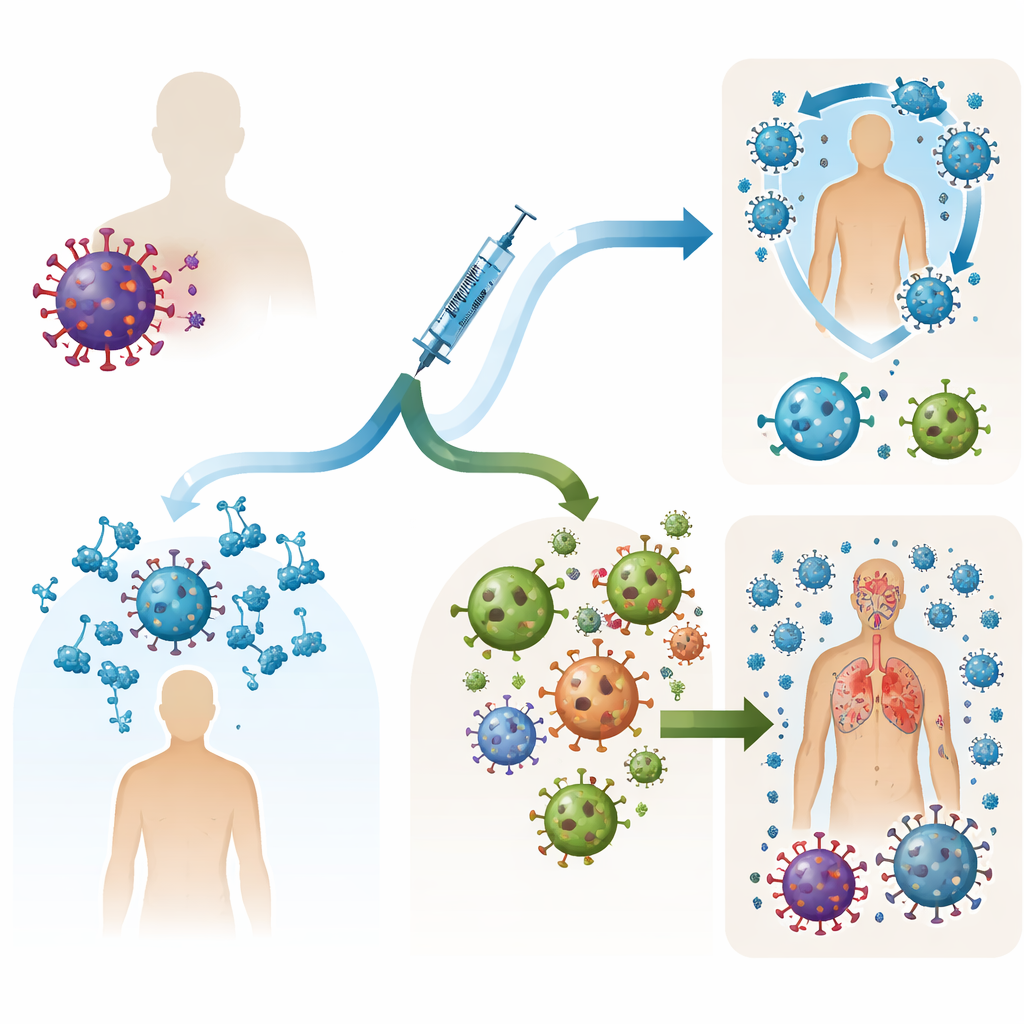
两条主要防线
我们的免疫系统对抗病毒有两种广泛方式。抗体在血液和黏液中游离,在病毒进入细胞之前结合并中和它们。中和抗体尤其强大,因为它们阻断了病毒用来入侵的关键结构。相比之下,T细胞在组织中巡逻,识别并摧毁已被感染的细胞,从而限制感染的扩散。许多不能产生良好抗体的患者——例如某些血液癌症患者或接受B细胞耗损药物治疗的人——在接种疫苗后仍能产生T细胞反应。这引发了希望,即“以T细胞为主”的疫苗可能保护那些抗体反应薄弱的人群。
设计有利于T细胞的疫苗
研究团队使用了DNA疫苗,这是一种利用小型环状DNA片段指示细胞合成病毒蛋白的平台。他们设计了几种不同的SARS-CoV-2刺突蛋白版本,包括一个尾部缩短的版本(ΔC),以及另一个去除了关键裂解位点并插入灵活连接子(Linker-ΔT)的版本。有些构建体还与一种称为MIP3α的趋化因子融合,帮助将刺突蛋白递送给抗原提呈细胞——这些免疫哨兵在激活T细胞方面尤其有效。在小鼠中,这些设计可靠地诱导出强烈的CD4和CD8 T细胞反应,分泌典型的病毒抗击型“1型”炎性信使分子。其中一个构建体Linker-ΔT甚至专门设计为足以扰乱刺突蛋白的形状,从而避免强烈刺激抗体反应,同时仍能提供大量的T细胞靶点。
病毒来袭时发生了什么
当在表达人体ACE2的易感转基因小鼠模型中更严格地测试这些疫苗时,情况变得更清晰。基于ΔC的疫苗产生了能够结合多种变体的刺突蛋白及其受体结合域的抗体,但这些抗体在标准实验室中并未表现出中和活性。正如预期,Linker-ΔT构建体几乎未产生可检测的抗体,但仍引发了强劲的T细胞活性。所有这些疫苗类型的小鼠对刺突蛋白均表现出强烈的T细胞细胞因子反应。然而,当它们暴露于致死剂量的活SARS-CoV-2时,与对照动物相比,任何接种组都未能避免体重下降或死亡。
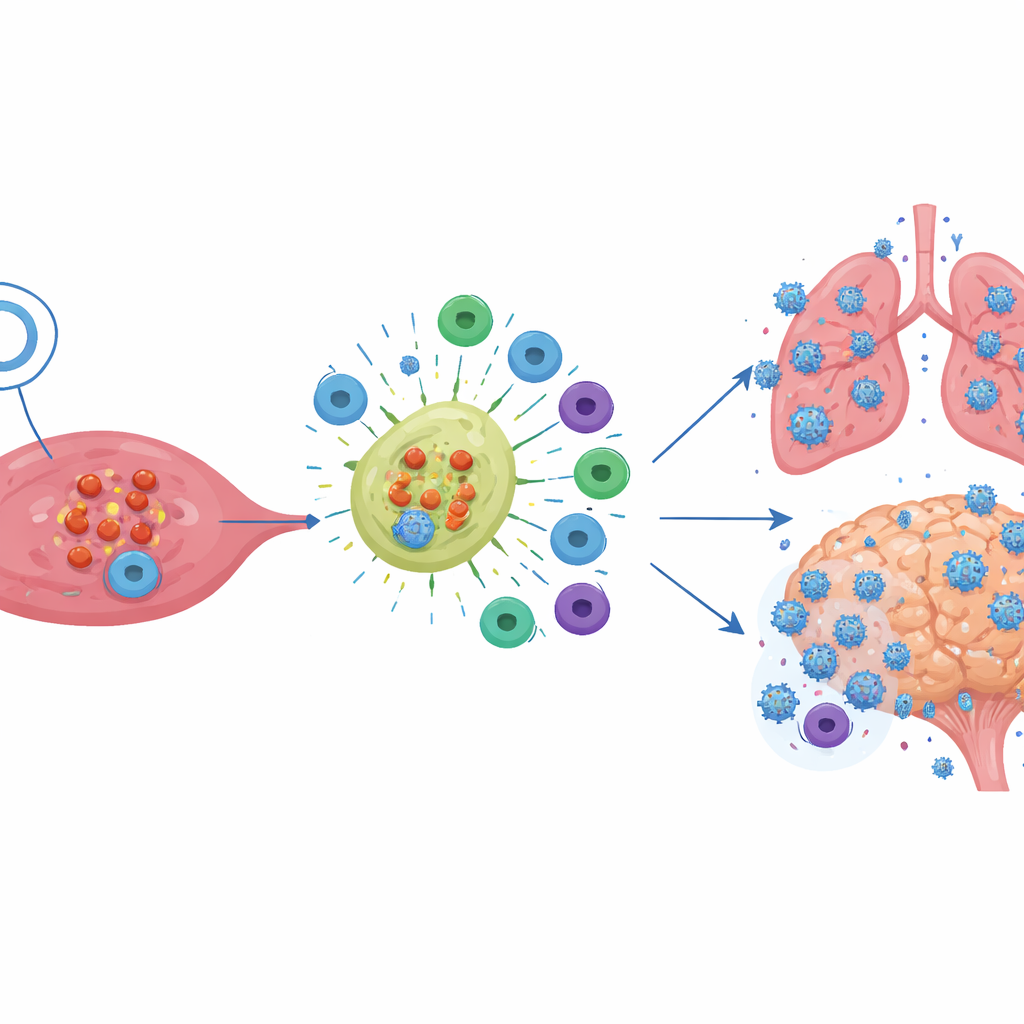
对疫苗设计的启示
这些结果与在人类和非人灵长类动物中日益增加的证据一致:中和抗体水平与疫苗预防有症状感染的效果密切相关。T细胞仍然非常重要——它们似乎有助于更快清除感染、减轻疾病严重性,并在抗体部分失效时仍对新变体保持活性。但在这个苛刻的小鼠模型中,由趋化因子融合DNA疫苗诱导的强大T细胞反应单独并不足以提供保护。作者认为,他们引入的刺突蛋白变化可能扭曲了关键的中和表位,而产生的T细胞可能缺乏最佳特性,例如恰当的组织分布或杀伤能力。
对未来的意义
对非专业读者来说,结论很明确:在这项研究中,主要训练T细胞但不产生中和抗体的疫苗未能保护小鼠免受严重COVID-19的侵害。这项工作支持了这样一种观点:最佳疫苗应同时做到两点——诱导强大且构型正确的中和抗体以阻断感染,并激发有力的T细胞反应以清除任何突破性感染。对于抗体反应受损的人群,这一点尤为重要。未来的疫苗可能会将保留中和靶位点的智能抗原设计与诸如趋化因子融合等递送技巧结合,寻求一种平衡的双管齐下的防护,而不是单靠T细胞。
引用: Cha, SC., Szymura, S.J., Anderson, A. et al. Vaccine-derived T-cell responses are insufficient to generate protective immunity to SARS-CoV-2. Sci Rep 16, 14331 (2026). https://doi.org/10.1038/s41598-026-44391-x
关键词: SARS-CoV-2疫苗, T细胞免疫, 中和抗体, DNA疫苗, COVID-19保护