Clear Sky Science · he
תגובת תאי T שמתקבלת מחיסון אינה מספיקה ליצירת חיסוניות מגוננת נגד SARS-CoV-2
מדוע המחקר הזה חשוב
כשהחיסונים נגד COVID-19 הופצו, מרבית תשומת הלב הופנתה לנוגדנים — החלבונים היכולים לחסום את הווירוס מלחדור לתאים שלנו. אולם צד אחר במערכת החיסון, תאי T, נחשב לעתים קרובות לכך שמונע מאנשים להידרש לאשפוז ומספק הגנה מתמשכת יותר. המחקר הזה שואל שאלה פשוטה אך מפתח: אם חיסון מעורר תגובות חזקות של תאי T אך מעט או ללא נוגדנים מנטרלים, האם זה מספיק כדי להגן מפני מחלה קשה של COVID-19?
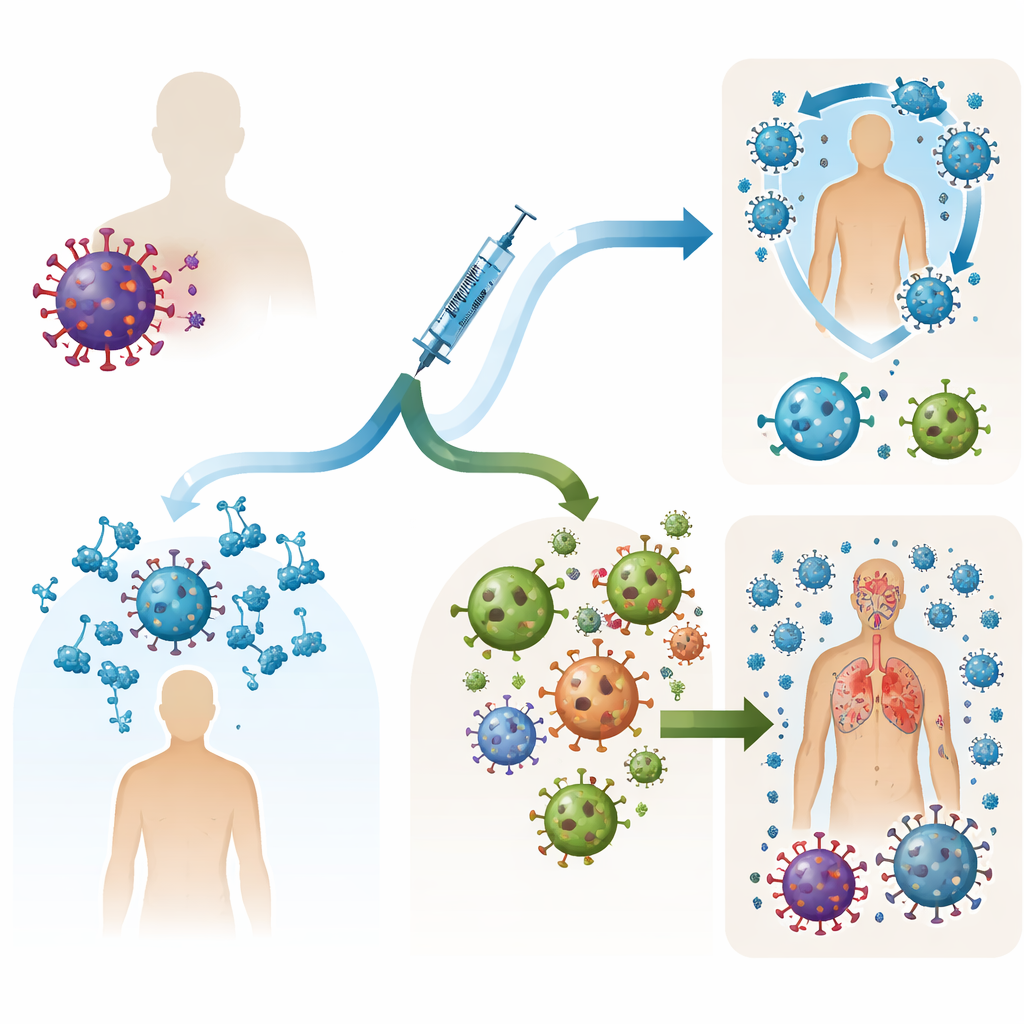
שני קווי ההגנה העיקריים
מערכת החיסון שלנו נלחמת בוירוסים בשתי דרכים רחבות. נוגדנים מסתובבים בדם ובבלוטות הריר ומתחברים לוירוסים לפני שהם נכנסים לתאים. נוגדנים מנטרלים הם עוצמתיים במיוחד כי הם חוסמים מבנים מרכזיים שהווירוס משתמש בהם כדי לפלוש. תאי T, לעומת זאת, סורקים רקמות בחיפוש אחר תאים שכבר נדבקו והורסים אותם, ובכך עוזרים להגביל את התפשטות הזיהום. מטופלים רבים שאינם יכולים לייצר נוגדנים טובים — למשל אלה עם סוגי סרטן דם מסוימים או הנוטלים תרופות המדכאות תאי B — עדיין מפתחים תגובות תאי T לאחר חיסון. זה עורר תקווה כי חיסון המתמקד ב־T עשוי להגן על אנשים שתגובת הנוגדנים שלהם חלשה.
עיצוב חיסונים שמקדמים תאי T
צוות המחקר השתמש בחיסוני DNA, פלטפורמה שבה קטעי DNA מעגליים קטנים מנחים תאים לייצר חלבוני וירוס. הם תכננו מספר גרסאות של חלבון ה־Spike של SARS‑CoV‑2, כולל אחת עם זנב מקוצר (ΔC) ואחת עם הסרת אזורי חיתוך חיוניים והכנסת מקשר גמיש (Linker‑ΔT). חלק מהגרסאות הותכו לכימוקין הנקרא MIP3α, שעוזר להעביר את חלבון ה‑Spike לתאים מציגי אנטיגן — שומרים חיסוניים שמצטיינים בהפעלת תאי T. בעכברים, העיצובים הללו עוררו באופן אמין תגובות חזקות של תאי CD4 ו‑CD8 שהפרישו מולקולות דלקתיות אופייניות לתגובה מסוג "סוג 1" המלחמת בוירוסים. אחד המבנים, Linker‑ΔT, נבנה במיוחד כדי לשבש את הצורה של ה‑Spike במידה שמקטינה את גירוי הנוגדנים אך עדיין מציגה שפע יעדי תאי T.
מה קרה כשהווירוס תקף
כאשר החיסונים נבחנו בקפדנות במודל עכבר טרנסגני שמבטא את מקבל ה‑ACE2 האנושי — אותו רצפטור שבו משתמש SARS‑CoV‑2 בבני אדם — התמונה הובהרה. החיסונים המבוססים על ΔC ייצרו נוגדנים שיכלו להיקשר ל‑Spike ולדומיין הקושר הרצפטור ממספר וריאנטים, אבל נוגדנים אלה לא נטרלו את הווירוס בבדיקות מעבדה סטנדרטיות. העיצובים של Linker‑ΔT, כמתוכנן, ייצרו כמעט אפס נוגדנים ניתנים לזיהוי אך עדיין הפעילו פעילות תאי T חזקה. בכל סוגי החיסונים הללו, העכברים הראו תגובות ציטוקין חזקות של תאי T נגד ה‑Spike. ועדיין, כאשר נחשפו למנת מוות של SARS‑CoV‑2 חי, אף אחת מהקבוצות המחוסנות לא עמדה בהגנה מפני אובדן משקל או מוות בהשוואה לבעלי החיים בקבוצת הביקורת.
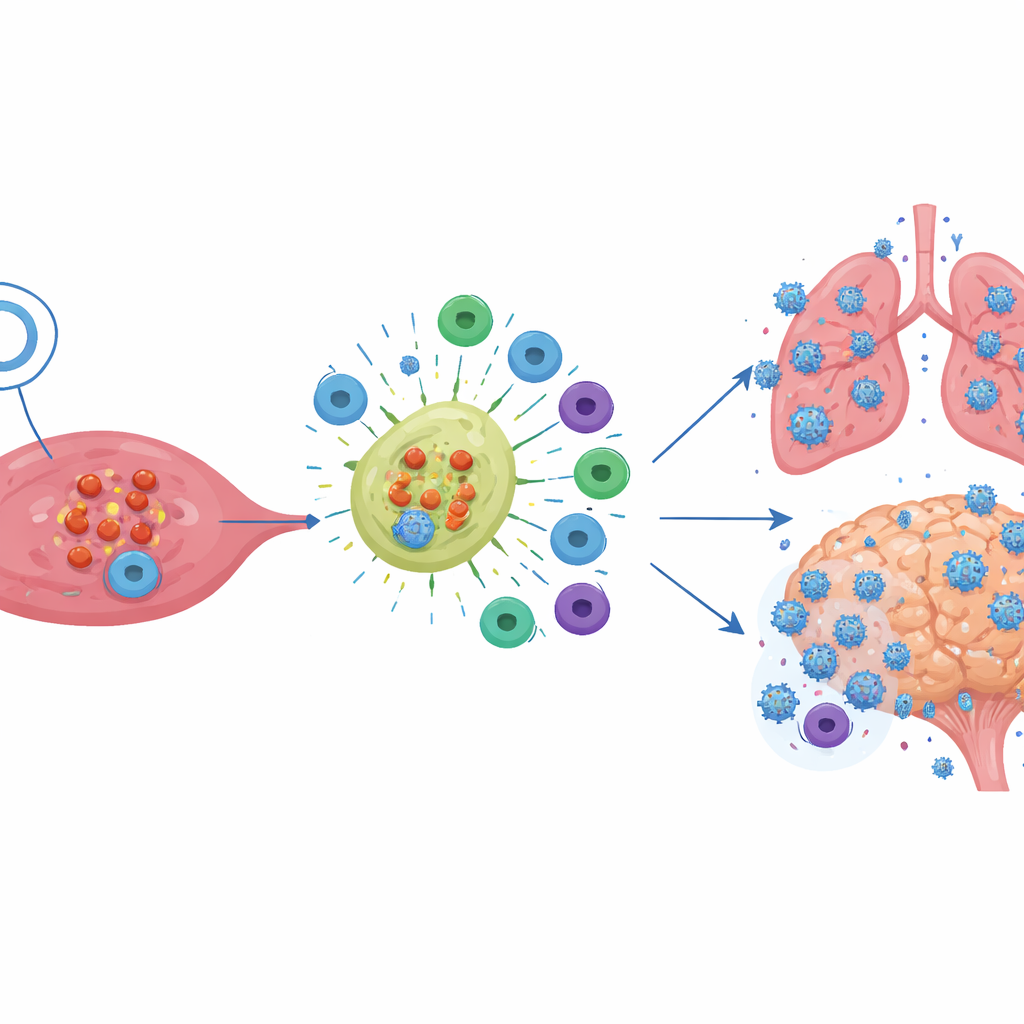
מסקנות לעיצוב חיסונים
תוצאות אלה תואמות גוף גדל של עדויות בבני אדם ובעכברים לא־אנושיים: רמות נוגדנים מנטרלים מתאימות היטב ליכולתם של חיסונים למנוע זיהום סימפטומטי. תאי T עדיין חשובים מאוד. הם נראים כעוזרים לנקות זיהום מהר יותר, להפחית את חומרת המחלה ולהישאר פעילים נגד וריאנטים חדשים גם כאשר הנוגדנים מאבדים חלק מהאפקטיביות שלהם. אך במודל העכבר הקפדני הזה, תגובות תאי T חזקות שנגרמו על ידי חיסוני DNA המוּחבלים בכימוקין לא הספיקו כשלעצמן. המחברים טוענים ששינויים מסוימים ב‑Spike שהכניסו ככל הנראה עיוותו תכונות ניטרול מפתח וייתכן שתאי ה‑T שנוצרו חסרו תכונות מיטביות כמו התפלגות רקמתית מתאימה או יכולת הרג מספקת.
מה משמעות הדבר להמשך
לציבור הרחב, המסקנה ברורה: חיסון שמאמן בעיקר תאי T, ללא יצירת נוגדנים מנטרלים, לא הגן על עכברים מפני מחלה קשה של COVID‑19 במחקר זה. העבודה תומכת ברעיון שהחיסונים הטובים ביותר צריכים לשאוף לשלב את שני המרכיבים — לעורר נוגדנים חזקים ומעוצבים נכון החוסמים זיהום ותגובות תאי T איתנות שעוזרות לנקות כל וירוס שעובר את החסימה. זה רלוונטי במיוחד לאנשים שתגובות הנוגדנים שלהם מוחלשות. חיסונים עתידיים עשויים לשלב עיצוב אנטיגן חכם ששומר על מטרות ניטרול יחד עם תחבולות משלוח כמו היתוך כימוקין, בחיפוש אחר מגן מאוזן דו‑זרועי במקום להסתמך על תאי T בלבד.
ציטוט: Cha, SC., Szymura, S.J., Anderson, A. et al. Vaccine-derived T-cell responses are insufficient to generate protective immunity to SARS-CoV-2. Sci Rep 16, 14331 (2026). https://doi.org/10.1038/s41598-026-44391-x
מילות מפתח: חיסוני SARS-CoV-2, חיסון בתאי T, נוגדנים מנטרלים, חיסוני DNA, הגנה מפני COVID-19